frança farmacêutica cro mercado tamanho e previsão
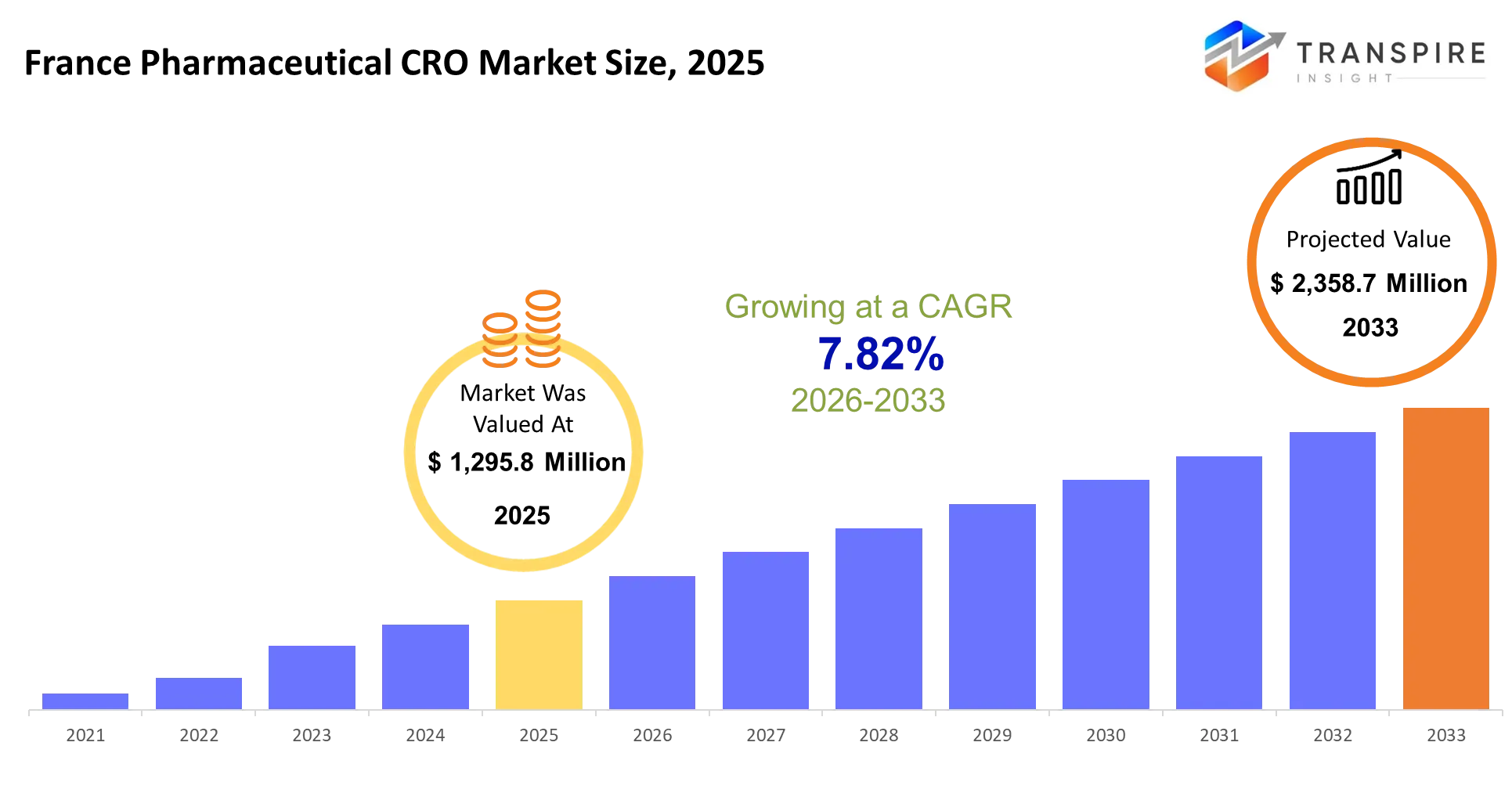
- frança farmacêutica cro tamanho do mercado 2025: usd 1,295,8 milhões
- frança farmacêutica cro tamanho do mercado 2033: usd 2,358,7 milhões
- França farmacêutica cro mercado cagr: 7,82%
- França segmentos de mercado: por tipo (pesquisa clínica, pesquisa pré-clínica, serviços laboratoriais, outros); por aplicação (desenvolvimento de drogas, ensaios clínicos, estudos toxicológicos, gerenciamento de dados, outros); por usuário final (empresas farmacêuticas, empresas de biotecnologia, institutos de pesquisa, outros); por fase (fase i, fase ii, fase iii, fase iv, outros)
para saber mais sobre este relatório, baixar relatório de amostra grátis
França farmacêutico cro resumo do mercado
o mercado de cro farmacêutica da frança foi avaliado em 1,295,8 milhões de usd em 2025. espera-se atingir a usd 2.358,7 milhões até 2033, crescendo em um cagr de 7,82%. as organizações de pesquisa contratual fornecem serviços de pesquisa terceirizados às empresas farmacêuticas e de biotecnologia, tratando de tudo, desde estudos pré-clínicos até a fase iv de vigilância pós-comercialização. os serviços de pesquisa clínica são responsáveis por 65% do mercado francês, pois os patrocinadores preferem transferir a gestão de ensaios complexos para fornecedores especializados em vez de manter capacidades internas em múltiplas áreas terapêuticas e jurisdições regulatórias.
três mudanças regulatórias entre 2020 e 2025 reformularam a forma como os cros franceses operam. primeiramente, a regulamentação de ensaios clínicos da eu introduziu processos de aprovação harmonizados entre os estados membros, o que reduziu a variabilidade temporal, mas aumentou os requisitos de documentação inicial. em segundo lugar, a plataforma nacional de dados de saúde de france abriu acesso a conjuntos de dados de evidências do mundo real que os patrocinadores agora podem se vincular aos resultados de ensaios clínicos, criando demanda por cros com capacidades bioinformáticas. em terceiro lugar, o ansm passou a aceitar protocolos descentralizados que permitem o monitoramento remoto do paciente, o que desviou a seleção do local do investigador das redes hospitalares tradicionais para provedores de saúde domiciliar e plataformas de telemedicina.
a atual expansão do mercado é impulsionada por empresas biotecnológicas externalizando o trabalho de desenvolvimento em estágio tardio que anteriormente realizavam internamente. as pequenas e médias empresas de biotecnologia carecem da expertise regulatória para navegar nas submissões de ema e na rede de sites para executar ensaios de fase iii multipaíses de forma eficiente. os cros oferecem a essas empresas acesso a relações estabelecidas de pesquisadores, expertise em área terapêutica e especialistas em assuntos regulatórios em uma base de projeto e não como headcount permanente. este modelo de negócio permite que os patrocinadores de biotecnologia preservem o dinheiro, ao mesmo tempo que aceleram os prazos de desenvolvimento, o que importa quando os ciclos de financiamento de empreendimentos exigem progresso clínico demonstrável a cada 18 a 24 meses.
chave frança farmacêutico cro insights mercado
- os serviços de pesquisa clínica dominam o mercado de cro farmacêutica frança com participação de 65% em 2024, impulsionado pelo aumento da externalização da fase ii e fase iii do manejo experimental.
- os serviços de pesquisa pré-clínica são responsáveis por 22% do mercado em 2024, apoiando candidatos a medicamentos em fase inicial que requerem testes toxicológicos e estudos farmacocinéticos.
- as aplicações de desenvolvimento de medicamentos representam 41,3% da demanda de serviços de cro em 2024, uma vez que as empresas farmacêuticas terceirizam o desenvolvimento de formulações e testes de estabilidade.
- as aplicações de ensaios clínicos possuem 38,7% de market share em 2024, concentradas em áreas terapêuticas de oncologia, imunologia e doenças raras onde o recrutamento de pacientes é desafiador.
- as empresas farmacêuticas constituem 52,8% da demanda do usuário final em 2024, outsourcing de atividades de desenvolvimento clínico não essenciais para focalizar recursos internos na descoberta e comercialização.
- as empresas de biotecnologia representam 31,4% do mercado em 2024 e representam o segmento de usuários finais de crescimento mais rápido, expandindo-se em 9,1% cagr até 2033.
- ensaios de fase iii geram 43,2% da receita de pesquisas clínicas em 2024, exigindo grandes populações de pacientes e longos períodos de monitoramento que favorecem o full-service cros.
- ensaios de fase ii contribuem com 28,6% de receita em 2024, com crescente demanda por projetos adaptativos de ensaios que exijam recursos especializados em estatística e gerenciamento de dados.
- a iqvia detém aproximadamente 15-18% do mercado francês de cro em 2025, alavancando seus serviços integrados de análise de dados e ensaios clínicos em múltiplas áreas terapêuticas.
- a labcorp expandiu suas operações de desenvolvimento clínico francês em 20% em 2024, acrescentando locais de investigação e especialistas em área terapêutica para atender a crescente demanda de biotecnologia.
quais são os principais condutores, restrições e oportunidades no mercado de produtos farmacêuticos da frança?
o principal impulsionador do crescimento é que as empresas farmacêuticas passam da terceirização seletiva para parcerias estratégicas onde os cros gerenciam programas de desenvolvimento inteiros e não estudos individuais. grandes firmas farmacêuticas agora adjudicam contratos multi-anuais que abrangem pré-clínicos por meio de trabalho de fase iii para áreas terapêuticas específicas, o que proporciona visibilidade de receita aos cros e lhes permite investir em capacidades especializadas como registros de pacientes com doenças raras ou plataformas de biomarcadores oncológicos. o iqvia, sineos health e parexel estruturaram suas operações francesas em torno dessas parcerias estratégicas, dedicando equipes a contas específicas de patrocinadores ao invés de operarem como prestadores de serviços transacionais. o impacto financeiro é substancial: os contratos de parceria estratégica normalmente duram de três a cinco anos e cobrem carteiras de desenvolvimento no valor de centenas de milhões de euros, em comparação com contratos de estudo único que duram de 18 a 36 meses.
a restrição mais significativa é a limitação da capacidade do local de investigação em áreas terapêuticas de alta demanda. centros de oncologia franceses e especialistas em imunologia são supersubscritos com protocolos experimentais, o que cria gargalos de recrutamento de pacientes que atrasam as linhas do tempo do estudo, independentemente de quão eficiente o cro gerencia outros aspectos da execução do teste. cros não pode simplesmente abrir novos sites para resolver este problema, pois investigadores qualificados exigem anos de treinamento e certificação regulatória. a restrição é particularmente aguda em ensaios de doenças raras onde a frança pode ter apenas cinco a dez centros com populações de pacientes relevantes, e esses centros já estão comprometidos com múltiplos protocolos concorrentes. isso obriga o cros a ampliar a linha do tempo de recrutamento ou a expandir-se para locais de investigação menos experientes, um dos quais aumenta os custos e os riscos para a qualidade do estudo.
a oportunidade mais clara está nos serviços de evidências do mundo real que conectam dados de ensaios clínicos à base de dados nacional de saúde da frança. a ansm agora aceita evidências do mundo real para apoiar submissões regulatórias para determinadas indicações, e os patrocinadores precisam de cros que possam projetar estudos híbridos combinando metodologia tradicional de ensaios clínicos randomizados controlados com dados observacionais de registros eletrônicos de saúde. isso requer capacidades que a maioria dos cros não possui atualmente: cientistas de dados que entendem de análise de saúde, especialistas reguladores que sabem estruturar submissões de evidências no mundo real e relações estabelecidas com autoridades francesas de dados de saúde. cros que constroem essas capacidades irão capturar trabalhos de alta margem que não podem ser facilmente replicados por concorrentes que carecem da infraestrutura técnica e expertise regulatória para executar esses projetos de estudo híbridos.
qual o impacto da inteligência artificial no mercado de cro farmacêutico da frança?
os sistemas de identificação de pacientes ai-powered passam a rastrear registros eletrônicos de saúde para encontrar candidatos que atendam a critérios específicos de inclusão no estudo, o que acelera as linhas do tempo de recrutamento, identificando pacientes elegíveis antes dos sites revisarem manualmente gráficos. iqvia e labcorp implantaram modelos de aprendizado de máquina em sistemas de saúde franceses que sinalizam pacientes com base em códigos de diagnóstico, valores laboratoriais, histórico de medicamentos e outros marcadores clínicos. esses sistemas reduziram o tempo médio de triagem de semanas para dias em locais com registros eletrônicos integrados de saúde, embora a adoção permaneça limitada a redes hospitalares maiores com dados digitalizados de pacientes. o benefício operacional é mais visível em ensaios de doenças raras, onde a revisão manual de prontuários exigiu meses de tempo do investigador para identificar até mesmo um punhado de pacientes elegíveis.
o processamento de linguagem natural automatiza o monitoramento de segurança, extraindo eventos adversos de notas clínicas, laudos laboratoriais e diários de pacientes, sem necessidade de entrada manual de dados pelos coordenadores do local. sineos health e icon têm implementado sistemas nlp que continuamente escaneiam a documentação de ensaios para sinais de segurança, sinalizando potenciais eventos adversos graves que exigem notificação imediata às autoridades reguladoras. esta automação reduziu o tempo mediano de notificação de eventos adversos de 48-72 horas para menos de 24 horas em locais que utilizam a tecnologia, o que importa quando os requisitos regulamentares obrigam a relatar eventos adversos graves no prazo de 24 horas após a conscientização do investigador. a limitação é que a acurácia do nlp depende da qualidade da documentação, e as notas clínicas francesas muitas vezes incluem terminologia médica abreviada e não padronizada que reduzem a confiabilidade da extração automatizada.
a principal barreira à adoção mais ampla da ai é a fragmentação de dados entre os profissionais de saúde franceses. os registros dos pacientes permanecem siloados dentro de sistemas hospitalares individuais, redes regionais de saúde e práticas privadas, o que impede que os cros treinem modelos de ai em conjuntos de dados abrangentes que refletem populações de pacientes do mundo real. adicionalmente, as normas francesas de proteção de dados exigem o consentimento explícito do paciente para o uso secundário de dados de saúde em contextos de pesquisa, o que adiciona o cumprimento de procedimentos gerais que muitos cros consideram proibitivos para projetos de desenvolvimento de ai. isso cria um paradoxo onde as aplicações de ai mais valiosas exigem grandes e diversos conjuntos de dados que os marcos regulatórios franceses dificultam a montagem legal.
tendências fundamentais do mercado
- os patrocinadores farmacêuticos passaram da compra de serviços transacionais para parcerias estratégicas multianuais entre 2022 e 2024, consolidando relações de cinco ou seis fornecedores para dois ou três provedores preferenciais.
- a adoção descentralizada do estudo acelerou em 2023 quando a ansm publicou orientações aceitando o monitoramento remoto do paciente e as visitas domiciliares de saúde como alternativas válidas para avaliações baseadas no local.
- as empresas de biotecnologia aumentaram a terceirização de uma média de 60% dos gastos de desenvolvimento em 2021 para mais de 75% em 2024, impulsionados pela pressão de capital de risco para minimizar custos fixos.
- a saúde do iqvia e dos sineos expandiu seus especialistas em área terapêutica francesa em 25-30% entre 2023 e 2025, contratando especialistas em oncologia e doenças raras para apoiar contratos de parceria estratégica.
- os serviços de evidências do mundo real surgiram como uma oferta distinta em 2024, com cros estabelecendo equipes dedicadas ao projeto de estudos híbridos combinando dados experimentais e registros observacionais de saúde.
- os cronogramas de recrutamento de pacientes para ensaios oncológicos aumentaram de 12 meses para 16-18 meses entre 2022 e 2024 devido às restrições de capacidade do local do investigador e protocolos concorrentes.
- os cros chineses entraram no mercado francês em 2024, oferecendo serviços de fase i e fase ii inicial a 20-25% abaixo dos preços históricos para estabelecer operações europeias.
- os serviços de gerenciamento de dados cresceram mais rapidamente do que o monitoramento clínico entre 2023 e 2025, refletindo o aumento da demanda de patrocinadores por análises avançadas e visualização de dados em tempo real durante os ensaios.
frança farmacêutica cro mercado segmentação
por tipo
os serviços de pesquisa clínica dominam o mercado francês de cro a 65% da receita total. este segmento abrange o recrutamento de pacientes, monitoramento do local, coleta de dados e suporte de submissão regulatória para a fase i através de ensaios clínicos de fase iv. a dominância reflete uma mudança estrutural em que patrocinadores farmacêuticos e biotecnológicos externalizam o gerenciamento de ensaios para cros ao invés de manter equipes de operações clínicas internas. cros full-service como iqvia, labcorp, and syneos health operam como braço de desenvolvimento clínico do patrocinador, gerenciando relacionamentos de investigadores, interações regulatórias e supervisão da qualidade de dados em múltiplos ensaios simultâneos. a proposta de valor é a transferência de risco: patrocinadores pagam cros para entregar os pacientes cadastrados e dados limpos no cronograma, enquanto o cro absorve a complexidade operacional e variabilidade temporal.
os serviços de pesquisa pré-clínica são responsáveis por 22% do mercado, englobando estudos toxicológicos, análise farmacocinética e desenvolvimento de formulações que ocorrem antes de ensaios em humanos. este segmento atende empresas de biotecnologia em fase inicial e equipes de descoberta farmacêutica que necessitam de capacidades laboratoriais especializadas sem construir instalações dedicadas. charles river, covance e eurofins dominam os serviços pré-clínicos franceses através da propriedade de laboratórios certificados pelo glp equipados para estudos regulatórios de toxicologia. o segmento é tecnicamente exigente, pois estudos pré-clínicos devem atender normas regulatórias rigorosas para a qualidade e reprodutibilidade dos dados, o que requer métodos analíticos validados e experimentados. laboratório cientistas. as margens são superiores às pesquisas clínicas, pois os custos de mudança são substanciais uma vez que um patrocinador qualifica um laboratório específico para um programa de desenvolvimento.
os serviços de laboratório e outras ofertas especializadas representam em conjunto 13% do mercado. isso inclui testes bioanalíticos, serviços de laboratório central para ensaios clínicos e capacidades de nicho como testes de dispositivos médicos ou validação de saúde digital. o segmento cresceu mais rápido que a pesquisa clínica central entre 2023 e 2025, pois os patrocinadores necessitam cada vez mais de serviços integrados que combinem o gerenciamento de ensaios clínicos com análises laboratoriais especializadas. por exemplo, os ensaios oncológicos muitas vezes necessitam de desenvolvimento diagnóstico droga testes, que exigem cros que possam coordenar a validação de biomarcadores, coleta de amostras clínicas e desenvolvimento de ensaios diagnósticos como um programa unificado. cros que oferecem esses serviços integrados captam maior receita por projeto do que aqueles que fornecem apenas gerenciamento de ensaios clínicos.
para saber mais sobre este relatório, baixar relatório de amostra grátis
por aplicação
as aplicações de desenvolvimento de drogas levam a 41,3% da demanda do mercado, abrangendo o desenvolvimento de formulações, testes de estabilidade, desenvolvimento de métodos analíticos e serviços de suporte à fabricação. as empresas farmacêuticas terceirizam essas atividades para cros quando as funções de desenvolvimento interno carecem de capacidade ou especialização para desafios específicos de formulação. por exemplo, o desenvolvimento de formulações estáveis para biologics requer equipamentos especializados e expertise que a maioria dos patrocinadores não mantêm internamente. cros como catalent, patheon e lonza fornecem essas capacidades em uma base contratual, permitindo que patrocinadores avancem com candidatos através do desenvolvimento sem investimento de capital em laboratórios de formulação. a aplicação é de margem-acretiva porque o trabalho de desenvolvimento de formulações é tecnicamente complexo e requer cientistas experientes que comandam taxas de faturamento premium.
as aplicações de ensaios clínicos são responsáveis por 38,7% da demanda, focadas especificamente nos serviços de registro de pacientes, gerenciamento de sites e execução de ensaios, em vez de suporte de desenvolvimento mais amplo. este segmento difere dos serviços de pesquisa clínica na medida em que capta apenas o componente de execução experimental, excluindo estratégia regulatória, análise de dados e atividades pós-julgamento. a aplicação cresceu entre 2022 e 2024, uma vez que as empresas de biotecnologia buscaram cros que pudessem lidar com o recrutamento de pacientes e monitoramento do local, mantendo outras atividades de desenvolvimento internamente. essa desagregação permitiu que os patrocinadores externalizassem os aspectos operacionais mais complexos e sensíveis à linha do tempo do desenvolvimento clínico, preservando o controle sobre decisões estratégicas como seleção de endpoints e design de ensaios.
estudos toxicológicos, gerenciamento de dados e outras aplicações em conjunto representam 20% do mercado. estudos toxicológicos são obrigatórios para submissão regulatória e requerem instalações certificadas pelo glp que a maioria dos patrocinadores não operam internamente. os serviços de gerenciamento de dados têm crescido rapidamente à medida que os ensaios geram volumes crescentes de dados eletrônicos a partir de wearables, dispositivos de monitoramento remoto e resultados relatados pelo paciente que requerem plataformas de banco de dados especializadas e capacidades de análise estatística. cros que investiram em plataformas de dados baseadas em nuvem e análises em tempo real entre 2020 e 2025 capturaram crescente demanda de patrocinadores para monitoramento de testes transparentes e projetos de testes adaptativos que exigem análise contínua de dados em vez de bancos de dados tradicionais analisados apenas na conclusão do estudo.
pelo utilizador final
as empresas farmacêuticas constituem 52,8% da demanda de cro na frança. grandes empresas farmacêuticas terceirizam programas de desenvolvimento específico onde a capacidade interna é restrita ou a área terapêutica é carente. por exemplo, uma empresa com fortes capacidades oncológicas pode externalizar o desenvolvimento de doenças raras para cros com registros de pacientes estabelecidos e redes de investigadores nessas indicações. a decisão de terceirização é impulsionada economicamente: a manutenção de operações clínicas internas para áreas terapêuticas onde a empresa realiza apenas um ou dois ensaios por ano é proibitiva de custos em comparação com o envolvimento de cros em uma base de projeto. isso cria uma demanda estável de cros em áreas terapêuticas onde o interesse do patrocinador é sustentado, mas os portfólios individuais da empresa são limitados.
as empresas de biotecnologia representam 31,4% do mercado e representam o segmento de crescimento mais rápido em 9,1% cagr até 2033. essas empresas normalmente carecem de capacidade de desenvolvimento clínico interno e externalizam a maioria dos trabalhos de desenvolvimento a partir de estudos pré-clínicos através de ensaios de fase iii. o motor de crescimento é a dinâmica de financiamento de capital de risco: espera-se que as empresas de biotecnologia demonstrem progresso clínico rapidamente, minimizando a queima de dinheiro, o que torna a terceirização para cros mais atrativa financeiramente do que a construção de capacidades internas que exigem contagem fixa de cabeças. Os cros fornecem aos patrocinadores de biotecnologia uma capacidade flexível que varia com as necessidades do programa, faturando apenas para projetos ativos ao invés de exigir pagamentos contínuos de retentor ou funcionários assalariados.
os institutos de investigação e outros utilizadores finais contribuem 15,8% da procura. centros médicos acadêmicos e organizações governamentais de pesquisa envolvem cros para estudos iniciados por pesquisadores e estudos de saúde pública que exigem coleta e monitoramento de dados de nível regulatório. esses clientes normalmente operam no financiamento de subsídios com orçamentos fixos e cronogramas definidos, o que requer que a cros preste serviços dentro de restrições de custos rígidas. o segmento oferece margens mais baixas do que o trabalho farmacêutico comercial, mas fornece aos cros acesso a novas abordagens terapêuticas e populações de pacientes com doenças raras que posteriormente se traduzem em oportunidades de desenvolvimento comercial quando descobertas acadêmicas avançam em direção à aprovação regulatória e comercialização.
por fase
ensaios de fase iii geram 43,2% da receita de pesquisas clínicas devido às suas grandes populações de pacientes, períodos de monitoramento prolongados e exigências regulatórias complexas. um ensaio típico de fase iii em oncologia na frança pode incluir 300-500 pacientes em 25-40 locais de investigação ao longo de três a quatro anos, exigindo monitoramento do local, gerenciamento de dados, relatórios de segurança e coordenação regulatória durante todo o período do estudo. os cros fornecem valor ao gerenciar essa complexidade operacional, permitindo que os patrocinadores se concentrem em decisões estratégicas em torno do design de julgamentos e submissões regulatórias. a concentração de receita na fase iii reflete tanto o custo direto da execução de testes em larga escala quanto o custo dos patrocinadores do prêmio de risco para entregar cros em prazos de inscrição agressivos que determinam datas de lançamento do produto.
ensaios de fase ii contribuem com 28,6% de receita, com foco em estudos de determinação de dose e avaliações iniciais de eficácia em populações de pacientes menores. estes ensaios utilizam cada vez mais projetos adaptativos que modificam critérios de matrícula ou esquemas de dosagem baseados em resultados provisórios, o que requer cros com fortes capacidades estatísticas e de gerenciamento de dados. a complexidade técnica de ensaios adaptativos cria barreiras à entrada de menores cros que carecem de expertise especializada, permitindo maiores provedores de serviços completos para comandar preços premium. o trabalho de fase ii é estrategicamente importante para cros, pois patrocinadores que completam com sucesso a fase ii tipicamente continuam com o mesmo cro na fase iii, criando oleodutos de receita multi-ano desde o início do engajamento.
a fase i, a fase iv e outras fases experimentais juntas representam 28,2% das receitas. ensaios de fase i são relativamente pequenos, mas tecnicamente exigentes, necessitando de instalações especializadas para estudos de segurança em primeiro lugar em humanos e monitoramento intensivo de pacientes. estudos de fase iv pós-comercialização estão crescendo como reguladores cada vez mais requerem evidências do mundo real para complementar dados clínicos pré-aprovação. cros que oferecem tanto o gerenciamento de testes de fase iv tradicional quanto as capacidades de evidências do mundo real, combinando dados experimentais com registros observacionais de saúde, estão captando crescente demanda de patrocinadores por programas integrados de vigilância pós-comercialização que atendem aos requisitos regulatórios, gerando evidências para negociações de reembolso do pagador e desenvolvimento de diretrizes clínicas.
quais são os principais casos de uso que impulsionam o mercado de cro farmacêutica da frança?
a aplicação primária é o gerenciamento experimental de fase iii de serviço completo para empresas de biotecnologia que não possuem capacidade de operações clínicas internas. esses patrocinadores envolvem cros para lidar com todos os aspectos da execução do julgamento a partir da seleção do site através de bloqueio de banco de dados, submissão regulatória e monitoramento de segurança pós-aprovação. um engajamento típico pode envolver uma indicação de doenças raras em que o patrocinador da biotecnologia tenha completado estudos de fase ii de comprovação de conceito e precise de um cro para executar o programa de fase iii fundamental necessário para a aprovação do ema. o cro fornece redes de sites de pesquisadores, expertise regulatória, estratégias de recrutamento de pacientes e infraestrutura de gerenciamento de dados em uma base turnkey, permitindo que a empresa de biotecnologia avance para a comercialização sem a construção de operações clínicas permanentes.
a demanda adjacente advém de grandes empresas farmacêuticas terceirizando programas de desenvolvimento de áreas terapêuticas específicas. por exemplo, uma empresa com pouca experiência em imunologia pode envolver um cro para gerenciar todo o desenvolvimento clínico para um ativo de imunologia adquirido, alavancando as relações estabelecidas do cro com pesquisadores de reumatologia e dermatologia franceses. essas parcerias estratégicas tipicamente abrangem múltiplos ensaios clínicos ao longo de vários anos, proporcionando ao cro uma receita previsível ao mesmo tempo em que concede ao patrocinador acesso à área terapêutica sem expansão permanente de pessoal. a lógica comercial é a especialização: cros que se concentram em áreas terapêuticas específicas desenvolvem relações profundas de pesquisadores e experiência de projeto de protocolo que equipes generalistas de desenvolvimento interno não podem reproduzir.
os casos de uso emergentes centram-se em projetos de ensaios híbridos combinando ensaios clínicos randomizados tradicionais com evidências do mundo real de bases de dados de saúde francesas. patrocinadores envolvem cros para projetar estudos onde o braço de controle usa pacientes pareados de registros eletrônicos de saúde em vez de se inscrever em uma coorte de placebo separada, o que reduz os custos do teste e acelera os prazos de inscrição. a iqvia e a sineos health estabeleceram equipes dedicadas à execução desses estudos híbridos, exigindo cientistas de dados, epidemiologistas e especialistas reguladores que compreendam tanto a metodologia de ensaios clínicos quanto os padrões de evidência do mundo real. a aplicação é tecnicamente exigente, mas oferece aos patrocinadores economias de custos substanciais, com alguns projetos híbridos reduzindo os custos da fase iii em 30-40% em comparação aos ensaios tradicionais totalmente matriculados.
métricas do relatório | detalhes |
valor de mercado em 2025 | USd 1,295,8 milhões |
valor de mercado em 2026 | USd 1.392,6 milhões |
Previsões de receitas em 2033 | 2,358,7 milhões de dólares |
taxa de crescimento | cagr de 7,82% de 2026 a 2033 |
ano de base | 2025 |
dados históricos | 2021 – 2024 |
período de previsão | 2026 – 2033 |
cobertura do relatório | previsão de receitas, paisagem competitiva, factores de crescimento e tendências |
âmbito regional | frança |
empresas-chave com perfil | iqvia, labcorps, syneos health, parexel, icon plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat |
escopo de personalização | personalização de relatório livre (espeço regional e segmento). Aproveite opções de compra personalizadas para atender às suas necessidades de pesquisa exatas. |
reportar segmentação | por tipo (pesquisa clínica, pesquisa pré-clínica, serviços laboratoriais, outros); por aplicação (desenvolvimento de drogas, ensaios clínicos, estudos toxicológicos, gerenciamento de dados, outros); por usuário final (empresas farmacêuticas, empresas de biotecnologia, institutos de pesquisa, outros); por fase (fase i, fase ii, fase iii, fase iv, outros) |
o que está impulsionando o crescimento no mercado de cro farmacêutico frança?
a frança oferece três vantagens estruturais que outros mercados europeus não podem replicar em escala equivalente. primeiramente, o país opera um sistema centralizado de saúde com registros eletrônicos abrangentes de saúde abrangendo mais de 65 milhões de cidadãos, proporcionando aos cros capacidades de identificação de pacientes e acesso a evidências do mundo real que sistemas de saúde fragmentados não podem corresponder. em segundo lugar, a frança mantém concentrações densas de sítios de pesquisadores especializados em paris, lyon e marseille, onde centros médicos acadêmicos, hospitais de ensino e institutos de pesquisa se agrupam dentro da proximidade geográfica, o que simplifica a logística experimental e reduz os custos de monitoramento em relação às redes de sítios geograficamente dispersas. em terceiro lugar, o ansm estabeleceu prazos previsíveis de revisão regulatória e orientações claras sobre metodologias de testes emergentes, como protocolos descentralizados e evidências do mundo real, o que reduz a incerteza dos patrocinadores no planejamento de programas de desenvolvimento multi-ano.
a dinâmica competitiva na frança difere de outros mercados europeus, pois as exigências linguísticas e regulatórias criam barreiras naturais para a entrada de não-eu cros. protocolos de julgamento, documentos de consentimento informado e submissões regulatórias devem estar em francês, o que requer pessoal local dedicado ao invés de equipes europeias centralizadas operando em inglês. adicionalmente, os regulamentos franceses de proteção de dados impõem requisitos específicos para o tratamento de dados de saúde que diferem das disposições gerais do gdpr, exigindo que o cros mantenha programas de conformidade específicos da frança. essas barreiras protegem atores estabelecidos como iqvia, labcorp e sineos de saúde que atuam na frança há décadas e investem em infraestrutura local, ao mesmo tempo que criam maiores custos de entrada para novos concorrentes que tentam estabelecer operações francesas.
o segmento de demanda mais rápido é o de ensaios de doenças raras, onde o banco de dados nacional de saúde da frança permite rápida identificação de pacientes para indicações ultra-raras. em condições que afetam menos de 1.000 pacientes franceses, o recrutamento tradicional baseado no site pode levar anos, pois os investigadores devem rastrear manualmente os prontuários para identificar candidatos elegíveis. cros que estabeleceram acordos de acesso de dados com autoridades de saúde francesas podem rastrear toda a população nacional de pacientes eletronicamente, identificando pacientes elegíveis em semanas ao invés de meses. essa capacidade tem feito da frança um local preferencial para ensaios europeus de doenças raras, com patrocinadores cada vez mais escolhendo sites franceses como países líderes em estudos multinacionais em indicações ultra-raras onde a velocidade de identificação do paciente determina cronogramas gerais do programa.
quem são os principais atores no mercado de cro farmacêutico frança e como eles competem?
o mercado francês de cro opera como uma estrutura de duas camadas. iqvia, labcorp, sineos health, parexel e icon possuem, coletivamente, cerca de 55-60% de market share e competem como provedores de serviços completos oferecendo capacidades integradas desde a fase pré-clínica até a fase iv. estas empresas competem na área terapêutica expertise, redes de sites de investigadores e plataformas de tecnologia que proporcionam aos patrocinadores visibilidade experimental em tempo real. cros mid-tier e menor ocupam nichos especializados baseados em foco terapêutico, tipo de serviço ou presença regional, tipicamente em parceria com cros maiores em programas complexos em vez de competir diretamente por contratos de serviço integral.
o iqvia compete por meio de sua plataforma integrada de dados e serviços clínicos que combina o gerenciamento de testes com capacidades de evidência do mundo real. a empresa opera o maior banco de dados de saúde comercial da frança abrangendo dados de prescrição, registros de alta hospitalar e informações de reclamações, que utiliza para identificação de pacientes, seleção de locais e avaliações de viabilidade. o iqvia expandiu suas operações clínicas francesas em 25% entre 2023 e 2025, somando especialistas em área terapêutica em oncologia, doenças raras e imunologia para apoiar contratos de parceria estratégica com grandes patrocinadores de farmacologia. a empresa diferencia-se em capacidades analíticas, fornecendo aos patrocinadores modelos preditivos de matrícula e análises comparativas de eficácia que cros menores não podem se replicar sem ativos de dados equivalentes.
a labcorp compete por meio da integração vertical de serviços de laboratório e gestão de ensaios clínicos, permitindo que a empresa ofereça aos patrocinadores programas unificados que combinem execução experimental com testes laboratoriais centrais, análise de biomarcadores e desenvolvimento diagnóstico acompanhante. esta integração é importante em ensaios de oncologia e doenças raras, onde a seleção e as avaliações farmacodinâmicas orientadas por biomarcadores requerem coordenação entre sítios clínicos e laboratórios especializados. a labcorp opera laboratórios certificados pela glp na frança que atendem tanto os patrocinadores de ensaios clínicos quanto os mercados de diagnóstico de rotina, criando economias de escala que cros puro-jogo não podem corresponder. a empresa tem como alvo os patrocinadores de biotecnologia que desenvolvem candidatos a medicina de precisão onde serviços laboratoriais e clínicos integrados reduzem a coordenação e aceleram as cronologias de desenvolvimento em comparação com o envolvimento de fornecedores separados para o gerenciamento de ensaios e testes laboratoriais.
desenvolvimentos recentes
em março de 2026, a iqvia anunciou uma parceria estratégica com um registro francês de pacientes com doenças raras para fornecer testes genéticos e dados de história natural para condições neurológicas ultra-raras. a colaboração tem como objetivo acelerar a identificação do paciente e as avaliações de viabilidade experimental para patrocinadores que desenvolvem terapias para doenças que afetam menos de 500 pacientes franceses. https://www.iqvia.com (iqvia)
em fevereiro de 2026, a labcorp expandiu suas operações de laboratório central francês com novas capacidades de teste de biomarcadores para ensaios de terapia celular e genética. as instalações processam amostras farmacodinâmicas e ensaios diagnósticos complementares para patrocinadores de terapia avançada que realizam estudos clínicos franceses. https://www.labcorp.com (labcorp)
quais insights estratégicos definem o futuro do mercado de cro farmacêutico frança?
ao longo dos próximos cinco a sete anos, a vantagem competitiva no mercado francês de cro passará de capacidades de execução operacional para plataformas de dados e tecnologia que possibilitam novas metodologias de teste. o mercado atual recompensa cros que podem se matricular rapidamente e fornecer dados limpos na programação, mas essas capacidades estão se tornando comoditizadas à medida que as ferramentas eletrônicas de captura de dados e monitoramento remoto padronizam em toda a indústria. a próxima fronteira competitiva é a integração de evidências do mundo real, a execução de testes descentralizados e a identificação de pacientes ai-powered, todos os quais requerem investimentos substanciais em tecnologia e acordos de acesso de dados que criem barreiras à entrada de concorrentes sem escala.
o risco de que as projeções de mercado possam subestimar é o cronograma de aceitação regulatória para novas metodologias experimentais. o ansm publicou orientações sobre ensaios descentralizados e evidências do mundo real, mas a revisão regulatória das submissões utilizando essas abordagens permanece limitada. se as autoridades reguladoras se mostrarem mais conservadoras na prática do que os documentos de orientação sugerem, os patrocinadores podem retardar a adoção dessas metodologias, o que reduziria a demanda por recursos de cr nessas áreas e favoreceria a execução de julgamentos tradicionais baseados em sites onde o precedente regulatório está bem estabelecido. isso beneficiaria os cros históricos com redes de sites fortes enquanto desfavoreciam novos operadores que investiram fortemente em plataformas de teste descentralizadas.
a oportunidade que permanece subprezada é a pós-aprovação de serviços de evidências do mundo real que combinam o gerenciamento de ensaios de fase iv com estudos observacionais utilizando bases de dados de saúde francesas. os pagadores exigem cada vez mais dados de eficácia do mundo real para apoiar decisões de reembolso, e os patrocinadores precisam de cros que possam projetar programas integrados que satisfaçam tanto os requisitos regulatórios de pós-comercialização quanto as necessidades de evidência do pagador. o segmento é atualmente pequeno, mas oferece margens mais elevadas do que o trabalho tradicional de fase iv, pois requer capacidades especializadas em economia de saúde, epidemiologia e análise de banco de dados que a maioria dos cros não mantém. empresas que constroem essas capacidades capturarão crescente demanda de patrocinadores para programas de geração de evidências que atendem múltiplos stakeholders ao invés de apenas satisfazer obrigações regulatórias.
Perguntas frequentes
Encontre respostas rápidas para as perguntas mais comuns.
espera-se que o mercado de cro farmacêutica da frança atinja a usd 2.358,7 milhões até 2033.
segmentos fundamentais para o mercado de cro farmacêutica frança são por tipo (pesquisa clínica, pesquisa pré-clínica, serviços laboratoriais, outros); por aplicação (desenvolvimento de drogas, ensaios clínicos, estudos toxicológicos, gerenciamento de dados, outros); por usuário final (empresas farmacêuticas, empresas de biotecnologia, institutos de pesquisa, outros); por fase (fase i, fase ii, fase iii, fase iv, outros).
os principais atores do mercado de cro farmacêutico france são iqvia, labcorp, sineos health, parexel, icon plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat.
o atual tamanho do mercado de cro farmacêutica da frança é de 1,295,8 milhões de dólares em 2025.
o cagr da frança farmacêutica é de 7,82% de 2026 a 2033.
Relatórios publicados recentemente
-
Apr 2026
Mercado de Serviços de Banco de Sangue Cord
serviços de banco de sangue de cordão, tamanho do mercado, compartilhamento & relatório de análise por tipo de serviço (coleção, processamento, armazenamento), por tipo de banco (bancos privados, bancos públicos e bancos híbridos), por componente (sangue de cordão, e tecido de cordão), por usuário final (hospitais, instituições de pesquisa, empresas de biotecnologia, entre outros) e geografia (norte américa, europa, ásia-pacífico, oriente médio e áfrica, sul e américa central), 2021 - 2031
-
Apr 2026
Mercado de Processadores ELISA
elisa processadores tamanho do mercado, share & analysis report by type (optical filter elisa analyzers, and optical grating elisa analysers), por modo (analisadores automatizados de elisa, e analisadores semi-automáticos de elisa), por meio de aplicações (imunologia, desenvolvimento de vacinas, monitoramento de medicamentos, entre outros), por usuários finais (empresas de biotecnologia, empresas farmacêuticas, organização de pesquisa contratual, laboratórios de diagnóstico) e geografia (north américa, europa, asia-pacífico, médio leste e áfrica, sul e américa central), 2021 - 2031
-
Apr 2026
Mercado de Scanner de Slide de Microscópio
microscópio scanner de slides tamanho do mercado, compartilhamento e relatório de análise por tipo (escâner de slides de microscópio portátil, e scanner de slides de microscópio desktop), por aplicação (pesquisa biológica, medicina, veterinária e outros) e geografia (norte américa, europa, ásia-pacífico, médio-oeste e áfrica, sul e américa central), 2021 - 2031
-
Apr 2026
Mercado de Microondas Cookware
micro-ondas tamanho do mercado, participação e relatório de análise por tipo de material (plástico, vidro, cerâmica, silicone e metal), por aplicação (cozinha, reaquecimento e descongelamento), por usuário final (casa, comercial (restaurantes, hotéis e cafés) e indústria de serviços alimentares), por canal de vendas (venda on-line, varejo offline (supermercados, hipermercados, lojas especializadas) e vendas diretas (mercados de empresas) e geografia (norte américa, europa, ásia-pacífico, oriente médio e áfrica, sul e américa central), 2021 - 2031


