トランス医薬品クロ市場規模と予測
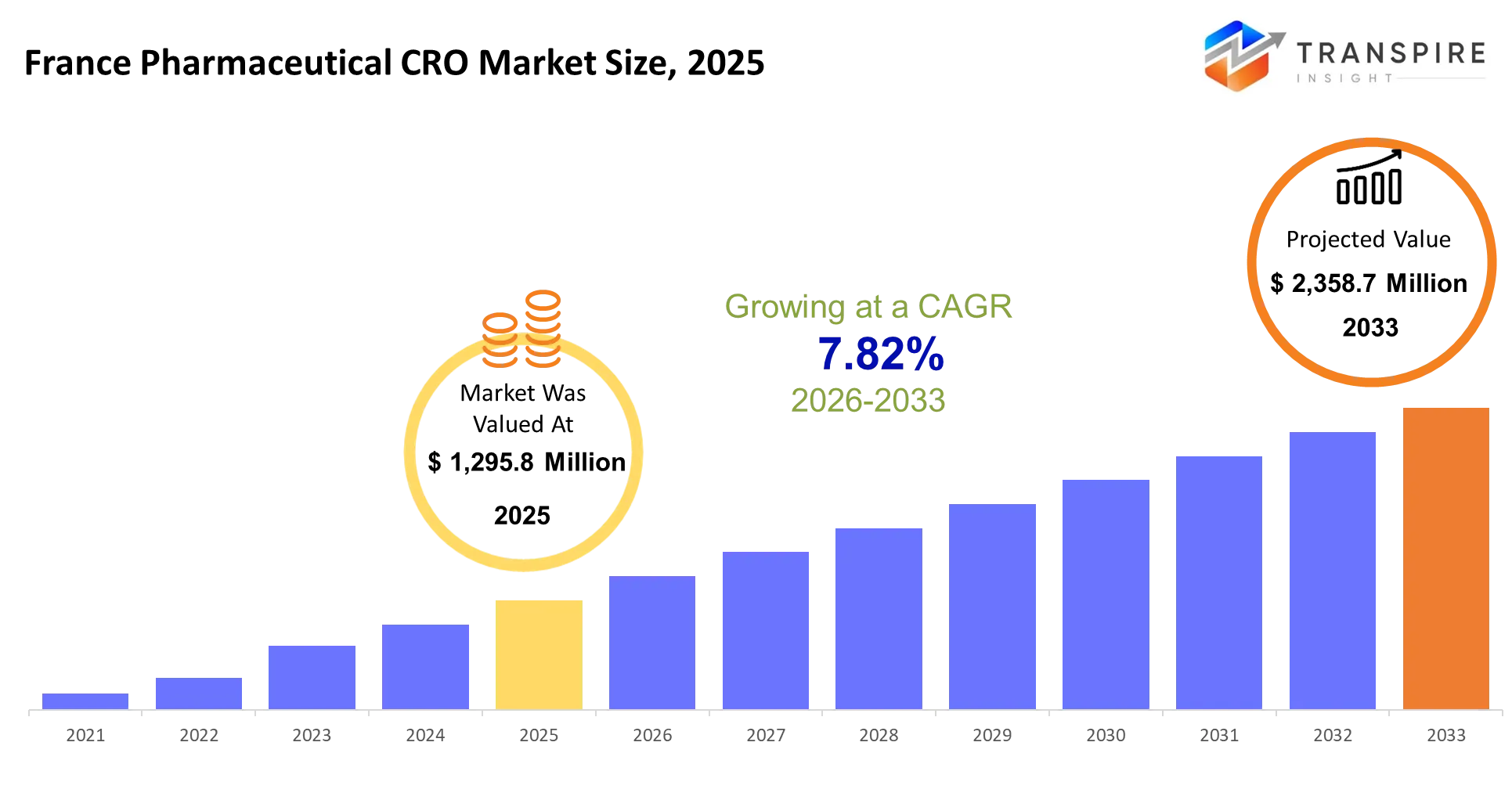
- 芳香の薬剤のcroの市場のサイズ2025:usd 1,295.8,000,000
- 芳香の薬剤のcroの市場のサイズ2033:usd 2,358.7,000,000
- 芳香の薬剤の Cro の市場 cagr: 7.82%
- 偽の薬剤のcroの市場区分:タイプによって(臨床研究、preclinicalの研究、実験室サービス、他);適用によって(drug開発、臨床試験、毒性学の調査、データ管理、他);エンド ユーザー(製薬会社、バイオテクノロジー会社、研究所、他)による;フェーズ(フェーズi、フェーズII、フェーズiii、フェーズIV、他)
このレポートについて詳しく知る 無料サンプルレポートをダウンロード
トランス医薬品クロ市場サマリー
フィンズ製薬クロ市場は、2025年に1,295.8億米ドルで評価されました。 2033年までに2,358.7億米ドルに達する見込みで、7.82%の樽で成長しています。 受託研究機関は、医薬品およびバイオテクノロジー企業に委託されたリサーチサービスを提供し、前臨床研究からフェーズ iv 市場調査まですべてを処理します。 スポンサーは、複数の治療分野および規制管轄区域にわたる社内能力を維持するのではなく、専門ベンダーに複雑な試験管理を転送することを好むので、フランスの市場の65%の臨床研究サービスアカウント。
2020年と2025年の間に3つの規制の変更は、フランス語の作物を操作する方法を再考しました。 第一に、eu 臨床試験規則は、タイムラインの分散性を削減し、文書の要件を上達する、メンバーの州間で調和した承認プロセスを導入しました。 2 番目に、France の国民の健康データ プラットフォームは、スポンサーが臨床試験結果にリンクできる現実世界の証拠データセットにアクセスし、バイオインフォマティクス機能を備えたクロの要求を作成します。 3つ目は、リモート患者モニタリングを可能にする分散型試験プロトコルを受け入れ始めました。これにより、従来の病院ネットワークからホームヘルスプロバイダーや遠隔医療プラットフォームに移行しました。
現在の市場拡大は、バイオテクノロジー企業が内部で処理した段階的な開発作業を外部化することで推進されます。 小規模で中規模のバイオテクノロジー企業は、規制の専門知識が欠如して、emaの投稿とサイトネットワークをナビゲートし、マルチカントリーフェーズiiiの試験を効率的に実行します。 crosは、これらの企業は、恒久的な頭文字ではなく、プロジェクトベースで確立された研究者関係、治療領域の専門知識、および規制業務の専門家へのアクセスを提供します。 このビジネスモデルは、開発のタイムラインを加速しながら、バイオテクノロジーのスポンサーが現金を維持できるようにします。これは、ベンチャーの資金調達サイクルが18〜24ヶ月ごとに実証可能な臨床進捗を必要とします。
重要なfranceの薬剤のcroの市場の洞察
- 臨床研究サービスは、フランス医薬品クロ市場を2024年の65%のシェアに支配し、フェーズIIおよびフェーズiiiの試験管理の外部化を増加させることによって運転しました。
- 2024年の市場の22%のための非法的な研究サービスアカウント, 毒性試験と薬理学的研究を必要とする初期段階の薬物候補をサポートしています.
- 医薬品開発アプリケーションは、医薬品会社が処方開発および安定性試験を委託するため、2024年にCroサービスの需要の41.3%を表しています。
- 臨床試験アプリケーションは、2024年に38.7%の市場シェアを保持し、腫瘍学、免疫学、および患者の採用が困難である希少疾患の治療分野に集中しています。
- 製薬会社は、2024年にエンドユーザーの要求の52.8%を構成し、非コアの臨床開発活動をアウトソーシングし、発見および商品化に関する内部リソースを集中させます。
- バイオテクノロジーは、2024年の市場における31.4%のアカウントを保有し、成長を続けるエンドユーザーセグメントを代表し、2033年までに9.1%のキャッシュで拡大しています。
- フェーズ iii 試験は、2024 年に臨床研究収益の 43.2% を生成します。, 大規模な患者の人口と完全なサービス cros を好む拡張監視期間を必要とします。.
- フェーズIIの試験は、2024年の収益の28.6%に寄与し、特化した統計的およびデータ管理能力を必要とする適応試験設計の需要が増えています。
- iqviaは、2025年にフランス語のCro市場の約15-18%を保持し、複数の治療領域にわたって統合されたデータ分析と臨床試験サービスを利用しています。
- ラボコープは、2024年に20%でフランスの臨床開発業務を拡大し、研究者サイトや治療分野の専門家を追加し、バイオテクノロジーの需要を増加させます。
重要なドライバ、拘束、およびフランス医薬品クロ市場での機会は何ですか?
第一次成長ドライバーは、選択的なアウトソーシングから、個々の研究ではなく、開発プログラム全体を管理する戦略的パートナーシップにシフトする製薬会社です。 大規模な製薬会社は、段階iiiによる前方性を覆う多年契約を、特定の治療分野のために達成しました。これにより、Crosは収益可視性を提供し、希少疾患患者の規制や腫瘍学バイオマーカープラットフォームなどの専門能力に投資することができます。 iqvia、Syneos Health、およびparexelは、これらの戦略的パートナーシップの周りのフランス語の操作をすべて構成し、トランザクションサービスプロバイダとして動作するのではなく、特定のスポンサーアカウントにチームを宣言しています。 財務への影響は実質的です。戦略的パートナーシップ契約は通常、18~36か月の単一学契約と比較して、数百万ユーロの投資ポートフォリオを3〜5年連続で実施しています。
最も重要な拘束は、需要の高い治療分野における調査者サイトの容量制限です。 フランスの腫瘍学センターと免疫学の専門家は、試験プロトコルで上書きされ、患者の採用ボトルネックが作成され、試験実行の他の側面を効率的に管理する方法に関係なく、学習時間を延期します。 crosは、資格のある研究者がトレーニングと規制認定の年を必要とするため、この問題を解決するために、単に新しいサイトを開くことができません。 フェンスは、特に希少疾患の試験で急性であり、フランスは関連する患者集団と5〜10のセンターしか持っていない可能性があり、それらのセンターはすでに複数の競合プロトコルにコミットしています。 この力は、採用のタイムラインを拡張したり、経験の浅い研究者のサイトに拡張したり、コストとリスクを増加させ、品質を研究します。
最も明確な機会は、臨床試験データを接続する現実的な証拠サービスで、フランス国民の健康データベースにあります。 ansmは現在、特定の指標の規制の提出をサポートするために、実際の証拠を受け入れています。そして、スポンサーは、電子健康記録から観察データと伝統的なランダム化された制御試験方法を組み合わせたハイブリッド研究を設計できるクロを必要とします。 これは、ほとんどの cros が現在所有していない機能を必要とします。: ヘルスケア分析、規制の専門家を理解しているデータ サイエンティスト、現実世界の証拠の提出を構造する方法を知っているし、フランスの保健機関との関係を確立します。 これらの機能を構築する作物は、これらのハイブリッド研究設計を実行するために、技術的なインフラと規制の専門知識が欠けている競合他社によって簡単にレプリカできないハイマージン作業をキャプチャします。
偽の医薬品クロ市場における人工知能の影響は?
ai-powered患者識別システムでは、電子健康記録をスクリーニングし、特定の試験インクルージョン基準を満たしている候補を見つけるようになり、サイトが手動でチャートを見直し、対象となる患者を特定することで、採用のタイムラインを加速します。 iqviaとLabcorpは、診断コード、ラボ値、薬の履歴、およびその他の臨床マーカーに基づいて患者をフラグするフランスの医療システムに機械学習モデルを展開しています。 これらのシステムは、統合された電子健康記録とサイトから数週間から数日間に及ぶスクリーニング時間を短縮しましたが、採用は、より大きな病院ネットワークに限らず、デジタル患者データで。 運用上のメリットは、対象となる患者の十分な数を識別するために、以前に必要な期間のマニュアルチャートレビューが必要なまれな疾患試験で最も見られます。
自然言語処理は、サイトコーディネーターによるマニュアルデータエントリーを必要としない臨床ノート、ラボレポート、および患者の日記から有害事象を抽出することにより、安全監視を自動化します。 Syneos Health と icon は、安全信号の試験文書を継続的にスキャンし、規制当局への即時報告を必要とする潜在的な深刻な有害事象のフラグを立てる nlp システムを導入しました。 この自動化は、48-72時間から技術を使用して24時間以内にメディアの有害事象報告時間を削減しました。規制要件が24時間以内に深刻な有害事象を報告するときに重要です。 制限は、nlpの精度が文書の品質に依存し、フランス語の臨床ノートには、自動抽出信頼性を削減する医学的短手および非標準化された用語が含まれます。
より広い ai の採用への第一次障壁はフランスのヘルスケア プロバイダーを渡るデータ フラグメンテーションです。 患者記録は、個々の病院システム、地域保健ネットワーク、および民間慣行内でサイロ化され、実際の患者集団を反映した包括的なデータセットで、アイモデルの訓練を防ぐことができます。 さらに、フランスのデータ保護規則は、研究コンテキストにおける健康データの二次使用のための明示的な忍耐強い同意を必要とします。これは、多くのCrossがAI開発プロジェクトに禁止されていることを遵守のオーバーヘッドを追加します。 これは、最も価値のある ai アプリケーションが大規模な要求するパラドックスを作成します。, フランスの規制枠組みが合法的に組み立てることが困難である多様なデータセット.
主要市場の傾向
- 医薬品のスポンサーは、取引サービスの購入から2022年と2024年の間の多年戦略的パートナーシップに移行し、5または6つのベンダーから2または3つの優先プロバイダーへのクロリレーションを統合しました。
- 分散型試験の採用は、2023年にansmの公開された指導が遠隔忍耐強い監視および場所ベースの評価に有効な代わりとして家の健康の訪問を受け入れると加速しました。
- バイオテクノロジー企業は、2021年に開発費の平均60%から2024年までに、ベンチャーキャピタルの圧力で駆動し、固定コストを削減しました。
- iqviaとSyneos Healthは、2023年から2025年の間に25-30%のフランスの治療領域の専門家を拡張し、腫瘍学および希少疾患の専門家を雇用し、戦略的パートナーシップ契約をサポートしました。
- 実際の証拠サービスは、2024年に異なる提供として登場しました。Crosは、試験データと観察健康記録を組み合わせたハイブリッド研究を設計するために専任のチームを確立しています。
- 腫瘍学試験のための患者の採用のタイムラインは、研究者サイト容量の制約と有能なプロトコルによる12ヶ月から16-18ヶ月に増加しました。
- 中国の作物は2024年にフランスの市場に参入し、フェーズiと初期フェーズIIは20〜25%で欧州の操作を確立するために、有罪な価格設定の下でサービスを提供します。
- データ管理サービスは、2023と2025の間の臨床監視よりも速く成長し、高度な分析と試験中にリアルタイムのデータ視覚化のための高められたスポンサーの要求を反映しています。
トランス医薬品クロ市場セグメンテーション
タイプ別
臨床研究サービスは、総収入の65%でフランスのクロ市場を支配します。 このセグメントは、患者の採用、サイト監視、データ収集、およびフェーズIV臨床試験によるフェーズiの規制提出サポートをカバーしています。 ドミナンスは、医薬品およびバイオテクノロジーが試験管理を外部化し、内部の臨床手術チームを維持するのではなく、クロスに外部化する構造的シフトを反映しています。 iqvia、Labcorp、およびSyneos Healthのようなフルサービスのcrosは、スポンサーの臨床開発アームとして機能し、複数の同時試験を横断して、研究者の関係、規制相互作用、およびデータ品質を管理します。 値の提案はリスク転送です。スポンサーは、登録した患者とスケジュール上のデータのクリーン化を促し、クロクロは運用の複雑さとタイムラインの分散性を吸収します。
市場22%の非臨床研究サービスアカウント、毒性学研究、薬理分析、およびヒト実験前に起こる製剤開発を網羅しています。 このセグメントは、初期段階のバイオテクノロジー企業と医薬品の発見チームで、専用の施設を建設することなく、専門ラボ機能を必要とする。 シャルル川、コヴァンス、およびユーロフィンは、規制毒性学研究のために装備されているグラップ認証研究所の所有権を通じて、フランスの非公式サービスを支配します。 セグメントは、前臨床研究は、検証された分析方法と経験を必要とするデータ品質と再現性のための厳格な規制基準を満たす必要があるため、技術的に要求されます 実験室 科学者。 マージンは、開発プログラムの特定のラボを認定した後、コストを交換するので、臨床研究よりも高くなります。
ラボサービス、その他専門メーカーは、市場の13%を表しています。 臨床検査、臨床検査、医療機器検査やデジタルヘルス検証などのニッチ機能など、バイオ分析試験、セントラルラボサービスが含まれます。 2023年~2025年の間には、臨床試験管理を専門とするラボ分析と組み合わせる統合サービスが増加しているため、セグメントはコア臨床研究よりも速く成長しました。 例えば、腫瘍学の試験は、多くの場合、コンパニオン診断開発を伴います 医薬品 生体マーカーの検証、臨床サンプル収集、および診断アッセイ開発を統一したプログラムとして調整できるCrosを必要とするテスト。 これらの統合サービスを提供する作物は、臨床試験管理のみを提供するよりも、より高いプロジェクトごとの収益をキャプチャします。
このレポートについて詳しく知る 無料サンプルレポートをダウンロード
用途別
医薬品開発アプリケーションは、市場需要の41.3%、製剤開発、安定性試験、分析方法開発、製造サポートサービスでリードしています。 製薬会社は、内部開発機能が特定の処方課題の能力や専門的専門知識が不足したときに、これらの活動をクロにアウトソースします。 たとえば、バイオロジックの安定的な処方を開発するには、ほとんどのスポンサーが社内で維持しない専門機器や専門知識が必要です。 カタレント、パッション、ロンザなどの作物は、契約ベースでこれらの機能を提供します。これにより、スポンサーは、フォーミュレーションラボへの資本投資なしで開発を進めることができます。 処方開発作業は技術的に複雑であるため、アプリケーションはマージン認定され、プレミアム請求率をコマンド経験豊富な科学者が必要です。
臨床試験のアプリケーションアカウント38.7%の需要, 特に患者の登録に焦点を当て, サイト管理, より広範な開発サポート. このセグメントは、規制戦略、データ分析、およびポストトライアル活動を除く、治験実行コンポーネントのみをキャプチャする臨床研究サービスとは異なります。 本アプリケーションは、2022年から2024年にかけて、バイオテクノロジー企業は、患者の採用や現場のモニタリングを処理し、他の開発活動を社内で維持できる作物を調達しました。 このunbundlingは、エンドポイントの選択や試験設計などの戦略的決定を上回る一方で、臨床開発の最も操作上の複雑でタイムラインに敏感な側面を外部化するためにスポンサーを許可しました。
毒性学研究、データ管理、その他のアプリケーションは、市場全体の20%を表しています。 毒性学研究は、規制当局の提出のために必須であり、ほとんどのスポンサーが内部で動作しないグルップ認証施設が必要です。 データ管理サービスは、特殊なデータベースプラットフォームや統計分析機能を必要とする、ウェアラブル、リモート・モニタリング・デバイス、および患者報告された結果から、電子データの量の増加を実証する試験として急速に成長しました。 2020年と2025年の間にクラウドベースのデータプラットフォームとリアルタイム分析に投資したCrossは、従来のロックされたデータベースではなく、継続的なデータ解析を必要とする、透明なトライアルモニタリングと適応試験設計のための成長しているスポンサーの需要を収集しました。
エンドユーザーによる
製薬会社は、フランスにおけるクロ需要の52.8%を構成する。 大規模な製薬会社は、内部容量が制約または治療領域の専門知識が不足している特定の開発プログラムを委託しています。 たとえば、強力な腫瘍学能力を持つ企業は、患者の組織や研究者ネットワークをそれらの指標に確立された患者の組織と作物にまれな病気の開発を外部化することがあります。 アウトソーシングの決定は経済的に推進されます:会社が1つまたは2つの試験を1年だけ実行する治療分野のための社内の臨床操作を維持することは、プロジェクトベースで作物をすることと比較して費用対効果が高いです。 これは、スポンサーの利益が持続するが、個々の企業ポートフォリオが限られている治療分野におけるCrosの安定的な要求を作成します。
バイオテクノロジーは、市場の31.4%を占め、2033年までに9.1%の樽で最速成長セグメントを表しています。 これらの企業は、通常、内部臨床開発能力が欠如し、フェーズ iii の試験を通じて、開発作業の大部分を外部化します。 成長ドライバーは、ベンチャーキャピタルの資金調達ダイナミクスです。バイオテクノロジー企業は、キャッシュバーンを最小限に抑えながら、臨床進捗を迅速に実証することが期待されています。これにより、固定されたヘッドカウントを必要とする内部機能を構築するよりも、より財務的に魅力的になります。 crosは、プログラムのニーズをスケールアップする柔軟な能力を備えたバイオテクノロジースポンサーを提供しています。継続的なリテーナーの支払いやサラリードスタッフを必要としているのではなく、アクティブなプロジェクトのみを請求します。
研究機関および他のエンドユーザーは、15.8%の需要に貢献します。 学術医療センターおよび政府研究機関は、規制レベルのデータ収集と監視を必要とする研究者主導の試験と公衆衛生学の研究のための作物に従事しています。 これらの顧客は、通常、固定予算と定義されたタイムラインで助成金基金で動作します。これは、Crosが厳格なコスト制約内でサービスを提供するために必要なものです。 セグメントは、市販の医薬品よりも低マージンを提供していますが、新しい治療アプローチとまれな病気の患者集団へのアクセスを伴って、その後、学術的発見が規制当局の承認と商品化に進むときに商業開発機会に変換します。
段階によって
フェーズiiiの試験は、大規模な患者集団、拡張監視期間、および複雑な規制要件による臨床研究収益の43.2%を生成します。 フランスの典型的なフェーズ iii 腫瘍学試験は、研究期間中にサイト監視、データ管理、安全報告、および規制調整を必要とする3〜4年以上にわたって 25-40 の研究者サイト全体に 300-500 人の患者を登録する可能性があります。 crosは、この運用の複雑性を管理し、スポンサーがトライアル設計と規制の提出に関する戦略的決定に集中できるようにすることで価値を提供します。 フェーズiiiの収益濃度は、大規模な試行実行の直接コストと、リスクプレミアムスポンサーは、製品の発売日を決定する積極的な登録タイムラインを配信するために、Crosの支払いを反映する。
フェーズIIの試験は、より小さい患者集団における線量調査と初期の有効性評価に焦点を当て、収益の28.6%に貢献します。 これらの試験は、暫定結果に基づいて、入学基準やスケジュールを変更する適応設計をますます使用しています。これは、強力な統計的およびデータ管理能力を有する作物を必要とします。 適応試験の技術的複雑性は、専門的専門知識が欠如する小作のエントリへの障壁を作成します。, 大規模なフルサービスプロバイダは、プレミアム価格設定をコマンドすることができます. フェーズIIの作業は、通常、フェーズIIを正常に完了するスポンサーがフェーズiiiに同じcroを続行しているため、Crosにとって戦略的に重要です。
フェーズi、フェーズIV、およびその他の試験フェーズは、収益の28.2%のアカウントをまとめました。 フェーズiの試験は比較的小さくても技術的に要求され、第一人者の安全調査および集中的な忍耐強い監視のための専門設備を要求します。 フェーズ iv のポストマーケティングの調査は、規制当局が前承認された臨床データを補うために現実世界の証拠を必要としているにつれて成長しています。 従来のフェーズ iv の試験管理と観察健康記録と試験データを組み合わせた現実的な証拠機能を提供する作物は、変圧器の払い戻し交渉と臨床ガイドライン開発のための証拠を生成しながら、規制要件を満たす統合後のマーケティング監視プログラムのための成長スポンサーの需要をキャプチャしています。
偽の医薬品クロ市場を運転する重要なユースケースは何ですか?
プライマリアプリケーションは、内部の臨床動作能力を欠くバイオテクノロジー企業のためのフルサービスフェーズiii試験管理です。 これらのスポンサーは、データベースロック、規制送信、およびポスト承認安全監視を通じて、サイト選択からトライアル実行のすべての側面を処理するために、Crosを従事しています。 典型的な関与は、バイオテクノロジーのスポンサーがフェーズIIの証拠受容試験を完了し、女性承認に必要なピボタルフェーズiiiプログラムを実行するために作物を必要とするまれな病気の徴候を伴うかもしれません。 クロは、研究者のサイトネットワーク、規制の専門知識、患者の採用戦略、およびターンキーベースのデータ管理インフラストラクチャを提供し、バイオテクノロジー企業は、永久的な臨床操作のヘッドカウントを構築することなく、商業化を進めることができます。
隣接する需要は、治療領域固有の開発プログラムをアウトソーシングする大規模な製薬会社から来ています。 例えば、限られた免疫学の専門知識を持つ会社は、取得された免疫学の資産のためのすべての臨床開発を管理するために、クロの確立された関係とフランスのリウマトロジーと皮膚病の調査者を活用するcroを従事するかもしれません。 これらの戦略的パートナーシップは、通常、数年にわたって複数の試用期間に及ぶもので、Croは予測可能な収益を提供し、スポンサーは、永続的なスタッフの拡張なしで治療領域の専門知識へのアクセスを提供します。 市販のロジックは、特定の治療領域に焦点を当てたcros は、一般的な内部開発チームが再現できない深い調査関係とプロトコル設計経験を開発しています。
従来のランダム化された制御試験と、フランスの健康データベースから現実世界の証拠を組み合わせたハイブリッド試験設計の新興ユースケースセンター。 スポンサーは、コントロールアームが別のプラセボコホートを登録するのではなく、電子健康記録から一致した患者を使用する研究を設計するためにクロを従事しています。これにより、試験コストを削減し、登録タイムラインを加速します。 iqvia と Syneos Health は、データサイエンティスト、疫学者、および臨床試験方法論と現実世界の証拠基準の両方を理解した規制の専門家を必要とする、これらのハイブリッド研究を実行するために専任のチームを確立しました。 アプリケーションは技術的に要求されますが、従来の十分に登録された試験と比較して、フェーズiiiコストを30〜40%削減するいくつかのハイブリッド設計で、スポンサーの実質的なコスト削減を提供しています。
レポートメトリック | インフォメーション |
2025年の市場規模の価値 | 1,295.8百万円 |
2026年の市場規模の価値 | 1,392.6百万円 |
2033年の収益予測 | USD 2,358.7百万円 |
成長率 | 2026年から2033年にかけて7.82%の樽 |
基礎年 | 2025年 |
過去のデータ | 2021年 – 2024年 |
予測期間 | 2026 - 2033年 |
レポートカバレッジ | 収益予測、競争力のある風景、成長因子、トレンド |
地域規模 | エントランス |
主要な会社のプロフィール | iqvia、Labcorp、Syneosの健康、parexel、アイコンplc、charles川、medpace、pra健康科学、covance、Eurofins、wuxi apptec、sgs、ppd、clinipace、veristat |
カスタマイズスコープ | 自由なレポートのカスタム化(地域及び区分の規模)。 あなたの厳密な調査の必要性を満たすavalyカスタマイズされた購入の選択。 |
レポートセグメンテーション | 種類別(臨床研究、前臨床研究、研究室サービス、その他); 応用(ドラッグ開発、臨床試験、毒性学研究、データ管理、その他); エンドユーザー(製薬会社、バイオテクノロジー会社、研究所、その他); フェーズ(フェーズi、フェーズII、フェーズiii、フェーズIV、その他) |
トランス医薬品クロ市場における成長は?
フランセは、他の欧州市場が同等の規模で再現できない3つの構造上の優位性を提供しています。 第一に、国は、65万人を超える市民をカバーする包括的な電子健康記録を備えた一元化された医療システムを運営し、患者識別能力と現実世界のエビデンスへのアクセスを提供し、そのフラグメント医療システムは一致できない。 第二に、フランスはパリ、ライヨン、およびマセリーユの専門的研究者サイトの密な集中を維持し、学術医療センター、教育病院、および地理的な近接内の研究機関クラスターが、試験物流を簡素化し、地理的に分散したサイトネットワークと比較して監視コストを削減します。 3 番目, アンスムは、予測可能な規制レビューの適性を確立し、分散プロトコルや現実的な証拠などの新興試験方法に関する明確なガイダンス, これは、スポンサーが複数の年の開発プログラムを計画するための不確実性を減らす.
フランスの競争力のあるダイナミックは、言語と規制要件は、非ユークロのエントリに自然な障壁を作成するため、他のヨーロッパの市場とは異なります。 試験プロトコル、通知された同意文書、および規制当局の提出はフランス語でなければならず、集中的なヨーロッパのチームではなく、専用のローカルスタッフが必要です。 さらに、フランスのデータ保護規則は、一般的なgdpr規定と異なる健康データ処理に関する特定の要件を課し、Crossを必要とすると、フランス固有のコンプライアンスプログラムを維持します。 これらの障壁は、iqvia、Labcorp、Syneos Healthなどの確立されたプレーヤーを保護し、数十年にわたりフランスで運営し、地元のインフラに投資し、フランスの操作を確立しようとする新しい競合他社のより高いエントリコストを作成します。
急成長の需要のセグメントは、フランス国民の健康データベースが超希少な適応症の迅速な患者識別を可能にするまれな疾患試験です。 少数の1,000人のフランスの患者に影響を与える条件では、研究者が適格な候補を識別するために医学の記録を手動で選別しなければならないので、従来のサイトベースの採用は年を取ることができます。 フランスの保健機関とのデータアクセス協定を確立した作物は、電子的に全国の患者の人口をスクリーニングすることができます, 数ヶ月ではなく数週間の対象となる患者を識別. この機能は、欧州のまれな病気の試験のための好まれな場所を偽りなくしました, スポンサーは、高度に超希少疾患の適応症における多国籍研究のためのフランスのサイトを選択すると、患者識別速度は、全体的なプログラムのタイムラインを決定します.
偽の医薬品クロ市場での重要な選手であり、どのように競争しますか?
フランスのクロウ市場は2層構造として作動します。 iqvia、Labcorp、Syneos Health、parexel、およびアイコンは、約55-60%の市場シェアを保持し、前方からフェーズIVを介して統合された機能を提供するフルサービスプロバイダとして競争します。 これらの企業は、治療領域の専門知識、調査サイトネットワーク、およびリアルタイムの試験可視性をスポンサーに提供する技術プラットフォームに競争しています。 中層およびより小さい cros は治療の焦点、サービス タイプ、または地域の存在に基づいて専門にされたニッチを占めます、通常、フルサービスの契約のために直接競争するのではなく、複雑なプログラムでより大きい cros と提携します。
iqviaは、その統合されたデータと臨床サービスプラットフォームを通じて、試験管理と実際の証拠機能を組み合わせた競争しています。 同社は、処方データ、病院の排出記録、および患者識別、サイト選択、および実現可能性評価のために使用するクレーム情報をカバーする、フランス最大の商業健康データベースを運営しています。 iqviaは、2023年から2025年の間にフランス臨床手術を25%拡大し、腫瘍学、希少疾患、免疫学に治療領域の専門家を追加し、大規模な製薬スポンサーとの戦略的パートナーシップ契約をサポートしました。 同社は、分析能力に差別化し、予測的な登録モデルと、より小さいCrosが等しいデータ資産なしで複製できない比較効果分析をスポンサーに提供しています。
ラボコープは、ラボサービスおよび臨床試験管理の垂直統合を通じて競争します, 同社は、セントラルラボのテストと試行実行を組み合わせたスポンサーユニファイドプログラムを提供できるようにします, バイオマーカー分析, そして、コンパニオン診断開発. この統合は、生体マーカー主導の患者選択と薬理学的評価が臨床サイトと専門研究所間の調整を必要とする、腫瘍学的およびまれな疾患試験で重要である。 ラボコープは、臨床試験のスポンサーと定期的な診断市場の両方を提供し、純粋なプレイのクロが一致できないスケールの経済性を作成する、フランスでグラップ認定研究所を運営しています。 同社は、統合ラボおよび臨床サービスが協調オーバーヘッドを削減し、開発のタイムラインを加速し、試験管理およびラボテストのための別のベンダーを関与させることと比較して、バイオテクノロジーのスポンサーを開発しています。
最近の開発
iqviaは2026年マーチで、フランス語の希少疾患患者レジストリと戦略的パートナーシップを結び、超希少神経疾患の遺伝子検査と自然史データを提供することを発表しました。 コラボレーションは、500人のフランスの患者に影響する条件のための治療を開発するスポンサーのための患者識別と試験の両立性評価を加速することを目指しています。 https://www.iqvia.com (iqvia)
2026年にラボコープは、セルと遺伝子治療の試験のための新しいバイオマーカーのテスト機能で、フランスの中央研究所の操作を拡大しました。 施設は、フランスの臨床研究を実施する高度な治療スポンサーのための薬学サンプルとコンパニオン診断アッセイを処理します。 https://www.labcorp.com (labcorp)
どのような戦略的洞察は、フランス医薬品クロ市場の未来を定義しますか?
次の5〜7年間で、フランスのクロ市場における競争上の優位性は、運用の実行能力から、新しい試用方法を可能にするデータおよび技術プラットフォームにシフトします。 現在の市場は、患者を素早く登録し、スケジュールにクリーンなデータを配信できるクロを報酬としていますが、これらの機能は、電子データキャプチャや遠隔監視ツールとして商品化され、業界全体で標準化されています。 次の競争のフロンティアは、現実世界証拠の統合、分散型試験の実行、およびaiパワード患者の識別です。これらすべてが、実質的な技術投資とデータアクセス契約を必要とし、競合他社の不足の規模への参入障壁を作成します。
市場予測が下落するリスクは、新規の試用方法論の規制承諾期限です。 ansm は、分散型試験と現実世界の証拠に関するガイダンスを発表しましたが、これらのアプローチを使用して提出された実際の規制レビューは限られています。 規制当局は、ガイダンス文書が提案するよりも、より保守的な慣行を証明する場合、スポンサーはこれらの手法の採用を遅らせるかもしれません。これにより、これらの分野におけるクロ機能の需要を削減し、規制の優先順位が確立される伝統的なサイトベースの試験実行を支持します。 これは、分散型トライアルプラットフォームに投資した新しいエントラントを分散しながら、強力なサイトネットワークで強力なクロクロスに利益をもたらします。
値下げされたままの機会は、フランスの健康データベースを使用して、フェーズ iv の試験管理と観察研究を組み合わせたポスト approval 実世界の証拠サービスです。 ペイアーは、再投資の決定をサポートするために現実世界の有効性データを必要とし、スポンサーは、規制後の市場要件とペイアの証拠の両方のニーズを満たす統合プログラムを設計できるクロを必要とします。 セグメントは現在小型ですが、従来のフェーズ iv 作業よりも高いマージンを提供しています。なぜなら、健康経済、疫学、およびほとんどの cro が維持しないデータベース分析の専門的能力を必要とするからです。 これらの機能を構築する企業は、規制義務を満たすだけでなく、複数の利害関係者にサービスを提供するエビデンスの世代別プログラムに対する成長しているスポンサー要求をキャプチャします。
よくある質問
よくある質問への素早い回答をご覧ください。
フィンズ製薬クロ市場は、2033年までに2,358.7億米ドルに達すると予想されます.
偽の薬剤のクロ市場のための主要な区分はタイプによってあります(臨床研究、preclinical研究、実験室サービス、他);適用によって(drug開発、臨床試験、毒性学の調査、データ管理、他);エンド ユーザーによって(製薬会社、バイオテクノロジー会社、研究所、他);フェーズ(フェーズi、フェーズii、フェーズiii、段階iv、他).
主要なフランス医薬品クロ市場プレーヤーは、iqvia、labcorp、syneos健康、parexel、アイコンplc、charles川、medpace、pra健康科学、共鳴、eurofins、wuxi apptec、sgs、ppd、clinipace、veristatです.
現行のフランス医薬品クロ市場規模は、2025年に1,295.8万米ドルです.
芳香の薬剤の cro の市場は 2026 から 2033 まで 7.82% です.
最近発行されたレポート
-
Apr 2026
コードブラッドバンキングサービス市場
コード血液銀行サービス市場規模、サービスの種類(回収、処理、保管)によるシェア&分析レポート、銀行タイプ(民間銀行、公共銀行、およびハイブリッド銀行)、コンポーネント(コード血液、コード組織)、エンドユーザー(病院、研究機関、バイオテクノロジー企業など)、および地理(北アフリカ、ヨーロッパ、アジア太平洋、中東、アフリカ、南、中央2031)、2021 - 2021 - 2021 - 2021 - 2021
-
Apr 2026
ELISAプロセッサー市場
エリサプロセッサは、タイプ(光学フィルターエリサアナライザアナライザアナライザアナライザ)による市場規模、シェア&分析レポート、モード(自動化エリサアナライザアナライザアナライザ)、アプリケーション(免疫学、ワクチン開発、医薬品監視、その他)、エンドユーザー(バイオテクノロジー企業、製薬会社、受託研究機関、および診断ラボ)、および地理情報(北東アジア、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、
-
Apr 2026
顕微鏡のスライドの走査器市場
顕微鏡のスライドの走査器はタイプ(携帯用顕微鏡のスライドの走査器およびデスクトップの顕微鏡のスライドの走査器)、適用(生物的研究、薬、獣医および他の)および地理学(北のアメリカ、ヨーロッパ、アジアpacific、中間の東およびアフリカ、南および中央アメリカ)、2021 - 2031年
-
Apr 2026
マイクロウェーブ調理器市場
マイクロウェーブ調理器市場規模、材料タイプ(プラスチック、ガラス、セラミック、シリコン、金属)によるシェア&分析レポート、アプリケーション(調理、再加熱、および解凍)、エンドユーザー(家庭用、商業(レストラン、ホテル、カフェ)、およびフードサービス業界)、販売チャネル(オンライン小売、オフライン小売(スーパーマーケット、スーパーマーケット、専門店)、および直接販売(会社アウトレット)および地理(中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/東/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/南/東/東/南/南/東/東/南/南/南/南/南/南/東/東/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/


