ヨーロッパのヘルスケアの契約の研究の組織の市場規模及び予測:
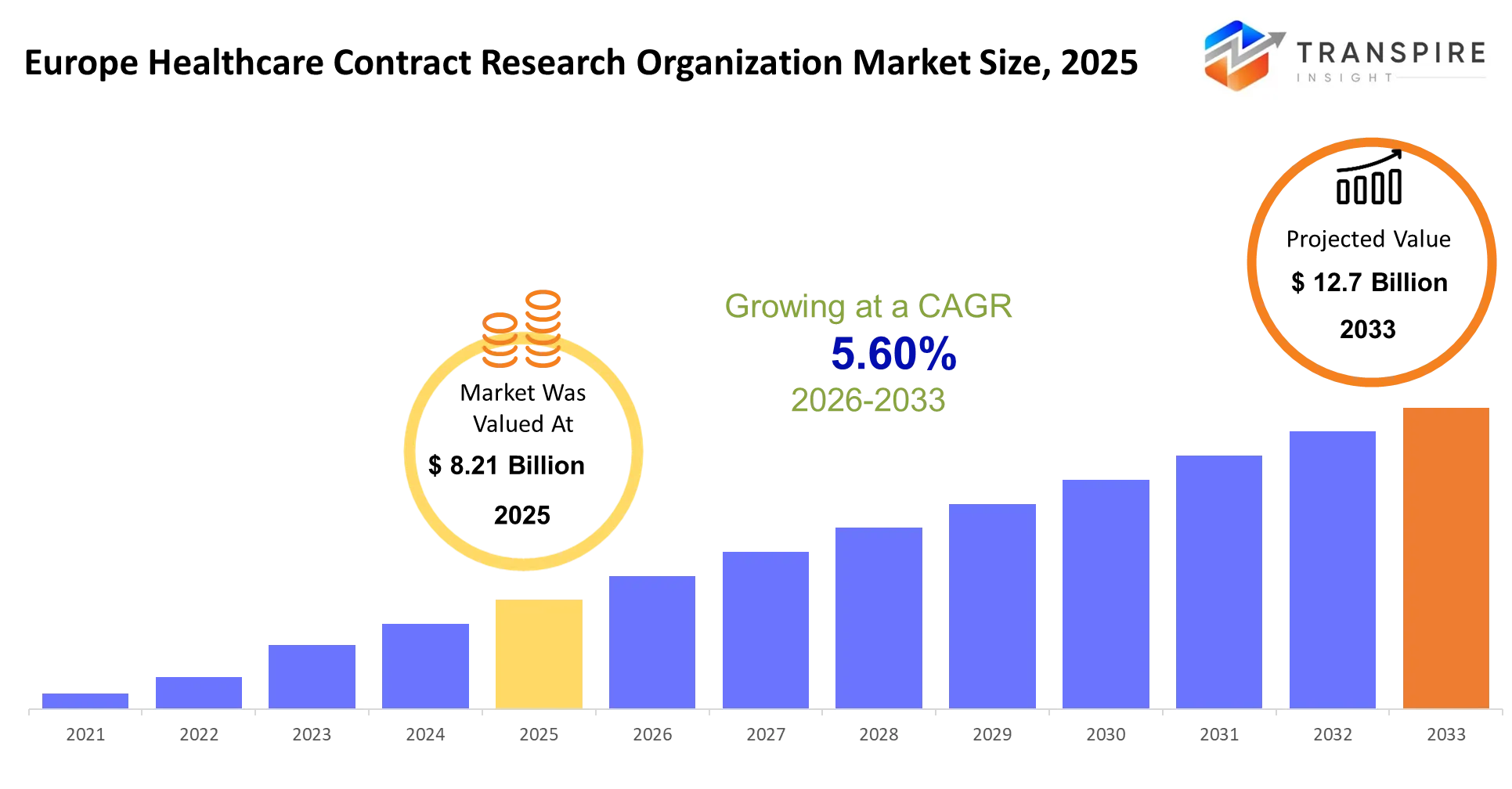
- 欧州のヘルスケアの契約の調査の組織の市場規模 2025: 米ドル 8.21 億
- 欧州のヘルスケアの契約の調査の組織の市場規模2033:usd 12.7億
- ヨーロッパのヘルスケアの契約の研究の組織の市場樽: 5.60%
- ユーロピーヘルスケア契約研究組織の市場セグメント:タイプ(臨床研究サービス、preclinicalサービス、ラボサービス、その他)、アプリケーション(医薬品開発、臨床試験、医療機器試験、規制サービス、その他)、エンドユーザー(製薬会社、バイオテクノロジー会社、医療機器会社、研究所、その他)、フェーズ(フェーズI、フェーズII、フェーズiii、フェーズiii、フェーズIV、その他)
このレポートについて詳しく知る 無料サンプルレポートをダウンロード
ヨーロッパのヘルスケアの契約の調査の組織の市場の概要:
欧州医療契約研究機関の市場規模は、2025年に8.21億米ドルで推定され、2033年までに12.7億米ドルに達すると予想され、2026年から2033年までの5.60%の樽で成長しています。 欧州の医療契約研究機関は、医薬品およびバイオテクノロジークライアントの臨床試験実行のすべての側面を処理する委託された医薬品開発研究所として機能します。 組織は、ラボテストから市場リリースまでの治療開発を、必要な運用リソースと専門的専門知識を提供することで実施することができます。
デジタル監視ツールとリモート患者のエンゲージメント方法を使用する分散型およびハイブリッド試験モデルは、過去3〜5年間の主な研究アプローチとなっています。 特定の研究施設を使用する必要性を減らすので、研究チームはより多くの患者と働くことを可能にします。 covid-19の流行は、動きの制限にもかかわらず、引き続き試行が必要で、規制機関による仮想方法の迅速な受諾につながるため、主要な触媒として機能しました。
高速かつフレキシブルなソリューションの需要増加は、今、より高い速度でアウトソーシングサービスを使用するスポンサーの背後にあるメインドライバーとして登場しました。 データ分析と現実世界の証拠と適応試験機能の組み合わせにより、Cros が機能し、運用の複雑さからスケーラブルな収益ストリームを作成できるようになりました。
主要な市場の洞察
- 西欧諸国は、欧州の医療契約研究機関の市場を制御します。なぜなら、彼らはドイツ、統一された王国、およびフランスが2024年にリードしている65%以上の市場シェアを保持しているためです。
- 東欧は、2030年までに最も急速に拡大するエリアとして、費用対効果の高い試験を実施し、参加者を迅速に採用し、欧州連合規制要件に適合するための進捗状況を把握しています。
- 臨床試験サービス部門は、欧州諸国がIIおよびiii研究を委託することを選ぶので、70%のシェアで市場をリードします。
- 業界における第2位の市場シェアは、バイオテクノロジー企業から新しい製品を開発し、研究開発活動を拡大するサポートを受けている、非法的なサービスに属しています。
- 2025年から2030年までにデジタルトライアルの実装が拡張するので、データ管理と現実世界の証拠サービスのセグメントは急速に成長しています。
- 腫瘍学分野は、医療研究者が複雑な試験研究を実施し、がん研究者が多数のがん薬を発症するので、2024年に30%に達した最大のアプリケーション市場シェアを保持しています。
- 希少疾患に対する規制支援とともに、パーソナライズド医薬品の開発は、標的療法を開発する最も急速に発展する医療分野を作成します。
- 製薬会社は、その医薬品開発プロセスを明示しながら、クロスと提携して運用コストを削減するため、市場の約60%を制御します。
- 小規模で中規模のバイオテクノロジー企業は、成長ニーズをサポートする完全なサービスアウトソーシングソリューションに依存する、最も急速に発展するユーザーセグメントを表しています。
欧州医療契約研究機関市場における主要なドライバー、拘束、機会は何ですか?
欧州医療契約研究機関の市場における成長を促進する主な要素は、現在承認された医薬品あたり2億米ドルを超える研究開発費の上昇から上昇する複雑な臨床開発作業のアウトソーシングから結果を得ます。 製薬会社は、さまざまな欧州諸国に存在する複雑な規制要件に対処する一方で、製品開発のタイムフレームを削減する必要があります。 組織は、初期段階の臨床試験には、最も困難な実行作業と患者の登録困難が含まれているため、より高いアウトソーシング率を実践しています。 外部の試用費用でより多くのお金を費やすスポンサーは、より多くの価値のある契約を作成して、Crossと拡張されたサービス関係につながる。
欧州規制制度は、研究活動を制御するema規制の存在にもかかわらず、異なる国の規制間で分かれています。 各国は、倫理の承認を得て、患者データを管理し、研究施設のコンプライアンスを強化するための独自のシステムを展開しています。 臨床研究機関(cros)の既存の運用モデルは、より長い試験準備時間と管理費の増加の結果、標準化された操作を維持する必要があるため、課題に直面しています。 プロセスは、一定の市場が利益機会を制限し、欧州全体の研究モデルの成長を制限することにより、それにより、特定の市場をアピールする遅延を調査する見込みです。
分散型臨床試験のための成長の可能性は、デジタルヘルスシステムがドイツやノルディック地域などの国でより高度になるため、重要な約束を示しています。 遠隔監視および環境および身につけられるデータ キャプチャの技術はより速い調査の登録に導くより多くの患者のために可能にします。
人工知能のインパクトは、ヨーロッパのヘルスケア契約研究機関の市場にあるものは何ですか?
欧州の契約研究機関は、人工知能と高度なデジタルツールを使用して、重要な運用タスクの自動化された実行を通じて、臨床試験の設計プロセスを変革します。 ai-poweredシステムは、ロボットプロセスの自動化とともに自然言語処理を使用して、患者識別プロセスとサイトの実現可能性評価とデータクリーニングタスクを実行します。 システムでは、複数の国間調査により、より正確なデータ結果を生成しながら、20%と20%の時間を節約するために、手動作業が少ない試験セットアップと監視プロセスを確立します。 デジタル制御レイヤーは、規制基準の変更に対する試験データを継続的に検証するため、組織がコンプライアンスを監視できるようにします。
機械学習モデルは、試験性能に直接影響する予測機能を追加します。 スポンサーや Cros は、患者の採用率を予測するためにアルゴリズムを使用しており、ドロップアウトリスクを予測し、歴史と現実世界のデータセットに基づいてサイト選択を最適化します。 プロセスは、高価な遅延を低下させるより良い入学効率で結果します, いくつかの研究報告で 15–25% 速い採用サイクル. aiは、実装前にプロトコルの変更をシミュレートすることにより、適応試験設計をサポートし、不確実な条件下での意思決定を強化します。
テクノロジーにより、組織は、より高い試験の成功率、より少ないプロトコルの修正、およびトータル開発費用を削減する3つの主な利点によって、より良い運用結果を達成することができます。 プロセスは、データエコシステムが断片化され、統合コストが高まっているため、特に様々なヨーロッパの規制枠組みを越えた伝統的な臨床システムを統一するための実装課題に直面しています。
主要市場の傾向
- 分散型およびハイブリッド試験の分野は、2020年以降急速に成長を経験しました。欧州の調査研究の40%以上がリモートテスト方式を採用し、旅行制限期間中の運用を継続しました。
- 製薬業界は、2018年の45パーセントから2024年の55パーセント以上でアウトソーシング活動を開始しました。これにより、業界は臨床研究を外部パートナーに委託するようになりました。
- 東部ヨーロッパは、2021年以降、臨床試験の最も人気のある場所になりました。この地域の患者の採用プロセスは、西欧市場よりも15〜20パーセントの時間を削減する必要があるためです。
- 2019年から2024年までの期間は、臨床研究機関がバイオマーカーテストと柔軟な試験開発ニーズのための完全なサービスソリューションを必要とする腫瘍学試験に複雑性を高めました。
- 中規模のスケールで動作するバイオテクノロジー企業は、2020年以降、クロスとの戦略的パートナーシップを確立し始めました。このアプローチにより、社内の運用能力が低下し、初めての試験をスピードアップしました。
- covid-19 の pandemic はリモート・モニタリングおよび環境に優しい使用するために代理店が許可した新しい調整可能な規則を作成しました、従って欧州全域の承諾の標準を変えて下さい。
- 実際の証拠の統合は、スポンサーとして2022後のスピードを獲得し、規制のアプリケーションや市場調査の作業をバックアップします。
- crosは、サービスプロバイダからビジネスモデルを変革し、デジタルヘルス技術とサイトネットワークの能力に投資することで、戦略的開発パートナーになるようにしました。
ユーロピーヘルスケア契約研究組織市場セグメンテーション
タイプ別
第一次臨床研究サービスカテゴリは、企業は、特に最大支出と規制の規模を含む段階的な試験の間に専門的専門知識を必要とする複雑な試験業務を委託しているため、市場リーダーシップを維持しています。 欧州のバイオテクノロジー企業は、バイオマーカー検査および集中診断サービスの要件を高めるため、ラボサービスが継続的な成長を経験しながら、初期研究活動を拡大し、安定したシェアを維持します。 スポンサーは、複数の独立したベンダーパートナーシップを使用するよりも、統合サービスモデルをより効果的に表示しているため、完全なサービスソリューションを好むようになりました。
高度なデータ分析と実際の証拠機能と組み合わせた臨床サービスを提供する作物は現在、市場のトレンドに応じて最高の需要を経験しています。 今後の成長期間は、プロバイダーが既存のサービスと組み合わせて、さまざまなフェーズの臨床試験を通じて運用効率を維持しながら、より価値のある契約を作成できるデジタルツールパッケージを開発する必要があります。
このレポートについて詳しく知る 無料サンプルレポートをダウンロード
によって アプリケーション
臨床試験は、継続的な資金調達を通じて研究の最大の部分を構成します。 医薬品 複雑な実行を必要とする開発パイプラインと欧州ベースの多国籍研究の研究. 医薬品開発サービス部門は、バイオテクノロジークラスターがベンチャーキャピタルの資金調達を経験し、初期研究作業をサポートするため、その地位を維持しています。 euの医療機器の規則は医療機器のテスト サービスのための高められた要求に導かれたより多くの承諾の仕事およびテストプロシージャを今要求します。
スポンサーは規制サービスを探し求めています。なぜなら、ビジネスオペレーションに存在する複数の承認プロセスをナビゲートする必要があるからです。 研究の分野は精密医学およびまれな病気の調査に焦点を合わせます異なった臨床試験方法および研究の参加者を選ぶための特定の技術を要求します。 将来の開発は、より迅速な試験承認プロセスのためのデータ駆動技術を使用して、規制要件と試験テストの適応管理を通じて、より緊密に協力してクロとスポンサーにつながります。
によって エンドユーザー
エンドユーザー市場は、広範な臨床研究プログラムと運用コストを最小限に抑える継続的なニーズのために、製薬企業をサポートしています。 バイオテクノロジー企業は、十分な内部能力が不足し、適応可能な開発プロセスを必要とするため、アウトソーシングに依存する最速成長グループを表しています。 医療機器企業は、厳しいコンプライアンス要件のために継続的な需要を維持します。, 研究機関は、彼らの学術と政府の有益研究プロジェクトを通じて知識を進めながら、.
製薬企業は、バイオテクノロジー企業が急速に拡大できる事業を開発する必要がある間、永続的なパートナーシップを確立することを好むので、異なるグループが関与のユニークなパターンを展示しています。 将来の研究の方向は、カスタマイズされたサービスパッケージとリスク共有契約が市場競争と顧客の保持方法を決定するため、クロ機能とスポンサーの組織サイズ間の強力な接続を確立します。
によって フェーズ
3つの試験フェーズは、その広範なサイズと高価な操作と規制当局の承認を得るための重要な機能のために、作物の主要収益源としてフェーズiiiを確立します。 証拠受容体研究および線量の最適化の研究のための増加の必要性は段階のIIの調査が実質的な市場シェアを維持するために可能にします。 より多くのバイオテクノロジー企業が新製品を作成し、初期の人間のテストを実施しているため、フェーズi試験の数は増加しています。 フェーズ iv サービスの需要は増加します。 企業が新しい安全監視規則の下で市場調査を実施する必要があるため。
需要パターンは、後でフェーズテストは、企業が業務をアウトソーシングし、専門的専門知識を求めているより多くの複雑なサービスを必要とすることを示しています。 未来は、新しい適応型試験設計を分散型メソッドと共に持ち出し、臨床試験がどのようにフェーズを分散させるかを変更し、すべての試験フェーズを完了し、運用パフォーマンスを向上させる方法を探します。
ユーロピーヘルスケア契約研究機関市場を牽引する重要なユースケースは何ですか?
大規模な製薬会社が欧州規制要件に応じて複数の国相IIおよびiii研究を操作しているため、臨床試験センターの主要アプリケーション。 患者の採用やサイト管理やコンプライアンスニーズを含む複数の管轄区域間の運用活動を含むため、このユースケースから最も要求される要件が生じる。
当社は、ユー医療機器の規制に応じて医療機器検査をサポートし、バイオテクノロジー企業向けの規制コンサルティングサービスを提供し、初めての試験に合格しました。 中小企業のバイオテクノロジー企業は、承認経路を調べ、初期開発プロセスの効率的な成長を達成するなど、2つの目的のためにクロに変わります。
分散型試験の新興ユースケースは、リモート監視ツールのアプリケーションを含みます, 実際の証拠は、市場監視のための方法として機能しながら、. 規制当局がデジタルエンドポイントを受け入れるようになったため、モデルがより普及していますが、スポンサーは高度な臨床研究方法を通じて、実質的なデータへのアクセスを迅速に追求しています。
レポートメトリック | インフォメーション |
2025年の市場規模の価値 | 2018年8月21日 |
2026年の市場規模の価値 | 2018年12月16日 |
2033年の収益予測 | 2018年12月1日 |
成長率 | 2026年から2033年までの5.60%の樽 |
基礎年 | 2025年 |
過去のデータ | 2021年 - 2024年 |
予測期間 | 2026 - 2033年 |
レポートカバレッジ | 収益予測、競争力のある風景、成長因子、トレンド |
地域規模 | ユーロピー(ガーマニー、統一王国、フランス、イタリア、スペイン、ユーロピーの残り) |
プロフィールされる主会社 | iqvia、Labcorp、parexel、アイコン、Syneos健康、シャルル川、medpace、ppd、covance、wuxi apptec、pra健康科学、sgs、Eurofins、envigo、clinipace |
カスタマイズスコープ | 自由なレポートのカスタム化(国、地域及び区分の規模)。 あなたの厳密な調査の必要性を満たすために便利なカスタマイズされた購入の選択。 |
レポートセグメンテーション | 用途別(医薬品開発、臨床試験、医療機器試験、規制サービス、その他)、エンドユーザー(製薬会社、バイオテクノロジー会社、医療機器会社、研究所、研究機関、その他)、フェーズ(フェーズI、フェーズII、フェーズiii、フェーズIV、その他)) |
欧州のヘルスケア契約研究機関の市場成長を促進する地域は?
西洋ヨーロッパは、欧州の医療契約研究機関の市場を制御します。 規制システムは、欧州の医薬品機関および先進レベルでの臨床研究施設機能を通じて運営しています。 ドイツのフランスと統一された王国の国は、資格のある調査者と一緒に試験現場や学術病院の広範なネットワークを維持しています。 医薬品本部を含む確立されたシステム バイオテクノロジー クラスターやデジタルヘルスプラットフォームは、アウトソーシングの継続的な要求を維持しています。 堅牢なデータ保護システムと高度な医療ネットワークの組み合わせにより、組織は多数の国が参加する複雑な国際臨床試験を実施することができます。
ノーザンヨーロッパは、患者レジストリの統合とデータ品質管理を優先するために、デマークとフィンランドの使用をスワッゲンする信頼できる地域として動作します。 この領域は、国民の健康データベースと統一されたデジタルシステムによってサポートされている、より小さいが非常に効率的な試験に焦点を合わせ、西欧とは異なります。 クロスは、定期的な規制遵守と政府主催の研究開発の取り組みのために、安定した運用条件を経験します。 透明性の高い患者データアクセスと高い公共医療の関与により、他のシステムが必要とする基本的な運用要件なしで開発を可能にし、成長を維持します。
東ヨーロッパは、欧州規制基準に準拠して、臨床インフラの最近の投資を通じて最速の開発率を実証しています。 ポーランドの飢餓とロマニアの国は、2020年以降、サイトの能力と承認時間を削減しました。 グローバルなスポンサーは、より低い運用コストと患者の採用のコンビネーションが効率向上をもたらすため、トライアルの実行に取り組むことを選択しました。 現在の勢力は、2026と2033の間の新しい市場の要求を捕獲しながら、容量を造りたいと思うcrosおよび投資家のための複数の記入項目ポイントを作成します。
欧州医療契約研究機関の市場における重要な選手であり、どのように競争しますか?
欧州の医療契約研究機関の市場は、統合と専門化の2つの反対市場トレンドの間に存在する競争を経験します。 グローバル・クロクロスは、幅広い業務と完全なサービス提供と医薬品会社との確立された関係を維持し、中規模およびニッチ企業は、特定の治療上の知識と地域の専門知識を使用して競争します。 同社は、データ統合と分散型トライアルシステムと迅速な実行方法により、以前のコストベースの方法よりも優れた結果を提供する技術ベースのサービスを通じて競争し、契約を獲得する能力を決定します。 デジタルプラットフォームと完全サービス拡張は、確立された企業のための市場シェアを維持します。, 新規参入者は、希少疾患に焦点を当て、初期段階の試験に焦点を合わせ、それらの柔軟な操作と専門知識.
iqviaが開発した高度な分析と現実的なデータプラットフォームは、適応型予測試験を作成するために必要なツールでスポンサーを提供します。 有能なインサイトに投資し、ヘルスケア組織とのパートナーシップを開発する組織は、データにアクセスする能力を高め、より優れた試験結果をもたらします。 icon plcは、臨床開発をヘルスケアインテリジェンスに接続し、複数の買収により、プロジェクトスケジュールと運用コストを適切に制御できる完全なサービスソリューションを提供します。 パレクセルは、専門コンサルティングサービスと実行支援を通じて、欧州の規制要件をナビゲートするのに役立ちます。
Labcorpの薬剤の開発の組織は臨床試験操作と診断テストをリンクするのに実験室設備を使用します。これにより、バイオマーカーベースの研究と患者のグループ化をよりよく設計できます。 Syneos Healthは、市場アクセスと臨床開発のためのサービスを接続する包括的なビジネスモデルを提供します。単一のシステムを介して、シームレスな試行実行と市場参入ソリューションを提供します。
会社案内
最近の開発ニュース
october 2025では、熱漁師はclarioの獲得の統合によって臨床試験サービスを拡張します: 熱漁師は積極的に買収を進めています clarioホールディングス, 欧州臨床試験データと分析サービスのフットプリントを強化. clarioは、臨床試験データのキャプチャと管理を専門としています。 段階的な試験のために、ヨーロッパ全域でCrosによって使用されるコアインフラストラクチャ。 2026年初旬の取引が予想されます。
アプライル2026、マイクロバイオロジービジネスをastorgに潜む熱漁師: サーモフィッシャー科学は、欧州プライベートエクイティ会社に微生物事業を販売することに同意しました アストラグ 〜$1.075億取引。 単位はヨーロッパで Cro-enabled の実験室サービスに密接につながっている臨床および薬剤のテストのワークフローを支えます。 領域における委託された臨床支援能力の継続的な統合を反映しています。
ソース: https://www.wsj.com からのツイート
戦略的インサイトは、欧州のヘルスケア契約研究機関市場の将来を定義するもの?
ヨーロッパのヘルスケア契約の調査の組織の市場は、デジタルインフラと現実的なデータと分散型の試験実行を使用して、競争上の優位性を作成するプラットフォームベースのシステムに対する構造的なシフトの後にいます。 この動きの背後にある基本ドライバーは、組織が開発時間を短縮し、大量のデータを必要とする複雑な治療法を開発し、バイオロジックやパーソナライズド医療などの治療を創出する必要が伴います。 市場は、組織が完全なデータと実行パートナーとして役立つ能力を開発する戦略的コラボレーションに向けて動きます。
患者のデータ使用に関するさまざまな規則とデータの断片化の隠された危険性は、AI主導の試験モデルがさまざまな国で動作するのに苦労する危険性を作成します。 この制限は、組織がデジタルトランスフォーメーションイニシアチブを通じて達成することを期待する効率性の利点を減らす国際的な標準化努力のための障害を作成します。
東部ヨーロッパでは、その開発インフラと規制枠組みにより、より簡単な患者様の採用をスケールアップできるため、ハイブリッドトライアル拡張のための新たな機会を提示します。 市場参加者は、規制の遵守と運用の柔軟性を確保しながら、データアクセスを維持するための目標を達成するために、地域のサイトネットワークを確立し、システム相互運用性を有効にするデジタルプラットフォームを開発する必要があります。
ユーロピーヘルスケア契約研究組織市場レポートセグメンテーション
タイプ別
- 臨床研究サービス
- 前処理サービス
- ラボサービス
- その他
用途別
- 医薬品開発
- 臨床試験
- 医療機器のテスト
- 規制サービス
- その他
エンドユーザーによる
- 製薬会社
- バイオテクノロジー企業
- 医療機器会社
- 研究機関
- その他
段階によって
- フェーズi
- フェーズII
- フェーズiii
- フェーズ iv
- その他
よくある質問
よくある質問への素早い回答をご覧ください。
市場規模は、2033年に12.7億米ドルとなりました.
欧州医療契約研究機関の市場の主要なセグメントは、アプリケーション(医薬品開発、臨床試験、医療機器試験、規制サービス、その他)、エンドユーザー(製薬会社、バイオテクノロジー会社、医療機器会社、研究機関、その他)、フェーズ(フェーズi、フェーズii、フェーズiii、フェーズiv、その他)によって、タイプ(臨床研究サービス、ラボサービス、その他)によって、あります.
ヨーロッパの医療契約研究機関の市場の主要なプレーヤーは、iqvia、labcorp、parexel、アイコン、syneosの健康、シャルル川、medpace、ppd、covance、wuxi apptec、pra健康科学、sgs、eurofins、envigo、clinipaceです.
欧州医療契約研究機関市場の現在の市場規模は、2025年に8.21億米ドルです.
ヨーロッパのヘルスケアの契約の調査の組織の市場は 5.60% です.
- ログイン
- ラボ
- パレクセル
- アイコン
- シナジーヘルス
- シャルル川
- メディパス
- ログイン
- コーヴァンス
- wuxiアプリテック
- プラ健康科学
- ログイン
- ユーロフィンズ
- ログイン
- ログイン
最近発行されたレポート
-
Apr 2026
コードブラッドバンキングサービス市場
コード血液銀行サービス市場規模、サービスの種類(回収、処理、保管)によるシェア&分析レポート、銀行タイプ(民間銀行、公共銀行、およびハイブリッド銀行)、コンポーネント(コード血液、コード組織)、エンドユーザー(病院、研究機関、バイオテクノロジー企業など)、および地理(北アフリカ、ヨーロッパ、アジア太平洋、中東、アフリカ、南、中央2031)、2021 - 2021 - 2021 - 2021 - 2021
-
Apr 2026
ELISAプロセッサー市場
エリサプロセッサは、タイプ(光学フィルターエリサアナライザアナライザアナライザアナライザ)による市場規模、シェア&分析レポート、モード(自動化エリサアナライザアナライザアナライザ)、アプリケーション(免疫学、ワクチン開発、医薬品監視、その他)、エンドユーザー(バイオテクノロジー企業、製薬会社、受託研究機関、および診断ラボ)、および地理情報(北東アジア、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、南米、
-
Apr 2026
顕微鏡のスライドの走査器市場
顕微鏡のスライドの走査器はタイプ(携帯用顕微鏡のスライドの走査器およびデスクトップの顕微鏡のスライドの走査器)、適用(生物的研究、薬、獣医および他の)および地理学(北のアメリカ、ヨーロッパ、アジアpacific、中間の東およびアフリカ、南および中央アメリカ)、2021 - 2031年
-
Apr 2026
マイクロウェーブ調理器市場
マイクロウェーブ調理器市場規模、材料タイプ(プラスチック、ガラス、セラミック、シリコン、金属)によるシェア&分析レポート、アプリケーション(調理、再加熱、および解凍)、エンドユーザー(家庭用、商業(レストラン、ホテル、カフェ)、およびフードサービス業界)、販売チャネル(オンライン小売、オフライン小売(スーパーマーケット、スーパーマーケット、専門店)、および直接販売(会社アウトレット)および地理(中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/東/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/中央/南/東/東/南/南/東/東/南/南/南/南/南/南/東/東/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/南/


