france farmaceutico cro dimensione del mercato e previsioni
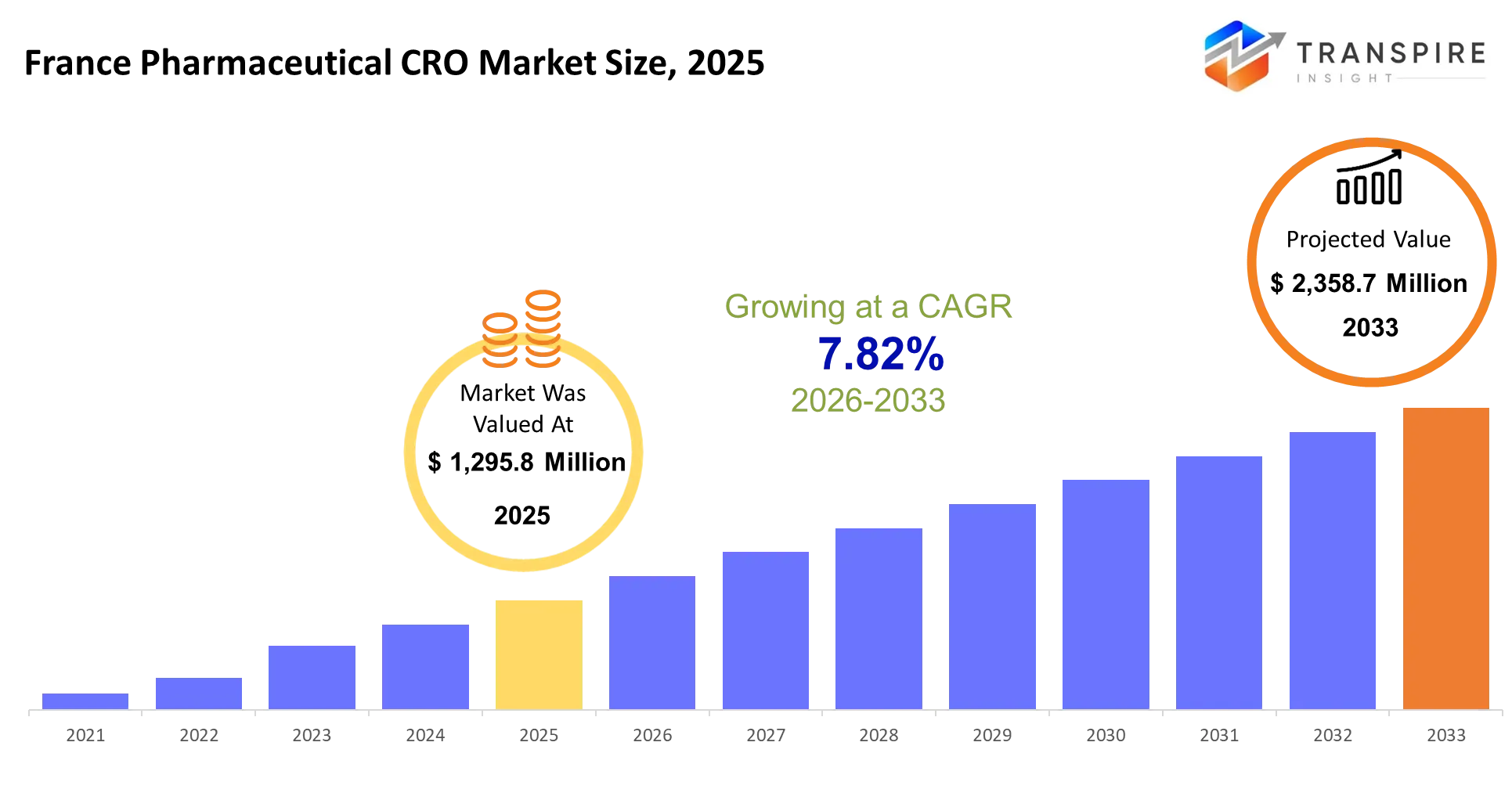
- franco farmaceutico cro dimensione del mercato 2025: usd 1.295,8 milioni
- franco farmaceutico cro dimensione del mercato 2033: usd 2,358.7 milioni
- france farmaceutica cro mercato cagr: 7,82%
- segmenti di mercato del cro farmaceutico franco: per tipo (ricerca clinica, ricerca preclinica, servizi di laboratorio, altri); per applicazione (sviluppo della droga, studi clinici, studi tossicologici, gestione dei dati, altri); per utente finale (società farmaceutiche, aziende biotecnologiche, istituti di ricerca, altri); per fase (fase ii, fase ii, fase iv, altri)
per saperne di più su questo rapporto, scaricare gratuitamente il report del campione
Francia farmaceutica cro sintesi del mercato
il mercato franco farmaceutico cro è stato valutato a 1.295,8 milioni nel 2025. si prevede di raggiungere usd 2.358.7 milioni entro il 2033, crescendo a un cagr del 7,82%. le organizzazioni di ricerca del contratto forniscono servizi di ricerca esterna alle aziende farmaceutiche e biotecnologiche, trattando tutto dagli studi preclinici alla sorveglianza post-mercato di fase iv. i servizi di ricerca clinica rappresentano il 65% del mercato francese perché gli sponsor preferiscono trasferire la gestione complessa di prova a fornitori specializzati piuttosto che mantenere le capacità interne in più aree terapeutiche e giurisdizioni normative.
tre cambiamenti normativi tra il 2020 e il 2025 riformulano il funzionamento dei cros francesi. In primo luogo, il regolamento di studi clinici eu ha introdotto processi di approvazione armonizzati in tutti gli stati membri, che ha ridotto la variabilità della linea temporale, ma ha aumentato i requisiti di documentazione in anticipo. seconda, la piattaforma nazionale di dati sulla salute di france ha aperto l'accesso ai dataset delle prove reali che gli sponsor possono ora collegare ai risultati della prova clinica, creando la domanda di cros con le capacità di bioinformatica. terzo, ansm ha iniziato ad accettare protocolli di prova decentrati che permettono il monitoraggio remoto del paziente, che ha spostato la selezione del sito di ricerca lontano dalle reti ospedaliere tradizionali verso i fornitori di salute domestica e piattaforme di telemedicina.
L'attuale espansione del mercato è guidata da aziende biotecnologiche che esternano i lavori di sviluppo del tardo stadio che in precedenza hanno gestito internamente. piccole e medie imprese biotecnologiche non hanno le competenze normative per navigare ema e la rete del sito per eseguire in modo efficiente le prove multi-paese. cros offrono a queste aziende l'accesso a relazioni di ricerca consolidate, competenze terapeutiche e specialisti di affari normativi su base di progetto piuttosto che come headcount permanente. questo modello di business consente agli sponsor biotech di preservare i contanti, accelerando i tempi di sviluppo, che conta quando i cicli di finanziamento di venture richiedono un progresso clinico dimostrabile ogni 18-24 mesi.
chiave france farmaceutica cro approfondimenti di mercato
- I servizi di ricerca clinica dominano il mercato franco-farmaceutico cro con una quota del 65% nel 2024, guidata da una crescente esternalizzazione della fase ii e la gestione di fase ii trial.
- I servizi preclinici di ricerca rappresentano il 22% del mercato nel 2024, sostenendo i candidati di droga che richiedono test tossicologici e studi farmacocinetici.
- applicazioni di sviluppo del farmaco rappresentano il 41,3% della domanda di servizi cro nel 2024, in quanto le aziende farmaceutiche superano lo sviluppo della formulazione e il test di stabilità.
- Le applicazioni di studi clinici detengono la quota di mercato del 38,7% nel 2024, concentrata in oncologia, immunologia e aree terapeutiche di malattia rara dove il reclutamento dei pazienti è impegnativo.
- le aziende farmaceutiche costituiscono il 52,8% della domanda dell'utente finale nel 2024, le attività di sviluppo clinico non-core per focalizzare le risorse interne sulla scoperta e la commercializzazione.
- Le aziende biotecnologiche rappresentano il 31,4% del mercato nel 2024 e rappresentano il segmento degli utenti finali in crescita più rapida, espandendosi al 9,1% passando dal 2033.
- Gli studi di fase iii generano il 43,2% dei ricavi di ricerca clinica nel 2024, che richiedono grandi popolazioni di pazienti e lunghi periodi di monitoraggio che favoriscono cros full-service.
- gli studi di fase ii contribuiscono al 28,6% dei ricavi nel 2024, con una crescente domanda di progetti di prova adattativi che richiedono capacità di statistica e gestione dei dati specializzate.
- iqvia detiene circa il 15-18% del mercato cro francese nel 2025, sfruttando i suoi servizi integrati di analisi dei dati e di sperimentazione clinica in più aree terapeutiche.
- labcorp ha ampliato le sue operazioni di sviluppo clinico francese del 20% nel 2024, aggiungendo siti di ricerca e specialisti di area terapeutica per servire la crescente domanda di biotecnologia.
Quali sono i principali driver, restrizioni e opportunità nel mercato cro farmaceutico franco?
il principale driver di crescita è aziende farmaceutiche che passano da outsourcing selettivo a partenariati strategici in cui cros gestisce interi programmi di sviluppo piuttosto che singoli studi. Le grandi aziende farmaceutiche ora assegnano contratti pluriennali che coprono preclinici attraverso il lavoro di fase iii per specifiche aree terapeutiche, che fornisce ai cros la visibilità dei ricavi e permette loro di investire in capacità specializzate come i registri dei pazienti con malattie rare o piattaforme di biomarcatori oncologici. iqvia, syneos health e parexel hanno strutturato tutte le loro operazioni di french intorno a queste partnership strategiche, dedicando team a specifici account di sponsor piuttosto che operare come fornitori di servizi transazionali. l'impatto finanziario è sostanziale: i contratti di partnership strategici tipicamente durano da tre a cinque anni e coprono portafogli di sviluppo del valore di centinaia di milioni di euro, rispetto ai contratti monostudio che durano dai 18 ai 36 mesi.
il controllo più significativo è i vincoli di capacità del sito di investigatore in aree terapeutiche ad alta domanda. centri oncologia french e specialisti immunologia sono sovrascritti con protocolli di prova, che crea pazienti che reclutano strozzature che ritardano lo studio timeline indipendentemente da quanto efficiente il cro gestisce altri aspetti dell'esecuzione di prova. cros non può semplicemente aprire nuovi siti per risolvere questo problema perché gli investigatori qualificati richiedono anni di formazione e certificazione di regolamentazione. il vincolo è particolarmente acuto nelle prove di malattia rara in cui la francia potrebbe avere solo cinque o dieci centri con popolazioni pazienti rilevanti, e questi centri sono già impegnati a protocolli concorrenti multipli. questo costringe cros ad estendere le timeline di reclutamento o espandersi in siti di ricerca meno esperti, uno dei quali aumenta i costi e i rischi per studiare la qualità.
l'opportunità più chiara è nei servizi di prova del mondo reale che collegano i dati di prova clinica al database sanitario nazionale di france. ansm ora accetta prove del mondo reale per sostenere le sottomissioni normative per alcune indicazioni, e gli sponsor hanno bisogno di cros che possono progettare studi ibridi che combinano la metodologia di prova controllata randomizzata tradizionale con i dati osservazionali dai record di salute elettronica. questo richiede capacità che la maggior parte dei cros attualmente non possiedono: gli scienziati di dati che comprendono analisi sanitarie, specialisti di regolamentazione che sanno come strutturare le presentazioni di prove del mondo reale, e le relazioni stabilite con le autorità di dati sanitari francesi. cros che costruiscono queste capacità catturerà un lavoro ad alto margine che non può essere facilmente replicato dai concorrenti che mancano delle infrastrutture tecniche e delle competenze normative per eseguire questi progetti di studio ibridi.
qual è l'impatto dell'intelligenza artificiale sul mercato cro farmaceutico franco?
I sistemi di identificazione dei pazienti alimentati ora schermano i record di salute elettronica per trovare i candidati che soddisfano specifici criteri di inclusione di prova, che accelera le linee temporali di reclutamento identificando i pazienti idonei prima dei siti manualmente rivedere i grafici. iqvia e labcorp hanno implementato modelli di apprendimento automatico in sistemi sanitari francesi che contrassegnano i pazienti in base a codici di diagnosi, valori di laboratorio, storie di farmaci e altri marcatori clinici. questi sistemi hanno ridotto il tempo di screening mediano da settimane a giorni in siti con record integrati di salute elettronica, anche se l'adozione rimane limitata a reti ospedaliere più grandi con dati digitali del paziente. il beneficio operativo è più visibile nelle prove di malattia rara in cui la revisione manuale del grafico precedentemente richiesto mesi di tempo di indagine per identificare anche una manciata di pazienti idonei.
l'elaborazione del linguaggio naturale automatizza il monitoraggio della sicurezza estraendo eventi avversi da note cliniche, rapporti di laboratorio e diari del paziente senza richiedere l'inserimento manuale dei dati da parte dei coordinatori del sito. syneos salute e icona hanno implementato sistemi nlp che scansionano continuamente la documentazione di prova per i segnali di sicurezza, segnalando potenziali gravi eventi avversi che richiedono una segnalazione immediata alle autorità di regolamentazione. questa automazione ha ridotto i tempi di segnalazione di eventi avversi mediani da 48-72 ore a meno di 24 ore nei siti che utilizzano la tecnologia, che conta quando i requisiti normativi richiedono la segnalazione di eventi avversi gravi entro 24 ore di consapevolezza dell'investigatore. la limitazione è che l'accuratezza nlp dipende dalla qualità della documentazione, e le note cliniche french spesso includono terminologia medica a breve e non standardizzata che riducono l'affidabilità di estrazione automatizzata.
la barriera primaria all'adozione più ampia ai è la frammentazione dei dati tra i fornitori di servizi sanitari francesi. I registri dei pazienti rimangono siloed all'interno di singoli sistemi ospedalieri, reti sanitarie regionali e pratiche private, che impedisce ai cros di formazione ai modelli su set di dati completi che riflettono le popolazioni di pazienti del mondo reale. Inoltre, le norme di protezione dei dati francesi richiedono un esplicito consenso del paziente per l'uso secondario dei dati sanitari in contesti di ricerca, che aggiunge la conformità in testa che molti cros trovano proibitivo per i progetti di sviluppo ai. questo crea un paradosso in cui le applicazioni ai più preziose richiedono grandi e diversi set di dati che i quadri normativi francesi rendono difficile da assemblare legalmente.
tendenze chiave del mercato
- Gli sponsor farmaceutici passarono dall'acquisto di servizi transazionali a partenariati strategici pluriennali tra il 2022 e il 2024, consolidando le relazioni cro da cinque o sei fornitori a due o tre fornitori preferiti.
- L'adozione decentralizzata del processo ha accelerato nel 2023 quando l'ansm ha pubblicato una guida che accetta il monitoraggio remoto dei pazienti e le visite di salute domestica come alternative valide alle valutazioni basate sul sito.
- Le aziende biotecnologiche hanno incrementato l'outsourcing cro da un 60% medio di spesa di sviluppo nel 2021 a oltre il 75% entro il 2024, guidato dalla pressione del capitale di rischio per ridurre al minimo i costi fissi.
- La salute iqvia e syneos hanno ampliato i loro specialisti della zona terapeutica francese del 25-30% tra il 2023 e il 2025, assumendo oncologia ed esperti di malattie rare per sostenere i contratti di partenariato strategico.
- I servizi di prova del mondo reale sono emersi come un'offerta distinta nel 2024, con la creazione di gruppi dedicati alla progettazione di studi ibridi che combinano i dati di prova e i record di salute osservazionale.
- I tempi di reclutamento dei pazienti per le prove oncologiche sono aumentati da 12 mesi a 16-18 mesi tra il 2022 e il 2024 a causa dei vincoli di capacità del sito di investigatore e dei protocolli concorrenti.
- cros cinese è entrato nel mercato francese nel 2024, offrendo i servizi fase i e fase iniziale ii al 20-25% sotto i prezzi inorganici per stabilire operazioni europee.
- i servizi di gestione dei dati sono cresciuti più velocemente del monitoraggio clinico tra il 2023 e il 2025, riflettendo una maggiore domanda di sponsor per analisi avanzate e visualizzazione dei dati in tempo reale durante le prove.
franco farmaceutico cro segmentazione di mercato
per tipo
i servizi di ricerca clinica dominano il mercato cro francese al 65% del fatturato totale. questo segmento riguarda il reclutamento dei pazienti, il monitoraggio del sito, la raccolta dei dati e il supporto di presentazione normativo per la fase iv trial clinici. il dominio riflette un cambiamento strutturale in cui gli sponsor farmaceutici e biotecnologici esternano la gestione delle prove a cros piuttosto che mantenere i team di operazioni cliniche interne. cros full-service come iqvia, labcorp e syneos salute operano come il braccio di sviluppo clinico dello sponsor, la gestione delle relazioni di ricerca, le interazioni normative e la supervisione della qualità dei dati attraverso più prove contemporaneamente. la proposizione del valore è il trasferimento del rischio: gli sponsor pagano i cros per fornire i pazienti iscritti e i dati puliti sul programma, mentre il cro assorbe la complessità operativa e la variabilità della linea temporale.
I servizi preclinici di ricerca rappresentano il 22% del mercato, comprendendo studi tossicologici, analisi farmacocinetica e sviluppo della formulazione che si verificano prima delle prove umane. Questo segmento serve aziende biotech di primo piano e team di scoperta farmaceutica che hanno bisogno di capacità di laboratorio specializzate senza costruire strutture dedicate. Il fiume, la covanza e le eurofins dominano i servizi preclinici francesi attraverso la proprietà di laboratori certificati glp dotati di studi di tossicologia regolamentare. il segmento è tecnicamente esigente perché gli studi preclinici devono soddisfare rigidi standard normativi per la qualità e la riproducibilità dei dati, che richiedono metodi analitici convalidati e sperimentati laboratorio scienziati. i margini sono superiori alla ricerca clinica perché i costi di commutazione sono sostanziali una volta che uno sponsor qualifica un laboratorio specifico per un programma di sviluppo.
servizi di laboratorio e altre offerte specializzate rappresentano insieme il 13% del mercato. Questo include test bioanalitici, servizi di laboratorio centrali per gli studi clinici e capacità di nicchia come test di dispositivi medici o convalida della salute digitale. il segmento è cresciuto più velocemente della ricerca clinica di base tra il 2023 e il 2025 perché gli sponsor richiedono sempre più servizi integrati che combinano la gestione della sperimentazione clinica con l'analisi di laboratorio specializzata. per esempio, le prove di oncologia spesso hanno bisogno di sviluppo diagnostico del compagno insieme droga test, che richiede cros che possono coordinare la convalida del biomarcatore, la raccolta di campioni clinici e lo sviluppo del test diagnostico come un programma unificato. cros che offrono questi servizi integrati catturano maggiori ricavi per progetto rispetto a quelli che forniscono solo la gestione clinica di prova.
per saperne di più su questo rapporto, scaricare gratuitamente il report del campione
per applicazione
Le applicazioni di sviluppo del farmaco conducono al 41,3% della domanda di mercato, coprendo lo sviluppo della formulazione, i test di stabilità, lo sviluppo dei metodi analitici e i servizi di supporto alla produzione. aziende farmaceutiche esternalizzano queste attività a cros quando le funzioni di sviluppo interno non hanno capacità o competenze specializzate per specifiche sfide di formulazione. per esempio, lo sviluppo di formulazioni stabili per i biologici richiede attrezzature specializzate e competenze che la maggior parte degli sponsor non mantengono in-house. cros come catalent, patheon e lonza forniscono queste capacità su base contrattuale, permettendo agli sponsor di avanzare candidati attraverso lo sviluppo senza investimenti di capitale nei laboratori di formulazione. l'applicazione è marginal-accretive perché il lavoro di sviluppo della formulazione è tecnicamente complesso e richiede scienziati esperti che comandano i tassi di fatturazione premium.
Le applicazioni di trial clinici rappresentano il 38,7% della domanda, focalizzate specificamente sui servizi di registrazione del paziente, gestione del sito e esecuzione di prova piuttosto che su un più ampio supporto allo sviluppo. questo segmento differisce dai servizi di ricerca clinica in quanto cattura solo il componente di esecuzione di prova, escludendo strategia di regolazione, analisi dei dati e attività post-trial. l'applicazione è cresciuta tra il 2022 e il 2024 come aziende biotech cercato cros che potrebbero gestire il reclutamento dei pazienti e il monitoraggio del sito pur mantenendo altre attività di sviluppo in-house. questo inflessibile ha permesso agli sponsor di esternalizzare gli aspetti più complessi e tempo-sensibili di sviluppo clinico, mantenendo il controllo sulle decisioni strategiche come la selezione endpoint e il design di prova.
studi tossicologici, gestione dei dati e altre applicazioni rappresentano insieme il 20% del mercato. studi tossicologici sono obbligatori per le presentazioni normative e richiedono strutture certificate glp che la maggior parte degli sponsor non operano internamente. i servizi di gestione dei dati sono cresciuti rapidamente in quanto le prove generano volumi crescenti di dati elettronici da wearables, dispositivi di monitoraggio remoto, e risultati riferiti ai pazienti che richiedono piattaforme di database specializzate e capacità di analisi statistica. cros che ha investito in piattaforme di dati basate su cloud e analisi in tempo reale tra il 2020 e il 2025 ha catturato crescente domanda di sponsor per il monitoraggio trasparente della prova e progetti di prova adattativi che richiedono analisi continua dei dati piuttosto che database bloccati tradizionali esaminati solo al completamento dello studio.
per utente finale
le aziende farmaceutiche costituiscono il 52,8% della domanda cro in franchigia. grandi aziende farmaceutiche esternalizzare programmi di sviluppo specifici in cui la capacità interna è limitata o l'esperienza di area terapeutica è carente. per esempio, una società con forti capacità oncologiche potrebbe esternalizzare lo sviluppo di malattie rare a cros con registri di pazienti stabiliti e reti di ricerca in tali indicazioni. la decisione di outsourcing è economicamente guidata: mantenere in-house le operazioni cliniche per le aree terapeutiche in cui l'azienda gestisce solo uno o due prove all'anno è proibitivo di costo rispetto a coinvolgere cros su base di progetto. Questo crea una domanda stabile di cros in aree terapeutiche dove l'interesse dello sponsor è sostenuto, ma i portafogli aziendali individuali sono limitati.
Le aziende biotecnologiche rappresentano il 31,4% del mercato e rappresentano il segmento in crescita più rapida al 9,1% di cagr fino al 2033. queste aziende tipicamente mancano di capacità di sviluppo clinico interno e esternalizzano la maggior parte dei lavori di sviluppo da studi preclinici attraverso studi di fase iii. Il driver di crescita è la dinamica di finanziamento del capitale di rischio: le aziende biotecnologiche dovrebbero dimostrare rapidamente il progresso clinico, riducendo al minimo le ustioni di cassa, il che rende il outsourcing a cros più finanziariamente attraente che la costruzione di capacità interne che richiedono un headcount fisso. cros fornisce agli sponsor biotech una capacità flessibile che ridimensiona le esigenze del programma, fatturando solo per progetti attivi, piuttosto che richiedere pagamenti continui di mantenimento o personale retribuito.
istituti di ricerca e altri utenti finali contribuiscono al 15,8% della domanda. centri medici accademici e organizzazioni di ricerca governative impegnano cros per le prove avviate dagli investigatori e gli studi di salute pubblica che richiedono la raccolta e il monitoraggio dei dati di livello normativo. Questi clienti tipicamente operano sul finanziamento di sovvenzioni con bilanci fissi e linee temporali definite, che richiedono cros per fornire servizi all'interno di vincoli di costo rigidi. il segmento offre margini inferiori rispetto al lavoro farmaceutico commerciale, ma fornisce ai cros l'accesso a nuovi approcci terapeutici e alle popolazioni di malati rari che in seguito si traducono in opportunità di sviluppo commerciale quando le scoperte accademiche si muovono verso l'approvazione normativa e la commercializzazione.
per fase
le prove di fase iii generano il 43,2% dei ricavi di ricerca clinica a causa delle loro grandi popolazioni di pazienti, periodi di monitoraggio prolungati e requisiti normativi complessi. un tipico processo di oncologia fase iiii in france potrebbe iscrivere 300-500 pazienti attraverso 25-40 siti di ricerca in tre a quattro anni, che richiedono il monitoraggio del sito, la gestione dei dati, la segnalazione della sicurezza e il coordinamento normativo durante il periodo di studio. cros fornisce valore gestendo questa complessità operativa, consentendo agli sponsor di concentrarsi sulle decisioni strategiche in materia di progettazione e presentazione delle normative. la concentrazione dei ricavi in fase iii riflette sia il costo diretto di esecuzione di prova su larga scala e gli sponsor premium di rischio pagano per i cros per consegnare su tempi di iscrizione aggressivi che determinano le date di lancio del prodotto.
Gli studi di fase ii contribuiscono al 28,6% dei ricavi, focalizzati sugli studi di dosaggi e sulle valutazioni iniziali di efficacia nelle popolazioni più piccole dei pazienti. questi studi utilizzano sempre più progetti adattativi che modificano i criteri di iscrizione o i programmi di dosaggio basati su risultati intermedi, che richiedono cros con forti capacità statistiche e di gestione dei dati. la complessità tecnica delle prove adattative crea barriere all'ingresso per i cros più piccoli che non hanno competenze specialistiche, consentendo ai fornitori full-service più grandi di comandare prezzi premium. fase ii lavoro è strategicamente importante per cros perché gli sponsor che completano con successo fase ii tipicamente continuano con lo stesso cro in fase iii, creando multi-year ricavi pipelines dal coinvolgimento del primo stadio.
fase i, fase iv e altre fasi di prova insieme rappresentano il 28,2% dei ricavi. le prove di fase i sono relativamente piccole ma tecnicamente impegnative, che richiedono strutture specializzate per studi di sicurezza di primo in-umano e monitoraggio intensivo del paziente. studi post-marketing fase iv stanno crescendo come regolatori sempre più richiedono prove reali per integrare i dati clinici pre-approvazione. cros che offrono sia la gestione tradizionale di prova iv fase e le capacità di prova del mondo reale che combinano i dati di prova con i record di salute osservativa stanno catturando crescente domanda di sponsor per i programmi integrati di sorveglianza post-marketing che soddisfano i requisiti normativi, generando prove per i negoziati di rimborso del pagamento e sviluppo di guida clinica.
Quali sono i casi chiave di utilizzo che guidano il mercato franco farmaceutico cro?
l'applicazione primaria è la gestione di studi di fase full-service iii per le aziende biotecnologiche che non hanno capacità di operazioni cliniche interne. questi sponsor impegnano cros a gestire tutti gli aspetti dell'esecuzione di prova dalla selezione del sito attraverso il blocco di database, la presentazione normativa e il monitoraggio della sicurezza post-approvazione. un impegno tipico potrebbe comportare un'indicazione di malattia rara in cui lo sponsor biotech ha completato gli studi di fase ii proof-of-concept e ha bisogno di un cro per eseguire il programma di fase iii fondamentale richiesto per l'approvazione di ema. Il cro fornisce reti di siti di ricerca, competenze regolamentari, strategie di reclutamento dei pazienti e infrastrutture di gestione dei dati su base chiavi in mano, consentendo all'azienda biotech di avanzare verso la commercializzazione senza costruire il headcount delle operazioni cliniche permanenti.
domanda adiacente proviene da grandi aziende farmaceutiche outsourcing programmi di sviluppo terapeutico area-specifico. Ad esempio, un'azienda con un'esperienza di immunologia limitata potrebbe coinvolgere un cro per gestire tutto lo sviluppo clinico per un asset di immunologia acquisito, sfruttando i rapporti consolidati del cro con reumatologia francese e ricercatori dermatologici. Questi partenariati strategici tipicamente abbracciano più prove in diversi anni, fornendo il cro con ricavi prevedibili, dando allo sponsor l'accesso alle competenze dell'area terapeutica senza espansione permanente del personale. la logica commerciale è specializzazione: i cros che si concentrano su specifiche aree terapeutiche sviluppano relazioni di ricerca profonde e l'esperienza di progettazione del protocollo che i team di sviluppo interno generalisti non possono replicare.
casi di uso emergente centro su disegni di prova ibridi che combinano le tradizionali prove randomizzate controllate con prove reali da database di salute francese. sponsor agganciano i cros a studi di progettazione in cui il braccio di controllo utilizza pazienti abbinati da record di salute elettronica piuttosto che iscrivere un coorte placebo separato, che riduce i costi di prova e accelera i tempi di iscrizione. iqvia e syneos salute hanno stabilito team dedicati per eseguire questi studi ibridi, richiedendo scienziati di dati, epidemiologi, e specialisti di regolamentazione che comprendono sia la metodologia di prova clinica che gli standard di prova del mondo reale. l'applicazione è tecnicamente impegnativa, ma offre sponsor consistenti risparmi sui costi, con alcuni progetti ibridi che riducono i costi di fase ii del 30-40% rispetto alle tradizionali prove completamente iscritta.
report metriche | dettagli |
valore dimensione del mercato in 2025 | usd 1.295,8 milioni |
valore dimensione del mercato in 2026 | usd 1,392,6 milioni |
previsione delle entrate nel 2033 | usd 2.358.7 milioni |
tasso di crescita | da 2026 a 2033 |
anno di base | 2025 |
dati storici | 2021 – 2024 |
periodo di previsione | 2026 – 2033 |
copertura report | previsione delle entrate, paesaggio competitivo, fattori di crescita e tendenze |
Ambito regionale | Franco |
aziende chiave profilate | iqvia, labcorp, syneos health, parexel, icon plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat |
campo di personalizzazione | Personalizzazione della relazione gratuita (area regionale e segmento). avvalersi di opzioni di acquisto personalizzate per soddisfare le vostre esigenze di ricerca esatte. |
relazione segmentazione | per tipo (ricerca clinica, ricerca preclinica, servizi di laboratorio, altri); per applicazione (sviluppo della droga, studi clinici, studi tossicologici, gestione dei dati, altri); per utente finale (società farmaceutiche, biotecnologie, istituti di ricerca, altri); per fase (fase i, fase ii, fase iii, fase iv, altri) |
che cosa sta guidando la crescita nel mercato cro farmaceutico franco?
france offre tre vantaggi strutturali che altri mercati europei non possono replicare a scala equivalente. In primo luogo, il paese gestisce un sistema sanitario centralizzato con registri di salute elettronici completi che coprono oltre 65 milioni di cittadini, fornendo cros con capacità di identificazione del paziente e accesso di prova reale che i sistemi sanitari frammentati non possono corrispondere. secondo, france mantiene dense concentrazioni di siti di ricerca specializzati a paris, lyon e marseille dove centri medici accademici, ospedali didattici e istituti di ricerca cluster all'interno della prossimità geografica, che semplifica la logistica di prova e riduce i costi di monitoraggio rispetto alle reti di siti geograficamente dispersi. terzo, l'ansm ha stabilito tempi di revisione regolamentare prevedibili e una chiara guida sulle metodologie di prova emergenti come i protocolli decentralizzati e le prove del mondo reale, che riduce l'incertezza per la pianificazione degli sponsor programmi di sviluppo pluriennali.
la dinamica competitiva in france differisce da altri mercati europei perché i requisiti linguistici e normativi creano barriere naturali all'ingresso per i non-eu cros. protocolli di prova, documenti di consenso informati e presentazioni regolamentari devono essere in francese, che richiede personale locale dedicato piuttosto che squadre europee centralizzate operanti in inglese. Inoltre, le norme di protezione dei dati francese impongono requisiti specifici per la gestione dei dati sanitari che differiscono da disposizioni generali gdpr, che richiedono cros per mantenere i programmi di conformità specifiche della franchigia. Queste barriere proteggono giocatori affermati come iqvia, labcorp e syneos salute che hanno operato in Francia per decenni e investito in infrastrutture locali, creando al contempo maggiori costi di ingresso per i nuovi concorrenti che tentano di stabilire operazioni di french.
il segmento di domanda in crescita è una prova di malattie rare in cui il database sanitario nazionale di france consente una rapida identificazione del paziente per le indicazioni ultra rare. in condizioni che interessano meno di 1.000 pazienti francesi, il reclutamento basato sul sito tradizionale può richiedere anni perché i ricercatori devono controllare manualmente i record medici per identificare i candidati idonei. I cros che hanno stabilito accordi di accesso ai dati con le autorità sanitarie francesi possono controllare elettronicamente l'intera popolazione del paziente nazionale, identificando i pazienti idonei in settimane piuttosto che mesi. questa capacità ha reso france una posizione preferita per le prove europee di malattie rare, con gli sponsor sempre più scegliendo siti francesi come i paesi leader per gli studi multinazionali in indicazioni ultra-rare dove la velocità di identificazione del paziente determina i tempi generali del programma.
chi sono i principali attori del mercato cro farmaceutico franco e come competono?
il mercato cro francese opera come una struttura a due livelli. iqvia, labcorp, syneos health, parexel e icon detengono collettivamente circa 55-60% quota di mercato e competono come fornitori di servizi completi che offrono capacità integrate da preclinici attraverso fase iv. queste aziende competono su competenze area terapeutica, reti di siti di ricerca e piattaforme tecnologiche che forniscono agli sponsor una visibilità di prova in tempo reale. le nicchie medie e più piccole occupano nicchie specializzate basate su focus terapeutico, tipo di servizio o presenza regionale, in genere collaborando con cros più grandi su programmi complessi piuttosto che competere direttamente per contratti a servizio completo.
iqvia compete attraverso la sua piattaforma di dati e servizi clinici integrata che combina la gestione di prova con le capacità di prova del mondo reale. l'azienda gestisce il più grande database sanitario commerciale di france che copre i dati di prescrizione, i registri di scarico ospedaliero e le informazioni di reclamo, che utilizza per l'identificazione del paziente, la selezione del sito e le valutazioni di fattibilità. iqvia ha ampliato le sue operazioni cliniche francesi del 25% tra il 2023 e il 2025, aggiungendo specialisti di area terapeutica in oncologia, malattie rare e immunologia per sostenere contratti di partnership strategici con grandi sponsor di farmaci. l'azienda si differenzia sulle capacità di analisi, fornendo agli sponsor modelli di registrazione predittiva e analisi di efficacia comparativa che i cros più piccoli non possono replicare senza risorse di dati equivalenti.
labcorp compete attraverso l'integrazione verticale dei servizi di laboratorio e la gestione di prova clinica, consentendo all'azienda di offrire agli sponsor programmi unificati che combinano l'esecuzione di prova con i test di laboratorio centrali, l'analisi del biomarcatore e lo sviluppo diagnostico dei compagni. Questa integrazione conta in studi oncologici e malattie rare, dove la selezione dei pazienti con biomarcatore e le valutazioni farmacodinamiche richiedono un coordinamento tra siti clinici e laboratori specializzati. labcorp gestisce laboratori certificati glp in france che servono sia gli sponsor di sperimentazione clinica che i mercati diagnostici di routine, creando economie di scala che i cros puro-play non possono corrispondere. l'azienda si rivolge agli sponsor biotech che sviluppano candidati di medicina di precisione in cui i servizi integrati di laboratorio e clinici riducono il controllo del coordinamento e accelerano i tempi di sviluppo rispetto a coinvolgere fornitori separati per la gestione delle prove e i test di laboratorio.
recenti sviluppi
nel marzo 2026, iqvia ha annunciato una partnership strategica con un registro dei pazienti con malattia rara francese per fornire i dati di test genetici e di storia naturale per condizioni neurologiche ultra rare. la collaborazione mira ad accelerare l'identificazione e la valutazione della fattibilità del paziente per gli sponsor che sviluppano terapie per condizioni che interessano meno di 500 pazienti francesi. https://www.iqvia.com (iqvia)
nel febbraio 2026, labcorp ha ampliato le sue operazioni di laboratorio centrale french con nuove capacità di test biomarcatori per le prove di terapia cellulare e genica. la struttura elabora campioni farmacodinamici e saggi diagnostici dei compagni per gli sponsor di terapia avanzata che conducono studi clinici francesi. https://www.labcorp.com (labcorp)
quali intuizioni strategiche definiscono il futuro del mercato cro farmaceutico franco?
nei prossimi cinque-sette anni, il vantaggio competitivo nel mercato cro francese passerà dalle capacità operative di esecuzione alle piattaforme di dati e tecnologie che consentono nuove metodologie di prova. l'attuale mercato premia cros che possono iscrivere rapidamente i pazienti e fornire dati puliti sul programma, ma queste capacità stanno diventando commoditized come strumenti di cattura elettronica dei dati e di monitoraggio remoto standardizzati in tutto il settore. la prossima frontiera competitiva è l'integrazione di prove reali, l'esecuzione di prova decentrata e l'identificazione dei pazienti ai-powered, tutti i quali richiedono notevoli investimenti tecnologici e accordi di accesso ai dati che creano barriere all'ingresso per i concorrenti che non hanno scala.
il rischio che le proiezioni di mercato possano sottovalutare è tempi di accettazione normativa per nuove metodologie di prova. ansm ha pubblicato una guida sulle prove decentrate e le prove del mondo reale, ma la revisione regolamentare effettiva delle conclusioni che utilizzano questi approcci rimane limitata. se le autorità di regolamentazione si rivelano più conservatrici nella pratica che i documenti di orientamento suggeriscono, gli sponsor possono ritardare l'adozione di queste metodologie, che ridurrebbe la domanda di capacità cro in questi settori e favorire l'esecuzione di prova basata sul sito tradizionale in cui il precedente normativo è ben stabilito. questo beneficerebbe cros incumbent con forti reti di sito, mentre disvantage nuovi concorrenti che hanno investito pesantemente in piattaforme di prova decentrate.
l'opportunità che rimane sottoprezzo è post-omologazione reale servizi di prova che combinano fase iv gestione di prova con studi osservazionali utilizzando database di salute francese. I pagatori sempre più richiedono dati di efficacia del mondo reale per sostenere le decisioni di rimborso, e gli sponsor hanno bisogno di cros che possono progettare programmi integrati che soddisfano sia i requisiti di regolazione post-marketing e le esigenze di prova del pagamento. il segmento è attualmente piccolo, ma offre margini più alti del lavoro tradizionale di fase iv perché richiede capacità specializzate in economia sanitaria, epidemiologia e analisi di database che la maggior parte dei cros non mantengono. aziende che costruiscono queste capacità cattureranno la crescente domanda di sponsor per i programmi di generazione di prove che servono più stakeholder piuttosto che soddisfare semplicemente gli obblighi normativi.
Domande frequenti
Trova risposte rapide alle domande più comuni.
il mercato franco farmaceutico cro è previsto per raggiungere usd 2.358.7 milioni entro il 2033.
i segmenti chiave per il mercato dei cro farmaceutici franco sono di tipo (ricerca clinica, ricerca preclinica, servizi di laboratorio, altri); per applicazione (sviluppo della droga, studi clinici, studi tossicologici, gestione dei dati, altri); per l'utente finale (società farmaceutiche, biotecnologie, istituti di ricerca, altri); per fase (fase i, fase ii, fase ii, fase iv, altri).
i principali operatori del mercato farmaceutico franco sono iqvia, labcorp, syneos health, parexel, icon plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat.
l'attuale dimensione del mercato del cro farmaceutico franco è usd 1.295,8 milioni nel 2025.
il mercato cro farmaceutico franco è 7,82% dal 2026 al 2033.
Rapporti pubblicati di recente
-
Apr 2026
Mercato dei servizi bancari del sangue
servizi bancari del sangue del cavo dimensione del mercato, rapporto di condivisione e analisi per tipo di servizio (collezione, elaborazione, stoccaggio), per tipo di banca (banche private, banche pubbliche e banche ibride), per componente (membro del sangue e del cordone), per utente finale (ospedali, istituti di ricerca, aziende di biotecnologia, e altri) e geografia (nord america, europe, asia-pacific, medio oriente e africa, sud e centrale america 2021)
-
Apr 2026
Mercato dei processori ELISA
elisa processori dimensione del mercato, rapporto di condivisione e analisi per tipo (analizzatore di elisa di filtro ottico e analizzatori di elisa gratificazione ottica), per modalità (analizzatori di elisa automatizzati, e analizzatori di elisa semi-automatizzati), per applicazioni (immunologia, sviluppo del vaccino, monitoraggio della droga, e altri), per gli utenti finali (soci biotecnologie, aziende farmaceutiche, organizzazione del contratto di ricerca e laboratori diagnostici) e geografia
-
Apr 2026
Mercato dello scanner dello scorrevole del microscopio
microscopio slide scanner dimensione del mercato, rapporto di condivisione e analisi per tipo (microscopio portabile scanner diapositiva, e desktop microscopio scanner), per applicazione (ricerca biologica, medicina, veterinaria e altro) e geografia (nord america, europe, asia-pacifico, medio oriente e africa, sud e america centrale), 2021 - 2031
-
Apr 2026
Forno a microonde Cookware Market
microonde pentole dimensioni del mercato, rapporto di condivisione e analisi per tipo di materiale (plastica, vetro, ceramica, silicone e metallo), per applicazione (cooking, riscaldamento e defrosting), per utente finale (household, commerciale (ristoranti, hotel e caffè), e industria del servizio alimentare), per canale di vendita (online retail, offline retail (supermercati, ipermercati, negozi specializzati), e vendita diretta (imprese) e geografia media


