europe settore sanitario contratto di ricerca organizzazione mercato dimensioni e previsioni:
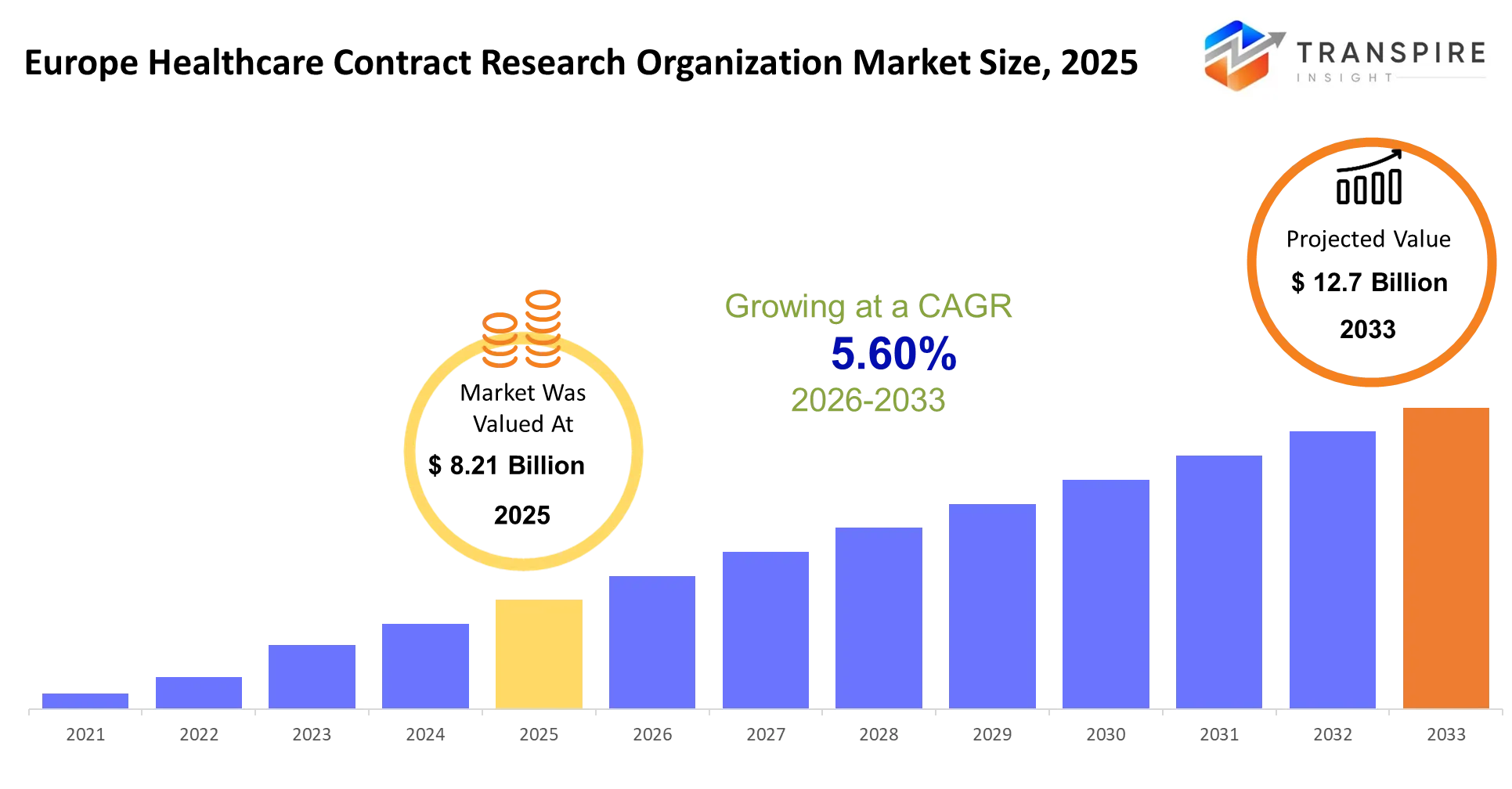
- europe settore sanitario contratto di ricerca organizzazione mercato dimensioni 2025: usd 8,21 miliardi
- europe settore sanitario contratto di ricerca organizzazione mercato dimensioni 2033: usd 12.7 miliardi
- europe settore sanitario contratto di ricerca organizzazione di mercato cagr: 5.60%
- segmenti di mercato dell'organizzazione della ricerca sui contratti sanitari europei: per tipo (servizi di ricerca clinici, servizi preclinici, servizi di laboratorio, altri), per applicazione (sviluppo della droga, studi clinici, test sui dispositivi medici, servizi normativi, altri), per end-user (società farmaceutiche, aziende di biotecnologie, società di dispositivi medici, istituti di ricerca, altri), per fase (fase ii, fase ii, fase ii, fase ii, fase i, fase iv, fase i, fase i, fase iv, altri)
per saperne di più su questo rapporto, scaricare gratuitamente il report del campione
Riassunto del mercato dell'organizzazione della ricerca sui contratti sanitari in Europa:
La dimensione del mercato dell'organizzazione per la ricerca sul contratto sanitario in Europa è stimata in 8,21 miliardi di USD nel 2025 e si prevede di raggiungere 12,7 miliardi entro il 2033, con una crescita del 5,60% dal 2026 al 2033. organizzazioni europee di ricerca di contratti sanitari funzionano come laboratori di sviluppo di droga outsourced che gestiscono tutti gli aspetti dell'esecuzione clinica di prova per i clienti farmaceutici e biotech. le organizzazioni permettono agli sponsor di condurre lo sviluppo terapeutico dal test di laboratorio al rilascio del mercato fornendo risorse operative essenziali e competenze specialistiche che mancano.
modelli di prova decentralizzati e ibridi che utilizzano strumenti di monitoraggio digitale e metodi di coinvolgimento dei pazienti remoti sono diventati l'approccio primario della ricerca negli ultimi tre a cinque anni. il turno consente ai team di ricerca di lavorare con più pazienti perché riduce la necessità di utilizzare specifiche strutture di ricerca. la pandemica covid-19 ha servito come catalizzatore principale perché ha richiesto le prove di continuare nonostante le restrizioni al movimento e ha portato ad una più rapida accettazione dei metodi virtuali da parte degli organismi di regolamentazione.
il crescente fabbisogno di soluzioni rapide e flessibili è emerso come il principale autista dietro sponsor che ora utilizzano servizi di outsourcing a prezzi più elevati. la combinazione di analisi dei dati e prove reali e capacità di prova adattativa ha permesso a cros di creare flussi di entrate scalabili dalle loro complessità operative.
approfondimenti chiave del mercato
- I paesi europei occidentali controllano il mercato dell'organizzazione europea della ricerca sui contratti sanitari perché detengono più del 65% della quota di mercato che la Germania, il Regno Unito e la Francia portano nel 2024.
- L'Europa orientale è la zona più in rapida espansione fino al 2030 a causa della sua capacità di condurre sperimentazioni convenienti e reclutare i partecipanti rapidamente e dei suoi progressi verso i requisiti normativi dell'Unione europea.
- il settore dei servizi di sperimentazione clinica porta il mercato con una quota del 70% perché i paesi europei scelgono di esternalizzare i loro studi di fase ii e iii.
- la seconda quota di mercato più grande del settore appartiene ai servizi preclinici che ricevono il sostegno delle aziende biotecnologiche che sviluppano nuovi prodotti e le loro attività di ricerca e sviluppo in espansione.
- il segmento della gestione dei dati e dei servizi di prova del mondo reale sperimenta una rapida crescita perché l'implementazione della prova digitale spinge l'espansione dal 2025 al 2030.
- il campo oncologia detiene la più grande quota di mercato delle applicazioni che ha raggiunto il 30% nel 2024 perché i ricercatori medici conducono studi di prova complessi e ricercatori del cancro sviluppano numerosi farmaci per il cancro.
- lo sviluppo della medicina personalizzata insieme al supporto normativo per le malattie rare crea le aree di trattamento medico più rapidamente in via di sviluppo che sviluppano terapie mirate.
- aziende farmaceutiche controllano circa il 60% del mercato perché collaborano con cros per ridurre le loro spese operative, mentre espedite il loro processo di sviluppo della droga.
- Le piccole e medie imprese biotecnologiche rappresentano il segmento di utenti più in rapido sviluppo che ora dipende da soluzioni complete di outsourcing di servizi per sostenere le loro esigenze di crescita.
Quali sono i principali driver, restrizioni e opportunità nel mercato dell'organizzazione del contratto sanitario europeo?
l'elemento principale che spinge la crescita nel mercato dell'organizzazione di ricerca del contratto sanitario europeo risulta da un aumento della outsourcing di complicato lavoro di sviluppo clinico che è sorto dall'aumento delle spese di ricerca e sviluppo che ora superano usd 2 miliardi per farmaco approvato. aziende farmaceutiche hanno bisogno di ridurre i tempi di sviluppo del prodotto, mentre si tratta di complicati requisiti normativi che esistono in vari paesi europei. le organizzazioni ora praticano più alti tassi di outsourcing perché i loro studi clinici di fine fase contengono le più difficili operazioni di esecuzione e le difficoltà di iscrizione dei pazienti. sponsor che spendono più soldi sulle spese di prova esterne creano contratti più preziosi che portano a rapporti di servizio estesi con cros.
il sistema normativo europeo rimane diviso tra diverse normative nazionali nonostante l'esistenza di normative ema che controllano le attività di ricerca. ogni nazione gestisce i propri sistemi separati per ottenere approvazioni etiche e gestire i dati dei pazienti e rafforzare la conformità alle strutture di ricerca. il modello operativo esistente per le organizzazioni di ricerca cliniche (cros) affronta le sfide perché hanno bisogno di mantenere le operazioni standardizzate che si traduce in tempi di preparazione di prova più lunghi e maggiori spese amministrative. il processo porta a ritardi di studio che rendono alcuni mercati meno attraente limitando così le opportunità di reddito e limitando la crescita dei modelli di ricerca a livello europeo.
il potenziale di crescita per gli studi clinici decentrati mostra una promessa significativa perché i sistemi sanitari digitali diventano più avanzati in paesi come la germania e la regione nordica. il monitoraggio remoto e le tecnologie di acquisizione dati esenti e indossabili rendono possibile che più pazienti partecipino a studi che portano a una più rapida registrazione di studio.
che cosa ha l'impatto dell'intelligenza artificiale è stato sul mercato dell'organizzazione di ricerca del contratto sanitario europeo?
Le organizzazioni europee di ricerca di contratti utilizzano ora l'intelligenza artificiale insieme a strumenti digitali avanzati per trasformare il loro processo di progettazione clinica attraverso l'esecuzione automatizzata di compiti operativi essenziali. I sistemi ai-powered ora utilizzano l'elaborazione del linguaggio naturale insieme all'automazione del processo robotico per eseguire il processo di identificazione del paziente e le valutazioni di fattibilità del sito e le attività di pulizia dei dati. il sistema stabilisce un processo di configurazione e monitoraggio di prova che richiede un lavoro meno manuale per raggiungere tra il 20% e il 20% di risparmio di tempo, producendo risultati di dati più accurati attraverso studi multi-paese. Gli strati di controllo digitale consentono alle organizzazioni di monitorare la conformità perché verificano continuamente i dati di prova contro i cambiamenti degli standard normativi.
i modelli di machine learning aggiungono capacità predittive che influiscono direttamente sulle prestazioni di prova. sponsor e cros utilizzano algoritmi per prevedere i tassi di reclutamento dei pazienti, prevedere i rischi di dropout e ottimizzare la selezione del sito in base a dataset storici e reali. il processo si traduce in una migliore efficienza di iscrizione che diminuisce ritardi costosi, con alcuni studi che riportano 15-25% cicli di reclutamento più veloci. ai supporta i progetti di prova adattativi simulando i cambiamenti del protocollo prima dell'implementazione, che migliora il processo decisionale in condizioni incerte.
Le tecnologie consentono alle organizzazioni di ottenere risultati operativi migliori attraverso tre principali vantaggi che includono tassi di successo di prova più elevati, meno modifiche del protocollo e riduzione delle spese totali di sviluppo. il processo affronta le sfide di implementazione perché gli ecosistemi di dati rimangono frammentati e i costi di integrazione rimangono elevati, soprattutto per unificare i sistemi clinici tradizionali in vari ambiti normativi europei.
tendenze chiave del mercato
- il campo delle sperimentazioni decentralizzate e ibride ha subito una rapida crescita dal 2020 perché più del 40% degli studi di ricerca europei ha adottato metodi di test remoti per continuare le loro operazioni durante i limiti di viaggio.
- l'industria farmaceutica ha aumentato le sue attività di outsourcing dal 45 per cento nel 2018 a più del 55 per cento nel 2024 che indica l'industria ora preferisce esternamente il suo lavoro di ricerca clinica a partner esterni.
- europe orientale è diventato la posizione più popolare per gli studi clinici dopo il 2021 perché i processi di reclutamento dei pazienti in questa regione hanno richiesto il 15-20 per cento meno tempo che nei mercati europei occidentali.
- il periodo dal 2019 al 2024 ha portato una maggiore complessità agli studi oncologici che hanno portato a organizzazioni di ricerca cliniche che necessitano di soluzioni complete di servizio per i loro test di biomarcatore e le esigenze di sviluppo di prova flessibili.
- Le aziende di biotecnologia che operano a scala media hanno iniziato a stabilire partnership strategiche con cros dopo il 2020, perché questo approccio ha permesso loro di ridurre la loro necessità di capacità operativa interna, accelerando le loro prime sperimentazioni umane.
- la pandemica covid-19 ha creato nuove regole regolamentari che hanno permesso alle agenzie di utilizzare il monitoraggio remoto e l'econsenso, cambiando così gli standard di conformità in tutta l'Europa.
- l'integrazione delle prove reali ha guadagnato la velocità dopo il 2022 come sponsor utilizzati al di fuori dei dati per sostenere le loro applicazioni di regolamentazione e lavoro di ricerca post-mercato.
- cros ha trasformato il proprio modello di business dall'essere fornitori di servizi per diventare partner di sviluppo strategico investendo in tecnologie per la salute digitale e capacità di rete del sito.
europe sanità contratto di ricerca organizzazione mercato segmentazione
per tipo
la categoria di servizi di ricerca clinica primaria mantiene la leadership di mercato perché le aziende esternalizzano le loro complesse operazioni di prova che richiedono competenze specializzate in particolare durante le prove di fine fase che coinvolgono la massima spesa e controllo normativo. I servizi preclinici mantengono una quota stabile perché le aziende biotecnologiche europee espandono le loro attività di ricerca in fase iniziale, mentre i servizi di laboratorio sperimentano una crescita continua a causa dei crescenti requisiti per le prove di biomarca e dei servizi diagnostici centralizzati. gli sponsor ora preferiscono soluzioni di servizio complete perché vedono i modelli di servizio integrati più efficaci che l'utilizzo di più partnership di fornitori separati.
cros che offrono servizi clinici combinati con l'analisi avanzata dei dati e le capacità di prova del mondo reale attualmente sperimentano la più alta domanda secondo le tendenze del mercato. il prossimo periodo di crescita richiederà ai fornitori di sviluppare pacchetti di strumenti digitali che possono combinare con i loro servizi esistenti per creare contratti più preziosi, mantenendo l'efficienza operativa in varie fasi di studi clinici.
per saperne di più su questo rapporto, scaricare gratuitamente il report del campione
di applicazione
gli studi clinici costituiscono la maggior parte della ricerca attraverso i loro finanziamenti in corso che supporta droga oleodotti di sviluppo e studi multinazionali basati su europe che hanno bisogno di esecuzione complessa. il settore dei servizi di sviluppo della droga mantiene la sua posizione perché i cluster di biotecnologia sperimentano un aumento dei finanziamenti dal capitale di rischio che supporta il loro lavoro di ricerca in fase iniziale. la regolazione del dispositivo medico eu richiede ora più procedure di conformità e test che ha portato ad una maggiore domanda di servizi di test del dispositivo medico.
sponsor ora cercano servizi normativi perché hanno bisogno di aiuto per navigare più processi di approvazione che esistono nelle loro operazioni aziendali. il campo della ricerca mostra crescente attenzione alla medicina di precisione e studi sulle malattie rare che richiedono metodi di prova clinici distinti e tecniche specifiche per la selezione dei partecipanti alla ricerca. Gli sviluppi futuri porteranno a cros e sponsor che lavorano insieme più da vicino attraverso la gestione adattativa dei requisiti normativi e test di prova che utilizza tecniche basate sui dati per processi di approvazione di prova più rapidi.
di utente finale
il mercato degli utenti finali supporta le aziende farmaceutiche perché i loro programmi di ricerca clinici e le esigenze in corso per ridurre al minimo le spese operative. Le aziende biotecnologiche rappresentano il gruppo in crescita più rapida, che dipende dall'outsourcing perché non hanno sufficienti capacità interne e necessitano di processi di sviluppo adattabili. le aziende di dispositivi medici mantengono la domanda continua a causa di requisiti di conformità più rigorosi, mentre gli istituti di ricerca avanzano la conoscenza attraverso i loro progetti di ricerca accademici e finanziati dal governo.
i diversi gruppi presentano modelli di coinvolgimento unici perché le aziende farmaceutiche preferiscono stabilire partnership permanenti mentre le aziende biotecnologiche devono sviluppare operazioni che possono espandersi rapidamente. la futura direzione di ricerca stabilirà connessioni più forti tra capacità cro e dimensione dell'organizzazione sponsor perché pacchetti di servizi personalizzati e accordi di condivisione del rischio determineranno la concorrenza di mercato e metodi di conservazione del cliente.
di fase
le tre fasi di prova stabiliscono fase iii come principale fonte di reddito per cros a causa delle sue dimensioni e costose operazioni e la sua funzione vitale per ottenere l'approvazione normativa. la crescente necessità di studi e ricerche di ottimizzazione delle dosi di prova-de-concetto consente studi di fase per mantenere la loro quota sostanziale di mercato. il numero di prove di fase i continua ad aumentare perché più aziende biotech creano nuovi prodotti e conducono i loro primi test umani. la domanda di servizi iv di fase aumenta perché le aziende devono condurre la sorveglianza post-marketing sotto nuove normative di monitoraggio della sicurezza.
i modelli di domanda mostrano che in seguito i test di fase hanno bisogno di servizi più complessi che portano alle aziende a outsourcing il loro lavoro e alla ricerca di competenze specialistiche. il futuro porterà nuovi progetti di prova adattativi insieme a metodi decentrati che cambieranno il modo in cui gli studi clinici distribuiscono le loro fasi mentre cercano modi più rapidi per completare tutte le fasi di test e migliorare le loro prestazioni operative.
Quali sono i casi chiave di utilizzo che guidano il mercato dell'organizzazione di ricerca del contratto sanitario europeo?
l'applicazione primaria dei centri di sperimentazione clinica sulla loro esecuzione perché le grandi aziende farmaceutiche operano studi multi-paese ii e iii secondo i requisiti normativi europei. il requisito più esigente deriva da questo caso di utilizzo perché coinvolge attività operative tra più giurisdizioni che includono il reclutamento del paziente e la gestione del sito e le esigenze di conformità.
l'azienda ha sviluppato le sue capacità per supportare i test di dispositivi medici in base alla normativa eu dispositivi medici e fornire servizi di consulenza normativa per le aziende biotech che entrano in processi di prima in-umani. Le piccole e medie imprese biotecnologiche si rivolgono ora a cros per due scopi, che includono la ricerca dei loro percorsi di approvazione e il raggiungimento di una crescita efficiente durante il loro processo di sviluppo del primo stadio.
i casi di utilizzo emergenti di studi decentralizzati comportano l'applicazione di strumenti di monitoraggio remoto, mentre gli studi di prove reali funzionano come metodi per la sorveglianza post-mercato. i modelli sono diventati più popolari perché i regolatori hanno iniziato ad accettare endpoint digitali, mentre gli sponsor ora perseguono un accesso più rapido ai dati sostanziali attraverso metodi di ricerca clinica avanzata.
report metriche | dettagli |
valore dimensione del mercato in 2025 | usd 8,21 miliardi |
valore dimensione del mercato in 2026 | usd 8.67 miliardi |
previsione delle entrate nel 2033 | usd 12.7 miliardi |
tasso di crescita | da 2026 a 2033 |
anno di base | 2025 |
dati storici | 2021 - 2024 |
periodo di previsione | 2026 - 2033 |
copertura report | previsione delle entrate, paesaggio competitivo, fattori di crescita e tendenze |
Ambito regionale | europe (germany, regno unito, france, italy, spagna e resto d'Europa) |
azienda chiave profilata | iqvia, labcorp, parexel, icona, syneos health, charles river, medpace, ppd, covance, wuxi apptec, pra health sciences, sgs, eurofins, envigo, clinipace |
campo di personalizzazione | personalizzazione del rapporto libero (paese, area regionale e segmento). avvalersi di opzioni di acquisto personalizzate per soddisfare le vostre esigenze di ricerca esatte. |
relazione segmentazione | per tipo (servizi di ricerca clinici, servizi preclinici, servizi di laboratorio, altri), per applicazione (sviluppo della droga, studi clinici, test di dispositivi medici, servizi normativi, altri), per utente finale (società farmaceutiche, aziende di biotecnologie, società di dispositivi medici, istituti di ricerca, altri), per fase (fase i, fase ii, fase ii, fase iv, altri) |
quali regioni stanno guidando la crescita del mercato dell'organizzazione di ricerca sul contratto sanitario europeo?
europe occidentale controlla il mercato dell'organizzazione di ricerca del contratto sanitario europe perché il suo sistema normativo opera attraverso l'agenzia di medicina europea e le sue strutture di ricerca clinica funzionano a livelli avanzati. i paesi di germania france e il regno unito mantenere vaste reti di siti di prova e ospedali accademici insieme a ricercatori qualificati. il sistema stabilito che comprende la sede farmaceutica e biotecnologia cluster e piattaforme sanitarie digitali mantiene la domanda continua di outsourcing. la combinazione di robusti sistemi di protezione dei dati e reti sanitarie avanzate consente alle organizzazioni di condurre complesse sperimentazioni cliniche internazionali che richiedono numerosi paesi di partecipare.
l'Europa settentrionale opera come una regione affidabile che sweden denmark e finland uso per priorizzare l'integrazione del registro di sistema del paziente e il controllo della qualità dei dati. Questa regione differisce dall'Europa occidentale attraverso il suo focus su studi più piccoli ma altamente efficienti supportati da database sanitari nazionali e sistemi digitali unificati. cros sperimenta condizioni operative stabili a causa della regolare conformità normativa e iniziative di sviluppo di ricerca sponsorizzate dal governo. il sistema mantiene la crescita attraverso l'accesso trasparente dei dati dei pazienti e l'alto coinvolgimento della sanità pubblica che consente lo sviluppo senza i requisiti operativi fondamentali di cui gli altri sistemi hanno bisogno.
L'Europa orientale dimostra il suo tasso di sviluppo più rapido attraverso i suoi recenti investimenti in infrastrutture cliniche insieme alla sua conformità agli standard normativi europei. i paesi di poland hangary e Romania hanno migliorato le capacità del sito e ridotto i tempi di approvazione dal 2020. Gli sponsor globali hanno scelto di lavorare in esecuzione di prova perché la combinazione di costi operativi inferiori e più veloce reclutamento dei pazienti porta loro guadagni di efficienza. l'attuale slancio crea più punti di ingresso per cros e investitori che vogliono costruire capacità, mentre catturano la nuova domanda di mercato tra il 2026 e il 2033.
chi sono i principali attori del mercato dell'organizzazione di ricerca del contratto sanitario europeo e come competono?
L'organizzazione europea della ricerca sui contratti sanitari sperimenta la concorrenza che esiste tra due opposte tendenze di mercato del consolidamento e specializzazione. i cros globali mantengono la loro leadership di mercato con le loro vaste operazioni e offerte complete di servizi e le loro relazioni consolidate con le aziende farmaceutiche, mentre le aziende di medie e nicchia utilizzano le loro conoscenze terapeutiche specifiche e competenze regionali per competere. le aziende ora competono attraverso servizi basati sulla tecnologia che forniscono risultati migliori rispetto ai loro precedenti metodi basati sui costi, perché l'integrazione dei dati e i sistemi di prova decentrati e i metodi di esecuzione rapida determinano la loro capacità di vincere i contratti. la piattaforma digitale e l'espansione completa dei servizi mantengono la quota di mercato per le aziende consolidate, mentre i nuovi arrivati interrompono i mercati che si concentrano sulle malattie rare e sulle sperimentazioni del primo stadio attraverso le loro operazioni flessibili e conoscenze specialistiche.
le piattaforme avanzate di analisi e dati reali sviluppate da iqvia forniscono agli sponsor gli strumenti di cui hanno bisogno per creare prove predittive adattative. organizzazioni che investono in approfondimenti ai-powered e sviluppano partnership con organizzazioni sanitarie migliorare la loro capacità di accedere ai dati, che porta a migliori risultati di prova. icon plc fornisce soluzioni complete di servizio che collegano lo sviluppo clinico all'intelligenza sanitaria, attraverso le sue acquisizioni multiple, per ottenere un migliore controllo sugli orari dei progetti e sulle spese operative. parexel aiuta gli sponsor a navigare i requisiti normativi europei attraverso i suoi servizi di consulenza specializzati e assistenza all'esecuzione.
l'organizzazione di sviluppo del farmaco di labcorp utilizza le sue strutture di laboratorio per collegare i test diagnostici con le operazioni di prova clinica, che consente una migliore progettazione di studi basati su biomarca e raggruppamento dei pazienti. syneos health fornisce un modello di business completo che collega i suoi servizi per lo sviluppo clinico con l'accesso al mercato, attraverso un unico sistema, che fornisce soluzioni di esecuzione di prova senza soluzione di continuità e di entrata di mercato.
elenco società
- Iqvia
- laboratorio
- Allegato
- icona icona
- syneos salute
- fiume charles
- Medpa
- pp.
- Covanza
- wuxi apptec
- pra scienze della salute
- #
- eurofins
- invigo
- Clinipace
notizie recenti sullo sviluppo
in ottobre 2025, termopescatore espande i servizi di sperimentazione clinica tramite l'integrazione di clario acquisizione: termo pescatore sta attivamente progredendo la sua acquisizione clario holdings, rafforzare la sua impronta di dati di prova clinica europea e servizi di analisi. clario si specializza nella cattura e nella gestione dei dati di prova clinica, l'infrastruttura principale utilizzata da cros in tutta Europa per le prove di fine fase. l'accordo dovrebbe chiudere all'inizio del 2026.
fonte: https://www.reuters.com
in aprile 2026, termopescatore per divest microbiologia business a astorg: termopescatore scientifico ha accettato di vendere la sua attività di microbiologia a società europea private equity Astorg in un accordo di 1.075 miliardi di dollari. l'unità supporta i flussi di lavoro di test clinici e farmaceutici, strettamente legati ai servizi di laboratorio cro-enabled in Europa. la mossa riflette il consolidamento continuo delle capacità di supporto clinico outsourced nella regione.
fonte: https://www.wsj.com
quali intuizioni strategiche definiscono il futuro del mercato delle organizzazioni di ricerca dei contratti sanitari in Europa?
Il mercato dell'organizzazione per la ricerca sui contratti sanitari in Europa sta seguendo uno spostamento strutturale verso sistemi basati sulla piattaforma che utilizzano l'infrastruttura digitale e i dati reali e l'esecuzione di prove decentrate per creare vantaggi competitivi. il driver fondamentale dietro questo movimento richiede alle organizzazioni di accorciare i loro tempi di sviluppo mentre sviluppano terapie complesse che richiedono grandi quantità di dati per creare trattamenti come la biologia e la medicina personalizzata. il mercato si muoverà verso la collaborazione strategica in quanto le organizzazioni sviluppano le loro capacità di servire come dati completi e partner di esecuzione che li aiuteranno a ottenere più finanziamenti da sponsor.
il pericolo nascosto della frammentazione dei dati insieme a diverse normative sull'uso dei dati del paziente crea un pericolo che i modelli di prova a na-driven lottano per operare in vari paesi. questa limitazione creerà ostacoli per gli sforzi internazionali di standardizzazione che ridurranno i benefici di efficienza che le organizzazioni si aspettano di raggiungere attraverso le loro iniziative di trasformazione digitale.
L'Europa orientale presenta un'opportunità emergente per l'espansione delle prove ibride perché la sua infrastruttura in via di sviluppo e il suo quadro normativo consentono un più facile reclutamento dei pazienti che può essere scalato. I partecipanti al mercato hanno bisogno di sviluppare piattaforme digitali che consentano l'interoperabilità del sistema insieme alla creazione di reti di siti regionali per raggiungere i loro obiettivi di mantenimento dell'accesso ai dati, garantendo al contempo la conformità normativa e la flessibilità operativa.
europe assistenza sanitaria contratto di ricerca organizzazione del mercato relazione segmentazione
per tipo
- servizi di ricerca clinica
- Servizi preclinici
- servizi di laboratorio
- altri
per applicazione
- sviluppo della droga
- studi clinici
- test del dispositivo medico
- servizi normativi
- altri
per utente finale
- Società farmaceutiche
- Imprese di biotecnologia
- società di dispositivi medici
- istituti di ricerca
- altri
per fase
- fase
- fase
- fase
- fase iv
- altri
Domande frequenti
Trova risposte rapide alle domande più comuni.
la dimensione approssimativa del mercato dell'organizzazione di ricerca sui contratti sanitari per il mercato sarà di 12,7 miliardi nel 2033.
i segmenti chiave del mercato dell'organizzazione di ricerca del contratto sanitario europeo sono di tipo (servizi di ricerca clinica, servizi preclinici, servizi di laboratorio, altri), per applicazione (sviluppo della droga, studi clinici, test di dispositivi medici, servizi normativi, altri), per utente finale (società farmaceutiche, aziende di biotecnologia, società di dispositivi medici, istituti di ricerca, altri), per fase (fase i, fase ii, fase ii, fase i, fase ii, fase iv, fase i).
i principali attori del mercato dell'organizzazione di ricerca del contratto sanitario europe sono iqvia, labcorp, parexel, icona, salute del sineos, fiume di charles, medpace, ppd, covance, wuxi apptec, pra health sciences, sgs, eurofins, envigo, clinipace.
l'attuale dimensione del mercato del mercato dell'organizzazione di ricerca del contratto sanitario europe è usd 8,21 miliardi nel 2025.
il mercato dell'organizzazione di ricerca del contratto sanitario europe è 5.60%.
- Iqvia
- laboratorio
- Allegato
- icona icona
- syneos salute
- fiume charles
- Medpa
- pp.
- Covanza
- wuxi apptec
- pra scienze della salute
- #
- eurofins
- invigo
- Clinipace
Rapporti pubblicati di recente
-
Apr 2026
Mercato dei servizi bancari del sangue
servizi bancari del sangue del cavo dimensione del mercato, rapporto di condivisione e analisi per tipo di servizio (collezione, elaborazione, stoccaggio), per tipo di banca (banche private, banche pubbliche e banche ibride), per componente (membro del sangue e del cordone), per utente finale (ospedali, istituti di ricerca, aziende di biotecnologia, e altri) e geografia (nord america, europe, asia-pacific, medio oriente e africa, sud e centrale america 2021)
-
Apr 2026
Mercato dei processori ELISA
elisa processori dimensione del mercato, rapporto di condivisione e analisi per tipo (analizzatore di elisa di filtro ottico e analizzatori di elisa gratificazione ottica), per modalità (analizzatori di elisa automatizzati, e analizzatori di elisa semi-automatizzati), per applicazioni (immunologia, sviluppo del vaccino, monitoraggio della droga, e altri), per gli utenti finali (soci biotecnologie, aziende farmaceutiche, organizzazione del contratto di ricerca e laboratori diagnostici) e geografia
-
Apr 2026
Mercato dello scanner dello scorrevole del microscopio
microscopio slide scanner dimensione del mercato, rapporto di condivisione e analisi per tipo (microscopio portabile scanner diapositiva, e desktop microscopio scanner), per applicazione (ricerca biologica, medicina, veterinaria e altro) e geografia (nord america, europe, asia-pacifico, medio oriente e africa, sud e america centrale), 2021 - 2031
-
Apr 2026
Forno a microonde Cookware Market
microonde pentole dimensioni del mercato, rapporto di condivisione e analisi per tipo di materiale (plastica, vetro, ceramica, silicone e metallo), per applicazione (cooking, riscaldamento e defrosting), per utente finale (household, commerciale (ristoranti, hotel e caffè), e industria del servizio alimentare), per canale di vendita (online retail, offline retail (supermercati, ipermercati, negozi specializzati), e vendita diretta (imprese) e geografia media


