taille du marché pharmaceutique et prévisions
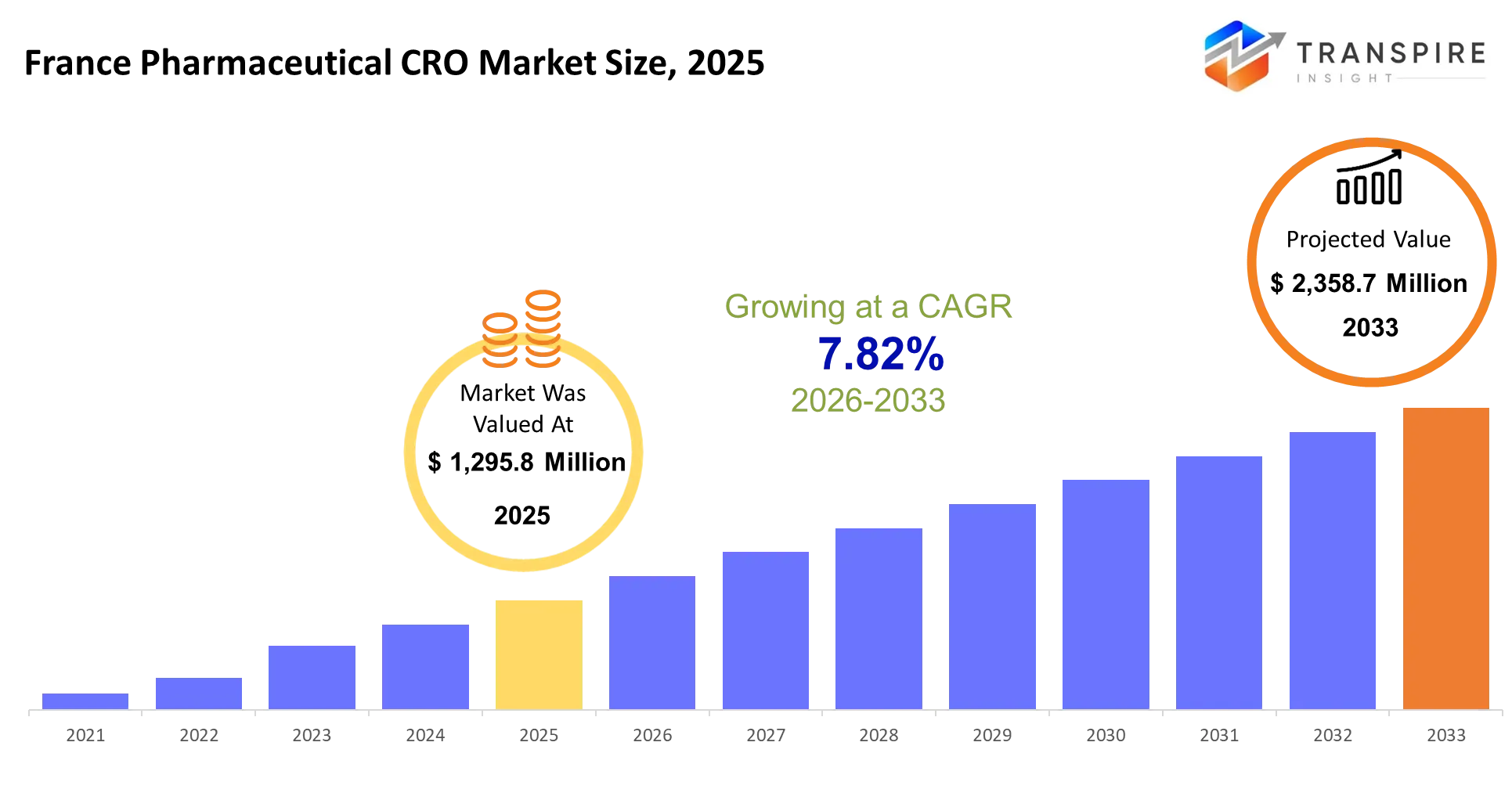
- taille du marché pharmaceutique france 2025: 1,295,8 millions
- taille du marché pharmaceutique 2033: 2,358,7 millions
- france pharmaceutique cro marché cagr: 7,82%
- segments du marché pharmaceutique france: par type (recherche clinique, recherche préclinique, services de laboratoire, autres); par application (développement de médicaments, essais cliniques, études toxicologiques, gestion des données, autres); par utilisateur final (entreprises pharmaceutiques, entreprises de biotechnologie, instituts de recherche, autres); par phase (phase i, phase ii, phase iii, phase iv, autres)
pour en savoir plus sur ce rapport, télécharger gratuitement l'exemple de rapport
synthèse du marché pharmaceutique
le marché du cro pharmaceutique france a été évalué à 1.295.8 millions en 2025. Il devrait atteindre 2,358,7 millions d'ici 2033, avec une croissance de 7,82 %. Les organismes de recherche sous-traités fournissent des services de recherche sous-traités aux entreprises pharmaceutiques et de biotechnologie, en traitant de tout, des études précliniques à la surveillance post-commercialisation. Les services de recherche clinique représentent 65% du marché français parce que les sponsors préfèrent transférer une gestion complexe des essais à des fournisseurs spécialisés plutôt que de maintenir des capacités internes dans plusieurs domaines thérapeutiques et juridictions réglementaires.
trois changements réglementaires entre 2020 et 2025 ont modifié le fonctionnement des cros français. d'abord, le règlement sur les essais cliniques eu introduisait des processus d'approbation harmonisés entre les États membres, ce qui réduisait la variabilité temporelle mais augmentait les exigences de documentation initiale. Deuxièmement, la plate-forme nationale de données sur la santé de la france a ouvert l'accès à des ensembles de données factuelles du monde réel que les sponsors peuvent maintenant relier aux résultats des essais cliniques, créant ainsi une demande de cros avec des capacités bioinformatiques. Troisièmement, Ansm a commencé à accepter des protocoles d'essai décentralisés qui permettent la surveillance des patients à distance, ce qui a déplacé la sélection des sites des chercheurs des réseaux hospitaliers traditionnels vers les fournisseurs de soins à domicile et les plateformes de télémédecine.
L'expansion actuelle du marché est motivée par des entreprises de biotechnologie qui externalisent les travaux de développement en fin d'étape qu'elles traitaient auparavant en interne. Les petites et moyennes entreprises de biotechnologie n'ont pas l'expertise en matière de réglementation pour naviguer dans les soumissions de ema et le réseau de sites pour exécuter efficacement les essais de phase iii multipays. Cros offre à ces entreprises l'accès à des relations de chercheurs établies, à des spécialistes du domaine thérapeutique et des affaires réglementaires sur une base de projet plutôt que de compte permanent. Ce modèle d'affaires permet aux commanditaires de la biotechnologie de conserver de l'argent liquide tout en accélérant les délais de développement, ce qui importe lorsque les cycles de financement des projets exigent des progrès cliniques démontrables tous les 18 à 24 mois.
clés du marché pharmaceutique france
- Les services de recherche clinique dominent le marché du cro pharmaceutique france avec une part de 65% en 2024, du fait de l'externalisation croissante de la gestion des essais de phase ii et de phase iii.
- Les services de recherche préclinique représentent 22 % du marché en 2024, soutenant les candidats au stade précoce qui nécessitent des tests toxicologiques et des études pharmacocinétiques.
- Les applications de développement de médicaments représentent 41,3 % de la demande de services cro en 2024, les entreprises pharmaceutiques externalisant le développement de la formulation et les tests de stabilité.
- Les demandes d'essais cliniques détiennent une part de marché de 38,7% en 2024, concentrée dans les domaines de l'oncologie, de l'immunologie et des maladies rares où le recrutement des patients est difficile.
- Les entreprises pharmaceutiques représentent 52,8 % de la demande des utilisateurs finals en 2024, et sous-traitent les activités de développement clinique autres que les activités de base pour concentrer les ressources internes sur la découverte et la commercialisation.
- Les entreprises de biotechnologie représentent 31,4 % du marché en 2024 et représentent le segment de l'utilisateur final qui connaît la croissance la plus rapide, passant de 9,1 % à 2033.
- Les essais de phase iii génèrent 43,2 % des revenus de la recherche clinique en 2024, ce qui nécessite de grandes populations de patients et des périodes de surveillance prolongées qui favorisent les cros à service complet.
- Les essais de phase ii représentent 28,6 % des revenus en 2024, la demande croissante de conceptions d'essais adaptatifs nécessitant des capacités spécialisées en matière de statistique et de gestion des données.
- iqvia détient environ 15 à 18 % du marché français des cro en 2025, exploitant ses services intégrés d'analyse de données et d'essais cliniques dans plusieurs domaines thérapeutiques.
- Labcorp a élargi ses activités de développement clinique français de 20 % en 2024, ajoutant des sites de chercheurs et des spécialistes du domaine thérapeutique pour répondre à la demande croissante en biotechnologie.
Quels sont les principaux moteurs, contraintes et opportunités sur le marché des cro pharmaceutiques de la france?
Le principal moteur de croissance est que les entreprises pharmaceutiques passent de l'externalisation sélective à des partenariats stratégiques où les cros gèrent des programmes de développement entiers plutôt que des études individuelles. Les grandes firmes pharmaceutiques attribuent maintenant des contrats pluriannuels couvrant des travaux précliniques au cours de la phase III pour des domaines thérapeutiques spécifiques, ce qui leur permet d'investir dans des capacités spécialisées comme les registres des patients atteints de maladies rares ou les plateformes de biomarqueurs oncologiques. iqvia, syneos health et parexel ont tous structuré leurs opérations françaises autour de ces partenariats stratégiques, consacrant des équipes à des comptes sponsors spécifiques plutôt qu'à des prestataires de services transactionnels. l'impact financier est important: les contrats de partenariat stratégique s'échelonnent généralement de trois à cinq ans et couvrent des portefeuilles de développement d'une valeur de centaines de millions d'euros, par rapport aux contrats d'études uniques d'une durée de 18 à 36 mois.
la restriction la plus importante est les contraintes de capacité du site de l'enquêteur dans les domaines thérapeutiques à forte demande. Les centres d'oncologie et les spécialistes en immunologie sont sursouscrits aux protocoles d'essai, ce qui crée des goulots d'étranglement pour le recrutement des patients qui retardent les délais d'étude indépendamment de l'efficacité avec laquelle le cro gère d'autres aspects de l'exécution d'essai. Cros ne peut pas simplement ouvrir de nouveaux sites pour résoudre ce problème parce que les chercheurs qualifiés ont besoin d'années de formation et de certification réglementaire. la contrainte est particulièrement aiguë dans les essais de maladies rares où la france n'a que cinq à dix centres avec des populations de patients pertinentes, et ces centres sont déjà engagés dans de multiples protocoles concurrents. Cela oblige les cros à prolonger les délais de recrutement ou à s'étendre à des sites de chercheurs moins expérimentés, ce qui augmente les coûts et les risques pour la qualité des études.
l'occasion la plus claire réside dans les services de données probantes du monde réel qui relient les données des essais cliniques à la base de données nationale sur la santé de la france. ansm accepte maintenant les preuves réelles pour appuyer les présentations réglementaires pour certaines indications, et les promoteurs ont besoin de cros qui peuvent concevoir des études hybrides combinant la méthodologie traditionnelle d'essais contrôlés randomisés avec les données d'observation des dossiers de santé électroniques. Cela nécessite des capacités que la plupart des cros ne possèdent pas actuellement : les data savants qui comprennent l'analyse des soins de santé, les spécialistes de la réglementation qui savent structurer les présentations de preuves dans le monde réel et les relations établies avec les autorités françaises de données sur la santé. Les entreprises qui construisent ces capacités capteront des travaux à forte marge qui ne peuvent être facilement reproduits par des concurrents qui n'ont pas l'infrastructure technique et l'expertise réglementaire nécessaires pour exécuter ces études hybrides.
Quel a été l'impact de l'intelligence artificielle sur le marché des cro pharmaceutiques de France ?
Les systèmes d'identification des patients dotés de moyens d'action sont maintenant utilisés pour vérifier les dossiers de santé électroniques afin de trouver des candidats qui répondent à des critères précis d'inclusion dans les essais, ce qui accélère les délais de recrutement en identifiant les patients admissibles avant que les sites n'examinent manuellement les tableaux. iqvia et labcorp ont déployé des modèles d'apprentissage automatique dans les systèmes de santé français qui identifient les patients à partir de codes de diagnostic, de valeurs de laboratoire, d'histoires de médicaments et d'autres marqueurs cliniques. Ces systèmes ont réduit le temps médian de dépistage de semaines à jours dans les sites dotés de dossiers de santé électroniques intégrés, bien que l'adoption reste limitée aux grands réseaux hospitaliers dotés de données numérisées sur les patients. l'avantage opérationnel est le plus visible dans les essais sur des maladies rares où l'examen du graphique manuel a nécessité des mois de temps pour identifier même une poignée de patients admissibles.
Le traitement du langage naturel automatise la surveillance de l'innocuité en extrayant les événements indésirables des notes cliniques, des rapports de laboratoire et des journaux des patients sans exiger la saisie manuelle des données par les coordonnateurs de site. syneos health et icon ont mis en place des systèmes nlp qui analysent en permanence la documentation d'essai pour détecter les signaux de sécurité, signalant d'éventuels événements indésirables graves qui nécessitent un rapport immédiat aux autorités réglementaires. cette automatisation a réduit le temps médian de déclaration des événements indésirables de 48 à 72 heures à moins de 24 heures sur les sites utilisant la technologie, ce qui importe lorsque les exigences réglementaires exigent la déclaration des événements indésirables graves dans les 24 heures suivant la sensibilisation des chercheurs. la limite est que l'exactitude des nlp dépend de la qualité de la documentation, et les notes cliniques françaises comprennent souvent des raccourcis médicaux et une terminologie non normalisée qui réduisent la fiabilité automatisée de l'extraction.
Le principal obstacle à une adoption plus large est la fragmentation des données entre les prestataires de soins de santé français. les dossiers des patients restent siloed au sein des systèmes hospitaliers individuels, des réseaux régionaux de santé et des pratiques privées, ce qui empêche les cros de former des modèles d'ai sur des ensembles de données complets qui reflètent les populations de patients du monde réel. En outre, les réglementations françaises en matière de protection des données exigent le consentement explicite du patient pour l'utilisation secondaire des données de santé dans les contextes de recherche, ce qui ajoute des frais généraux de conformité que beaucoup de cros trouvent prohibitifs pour les projets de développement. Cela crée un paradoxe où les applications les plus précieuses nécessitent de grands ensembles de données diversifiés que les cadres réglementaires français rendent difficiles à assembler légalement.
principales tendances du marché
- Les promoteurs pharmaceutiques sont passés de l'achat de services transactionnels à des partenariats stratégiques pluriannuels entre 2022 et 2024, regroupant les relations entre cinq ou six fournisseurs à deux ou trois fournisseurs privilégiés.
- L'adoption décentralisée des essais s'est accélérée en 2023 lorsque l'ansm a publié des directives acceptant la surveillance à distance des patients et les visites à domicile comme solutions de rechange valables aux évaluations basées sur le site.
- Les entreprises de biotechnologie ont augmenté leur externalisation, passant de 60 % en moyenne des dépenses de développement en 2021 à plus de 75 % en 2024, sous l'effet de la pression exercée sur le capital-risque pour minimiser les coûts fixes.
- iqvia et syneos santé ont élargi leur domaine thérapeutique français de 25-30% entre 2023 et 2025, embauche d'oncologie et d'experts en maladies rares pour soutenir les contrats de partenariat stratégique.
- En 2024, les services de données probantes du monde réel sont apparus comme une offre distincte, les cros créant des équipes dédiées à la conception d'études hybrides combinant des données expérimentales et des dossiers de santé d'observation.
- Le délai de recrutement des patients pour les essais en oncologie est passé de 12 mois à 16-18 mois entre 2022 et 2024 en raison des contraintes de capacité du site de l'investigateur et des protocoles concurrents.
- Les cros chinois sont entrés sur le marché français en 2024, offrant des services de phase I et de phase II précoce à 20-25 % de moins que les prix historiques pour établir des opérations européennes.
- Les services de gestion des données ont connu une croissance plus rapide que la surveillance clinique entre 2023 et 2025, ce qui reflète la demande accrue des promoteurs en matière d'analyse avancée et de visualisation des données en temps réel au cours des essais.
segmentation du marché pharmaceutique
par type
Les services de recherche clinique dominent le marché français des cro à 65% du chiffre d'affaires total. ce segment couvre le recrutement des patients, la surveillance du site, la collecte de données et l'aide à la présentation réglementaire pour les essais cliniques de phase I à la phase IV. la dominance reflète un changement structurel où les sponsors pharmaceutiques et biotechnologiques externalisent la gestion des essais vers les cros plutôt que de maintenir des équipes internes d'opérations cliniques. Les cros à service complet comme iqvia, labcorp et syneos health agissent comme bras de développement clinique du promoteur, gérant les relations des chercheurs, les interactions réglementaires et la surveillance de la qualité des données dans le cadre de multiples essais concomitants. la proposition de valeur est le transfert de risque: les sponsors paient les cros pour fournir les patients inscrits et des données propres à l'horaire, tandis que les cro absorbent la complexité opérationnelle et la variabilité temporelle.
Les services de recherche préclinique représentent 22 % du marché, ce qui englobe les études toxicologiques, l'analyse pharmacocinétique et le développement de formulations avant les essais chez l'humain. Ce segment dessert les entreprises de biotechnologie en phase initiale et les équipes de découverte pharmaceutique qui ont besoin de capacités de laboratoire spécialisées sans construire d'installations dédiées. Les services précliniques français sont dominés par les rivières charles, les corvées et les eurofins grâce à la propriété de laboratoires certifiés glp équipés pour des études toxicologiques réglementaires. le segment est techniquement exigeant parce que les études précliniques doivent respecter des normes réglementaires strictes pour la qualité des données et la reproductibilité, ce qui nécessite des méthodes analytiques validées et expérimentées laboratoire scientifiques. les marges sont plus élevées que la recherche clinique parce que les coûts de changement sont importants une fois qu'un promoteur qualifie un laboratoire particulier pour un programme de développement.
Les services de laboratoire et les autres offres spécialisées représentent ensemble 13 % du marché. Cela comprend les tests bioanalytiques, les services centraux de laboratoire pour les essais cliniques et les capacités de niche comme les tests d'instruments médicaux ou la validation numérique de la santé. le segment a augmenté plus rapidement que la recherche clinique fondamentale entre 2023 et 2025 parce que les promoteurs ont de plus en plus besoin de services intégrés qui combinent la gestion des essais cliniques et l'analyse de laboratoire spécialisée. Par exemple, les essais oncologiques ont souvent besoin d'un diagnostic complémentaire médicament les tests, qui exigent des cros qui peuvent coordonner la validation des biomarqueurs, la collecte d'échantillons cliniques et le développement des tests diagnostiques comme un programme unifié. Les entreprises qui offrent ces services intégrés perçoivent des revenus par projet plus élevés que celles qui ne fournissent que la gestion des essais cliniques.
pour en savoir plus sur ce rapport, télécharger gratuitement l'exemple de rapport
par demande
Les applications de mise au point de médicaments représentent 41,3 % de la demande du marché, ce qui englobe le développement de la formulation, les essais de stabilité, le développement de méthodes d'analyse et les services de soutien à la fabrication. Les entreprises pharmaceutiques sous-traitent ces activités à des entreprises lorsque les fonctions de développement interne manquent de capacités ou d'expertise spécialisée pour résoudre des problèmes particuliers de formulation. Par exemple, l'élaboration de formulations stables pour les produits biologiques nécessite un équipement et une expertise spécialisés que la plupart des promoteurs ne maintiennent pas à l'interne. Les partenaires comme Catalent, Patheon et lonza fournissent ces capacités sur une base contractuelle, permettant aux sponsors de faire avancer les candidats par le développement sans investissement en capital dans les laboratoires de formulation. l'application est une augmentation de marge parce que le travail de développement de la formulation est techniquement complexe et exige des scientifiques expérimentés qui commandent des taux de facturation majorés.
Les demandes d'essais cliniques représentent 38,7% de la demande, plus particulièrement en ce qui a trait à l'inscription des patients, à la gestion du site et aux services d'exécution des essais plutôt qu'à un soutien plus large au développement. ce segment diffère des services de recherche clinique en ce sens qu'il ne saisit que la composante exécution des essais, à l'exclusion de la stratégie réglementaire, de l'analyse des données et des activités post-essai. l'application a augmenté entre 2022 et 2024 à mesure que les entreprises de biotechnologie recherchaient des cros qui pourraient gérer le recrutement des patients et la surveillance du site tout en conservant d'autres activités de développement à l'interne. Ce dégroupage a permis aux promoteurs d'externaliser les aspects du développement clinique les plus complexes sur le plan opérationnel et qui tiennent compte des délais, tout en préservant le contrôle des décisions stratégiques comme la sélection des critères et la conception des essais.
Les études toxicologiques, la gestion des données et d'autres applications représentent 20 % du marché. Les études toxicologiques sont obligatoires pour les présentations réglementaires et exigent des installations certifiées glp que la plupart des promoteurs ne fonctionnent pas à l'interne. Les services de gestion des données se sont développés rapidement à mesure que les essais génèrent des volumes croissants de données électroniques provenant de portables, de dispositifs de surveillance à distance et de résultats déclarés par les patients qui nécessitent des plates-formes de bases de données spécialisées et des capacités d'analyse statistique. Les entreprises qui ont investi dans les plates-formes de données en nuage et l'analyse en temps réel entre 2020 et 2025 ont enregistré une demande croissante de sponsors pour une surveillance d'essai transparente et des conceptions d'essais adaptatifs qui nécessitent une analyse continue des données plutôt que des bases de données verrouillées traditionnelles examinées uniquement à la fin de l'étude.
par utilisateur final
Les sociétés pharmaceutiques représentent 52,8 % de la demande en france. Les grandes firmes pharmaceutiques sous-traitent des programmes de développement spécifiques où la capacité interne est limitée ou où l'expertise thérapeutique est insuffisante. Par exemple, une entreprise qui possède de solides capacités en oncologie pourrait externaliser le développement de maladies rares vers les cros avec des registres de patients établis et des réseaux de chercheurs dans ces indications. la décision d'externalisation est économiquement dictée: le maintien d'opérations cliniques internes dans des zones thérapeutiques où l'entreprise n'effectue qu'un ou deux essais par an est prohibitif par rapport à la participation de cros sur une base de projet. Cela crée une demande stable de cros dans les domaines thérapeutiques où l'intérêt du sponsor est soutenu, mais les portefeuilles individuels des entreprises sont limités.
Les entreprises de biotechnologie représentent 31,4 % du marché et représentent le segment qui connaît la croissance la plus rapide, avec 9,1 % de cagr jusqu'en 2033. Ces entreprises manquent généralement de capacités de développement clinique interne et externalisent la majorité des travaux de développement des études précliniques jusqu'aux essais de phase iii. le moteur de la croissance est la dynamique du financement du capital-risque: les entreprises de biotechnologie sont censées démontrer rapidement des progrès cliniques tout en minimisant la consommation d'argent, ce qui rend l'externalisation vers des entreprises plus attrayantes sur le plan financier que la création de capacités internes qui nécessitent un décompte fixe. Les promoteurs de la biotechnologie disposent d'une capacité souple qui tient compte des besoins des programmes, ne facture que pour les projets actifs plutôt que d'exiger des paiements continus ou du personnel rémunéré.
Les instituts de recherche et les autres utilisateurs finals contribuent à 15,8 % de la demande. Les centres médicaux universitaires et les organismes de recherche gouvernementaux s'engagent pour des essais et des études de santé publique initiés par des chercheurs qui nécessitent la collecte et la surveillance de données de niveau réglementaire. Ces clients utilisent généralement des subventions avec des budgets fixes et des échéanciers précis, ce qui oblige les cros à fournir des services dans des limites de coûts rigides. le segment offre des marges plus faibles que les travaux pharmaceutiques commerciaux, mais permet à cros d'accéder à de nouvelles approches thérapeutiques et à des populations de patients atteints de maladies rares qui se traduisent par la suite par des possibilités de développement commercial lorsque les découvertes universitaires se tournent vers l'approbation réglementaire et la commercialisation.
par phase
Les essais de phase iii génèrent 43,2 % des revenus de la recherche clinique en raison de leur nombre important de patients, de périodes de surveillance prolongées et d'exigences réglementaires complexes. Un essai d'oncologie type de phase iii en France pourrait inscrire 300 à 500 patients sur 25 à 40 sites de recherche sur une période de trois à quatre ans, ce qui nécessiterait la surveillance du site, la gestion des données, la déclaration de sécurité et la coordination réglementaire tout au long de la période d'étude. La gestion de cette complexité opérationnelle permet aux promoteurs de se concentrer sur les décisions stratégiques concernant la conception des essais et les présentations réglementaires. la concentration des revenus dans la phase iii reflète à la fois le coût direct de l'exécution d'essais à grande échelle et les sponsors de primes de risque paient pour les cros afin de respecter des délais d'inscription agressifs qui déterminent les dates de lancement du produit.
Les essais de phase ii contribuent à 28,6 % des revenus, axés sur les études de détermination de la dose et les évaluations initiales de l'efficacité chez les populations de patients plus petites. Ces essais utilisent de plus en plus des conceptions adaptatives qui modifient les critères d'inscription ou les calendriers de dosage en fonction des résultats provisoires, ce qui exige des cros dotés de solides capacités de gestion des statistiques et des données. la complexité technique des essais adaptatifs crée des obstacles à l'entrée pour les petits cros qui manquent d'expertise spécialisée, ce qui permet aux plus grands fournisseurs de services complets de commander des prix élevés. Le travail de la phase II est stratégiquement important pour les cros parce que les commanditaires qui terminent la phase II avec succès continuent généralement avec la même cro jusqu'à la phase iii, créant des pipelines de revenus pluriannuels à partir de l'engagement initial.
La phase I, la phase IV et les autres phases d'essai représentent ensemble 28,2 % des recettes. Les essais de phase i sont relativement petits mais exigeants sur le plan technique, nécessitant des installations spécialisées pour les études sur la sécurité du premier patient et la surveillance intensive des patients. Les études post-commercialisation de phase IV sont en croissance, car les organismes de réglementation ont de plus en plus besoin de données réelles pour compléter les données cliniques pré-approbation. Les partenaires qui offrent à la fois la gestion des essais de phase IV et les capacités de données probantes du monde réel combinant les données d'essais et les dossiers de santé d'observation saisissent la demande croissante des promoteurs de programmes intégrés de surveillance post-commercialisation qui satisfont aux exigences réglementaires tout en produisant des preuves pour les négociations sur le remboursement des payeurs et l'élaboration de lignes directrices cliniques.
Quels sont les principaux cas d'utilisation qui sont à l'origine du marché du cro pharmaceutique france?
l'application principale est la gestion d'essais de phase iii à service complet pour les entreprises de biotechnologie qui n'ont pas de capacités internes d'exploitation clinique. Ces commanditaires engagent les cros à traiter tous les aspects de l'exécution d'essai à partir de la sélection du site, en passant par la fermeture de la base de données, la présentation réglementaire et la surveillance de la sécurité après l'approbation. un engagement typique pourrait comprendre une indication de maladie rare où le promoteur de la biotechnologie a terminé les études de phase ii de preuve de concept et a besoin d'un cro pour exécuter le programme pivot de phase iii requis pour l'approbation de l'EMA. le cro fournit des réseaux de sites de chercheurs, de l'expertise réglementaire, des stratégies de recrutement des patients et une infrastructure de gestion des données clé en main, permettant à l'entreprise de biotechnologie de progresser vers la commercialisation sans construire un effectif permanent d'opérations cliniques.
La demande adjacente provient de grandes sociétés pharmaceutiques qui sous-traitent des programmes de développement de zones thérapeutiques spécifiques. Par exemple, une entreprise ayant une expertise en immunologie limitée pourrait engager un cro pour gérer tout le développement clinique d'un actif en immunologie acquis, en tirant parti des relations établies du cro avec les chercheurs en rhumatologie et dermatologie française. ces partenariats stratégiques couvrent généralement plusieurs essais sur plusieurs années, fournissant à la cro des revenus prévisibles tout en donnant au promoteur l'accès à une expertise thérapeutique sans expansion permanente du personnel. la logique commerciale est la spécialisation: les cros qui se concentrent sur des domaines thérapeutiques spécifiques développent des relations de chercheurs profondes et une expérience de conception de protocole que les équipes de développement interne généralistes ne peuvent pas reproduire.
Les nouveaux cas d'utilisation sont centrés sur les modèles d'essais hybrides combinant des essais contrôlés randomisés traditionnels avec des preuves du monde réel provenant de bases de données de santé françaises. Les promoteurs engagent les cros à concevoir des études où le bras témoin utilise des patients appariés provenant de dossiers de santé électroniques plutôt que d'inscrire une cohorte de placebo distincte, ce qui réduit les coûts des essais et accélère les délais d'inscription. iqvia et la santé synéos ont créé des équipes dédiées à l'exécution de ces études hybrides, exigeant des chercheurs en données, des épidémiologistes et des spécialistes de la réglementation qui comprennent à la fois la méthodologie des essais cliniques et les normes factuelles. la demande est techniquement exigeante, mais offre aux promoteurs des économies substantielles de coûts, avec certaines conceptions hybrides réduisant les coûts de phase iii de 30 à 40% par rapport aux essais traditionnels entièrement inscrits.
les paramètres du rapport | détails |
Valeur de la taille du marché en 2025 | 1 295,8 millions d'euros |
valeur de la taille du marché en 2026 | 1 392,6 millions d'euros |
recettes prévues en 2033 | 2 358,7 millions d'euros |
taux de croissance | de 7,82 % entre 2026 et 2033 |
année de référence | 2025 |
données historiques | 2021 – 2024 |
période de prévision | 2026 – 2033 |
couverture du rapport | prévisions de recettes, paysage concurrentiel, facteurs de croissance et tendances |
portée régionale | france |
les principales entreprises | iqvia, labcorp, syneos health, parexel, icon plc, charles River, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat |
personnalisation | personnalisation gratuite du rapport (étendue régionale et segmentaire). utilisez des options d'achat personnalisées pour répondre à vos besoins de recherche exacts. |
segmentation du rapport | par type (recherche clinique, recherche préclinique, services de laboratoire, autres); par application (développement de médicaments, essais cliniques, études toxicologiques, gestion des données, autres); par utilisateur final (entreprises pharmaceutiques, entreprises de biotechnologie, instituts de recherche, autres); par phase (phase i, phase ii, phase iii, phase iv, autres) |
Qu'est-ce qui stimule la croissance sur le marché des cro pharmaceutiques de la france?
France offre trois avantages structurels que d'autres marchés européens ne peuvent pas reproduire à une échelle équivalente. Premièrement, le pays exploite un système de soins de santé centralisé avec des dossiers de santé électroniques complets couvrant plus de 65 millions de citoyens, fournissant à cros des capacités d'identification des patients et un accès aux données réelles que les systèmes de soins de santé fragmentés ne peuvent pas égaler. Deuxièmement, la france maintient des concentrations denses de sites de chercheurs spécialisés à Paris, au lyon et à la marseille où les centres médicaux universitaires, les hôpitaux d'enseignement et les instituts de recherche se côtoient à proximité géographique, ce qui simplifie la logistique des essais et réduit les coûts de surveillance par rapport aux réseaux de sites géographiquement dispersés. Troisièmement, Ansm a établi des délais d'examen réglementaire prévisibles et des directives claires sur les nouvelles méthodes d'essai, comme des protocoles décentralisés et des données factuelles, ce qui réduit l'incertitude pour les promoteurs qui planifient des programmes de développement pluriannuels.
la dynamique concurrentielle en france diffère des autres marchés européens parce que les exigences linguistiques et réglementaires créent des barrières naturelles à l'entrée pour les non-eu cros. Les protocoles d'essai, les documents de consentement éclairé et les soumissions réglementaires doivent être en français, ce qui nécessite un personnel local spécialisé plutôt que des équipes européennes centralisées opérant en anglais. En outre, la réglementation française en matière de protection des données impose des exigences spécifiques en matière de traitement des données de santé qui diffèrent des dispositions générales en matière de gdpr, obligeant les cros à maintenir des programmes de conformité spécifiques à la france. ces barrières protègent les acteurs établis comme iqvia, labcorp et syneos santé qui ont opéré en france pendant des décennies et investi dans les infrastructures locales, tout en créant des coûts d'entrée plus élevés pour les nouveaux concurrents qui tentent d'établir des opérations françaises.
Le segment de la demande qui connaît la croissance la plus rapide est celui des essais sur les maladies rares où la base de données nationale sur la santé de la france permet une identification rapide des patients pour les indications ultra-rares. dans des conditions touchant moins de 1 000 patients français, le recrutement traditionnel sur place peut prendre des années parce que les enquêteurs doivent vérifier manuellement les dossiers médicaux pour identifier les candidats admissibles. Les entreprises qui ont conclu des accords d'accès aux données avec les autorités sanitaires françaises peuvent contrôler l'ensemble de la population nationale de patients par voie électronique, en identifiant les patients éligibles en semaines plutôt qu'en mois. cette capacité a fait de la france un endroit privilégié pour les essais européens sur les maladies rares, les sponsors choisissant de plus en plus les sites français comme pays de tête pour les études multinationales dans des indications ultra-rares où la vitesse d'identification des patients détermine le calendrier global du programme.
qui sont les acteurs clés du marché des cro pharmaceutiques france et comment sont-ils compétitifs?
le marché français des cro fonctionne comme une structure à deux niveaux. iqvia, labcorp, syneos health, parexel et icon détiennent collectivement une part de marché d'environ 55 à 60 % et se font concurrence en tant que fournisseurs de services complets offrant des capacités intégrées de la phase préclinique à la phase iv. ces entreprises font concurrence à l'expertise thérapeutique, aux réseaux de sites de chercheurs et aux plateformes technologiques qui offrent aux commanditaires une visibilité d'essai en temps réel. Les cros moyens et plus petits occupent des créneaux spécialisés basés sur l'orientation thérapeutique, le type de service ou la présence régionale, généralement en partenariat avec des cros plus grands sur des programmes complexes plutôt que de concurrencer directement pour des contrats de service complet.
iqvia est en concurrence avec sa plateforme intégrée de données et de services cliniques qui combine la gestion d'essais et les capacités factuelles du monde réel. l'entreprise exploite la plus grande base de données sur la santé commerciale de la france, qui couvre les données sur les ordonnances, les dossiers de sortie d'hôpital et les renseignements sur les demandes, qu'elle utilise pour l'identification du patient, la sélection du site et les évaluations de faisabilité. iqvia a élargi ses opérations cliniques françaises de 25% entre 2023 et 2025, ajoutant des spécialistes du domaine thérapeutique en oncologie, maladies rares et immunologie pour soutenir des contrats de partenariat stratégique avec de grands sponsors pharmaceutiques. l'entreprise différencie sur les capacités d'analyse, fournissant aux sponsors des modèles d'inscription prédictifs et des analyses d'efficacité comparative que les petits cros ne peuvent pas reproduire sans des actifs de données équivalents.
Labcorp rivalise avec l'intégration verticale des services de laboratoire et la gestion des essais cliniques, ce qui permet à l'entreprise d'offrir des programmes unifiés qui combinent l'exécution des essais avec les tests de laboratoire centraux, l'analyse des biomarqueurs et le développement de diagnostics complémentaires. Cette intégration est importante dans les essais en oncologie et en maladies rares où la sélection des patients et les évaluations pharmacodynamiques par les biomarqueurs nécessitent une coordination entre les sites cliniques et les laboratoires spécialisés. Labcorp exploite des laboratoires certifiés glp en France qui servent à la fois les promoteurs d'essais cliniques et les marchés de diagnostic de routine, créant des économies d'échelle que les cros de jeu pur ne peuvent pas égaler. l'entreprise cible les promoteurs de biotechnologie en développant des candidats en médecine de précision où les services de laboratoire et cliniques intégrés réduisent les frais généraux de coordination et accélèrent les délais de développement par rapport à la participation de fournisseurs distincts pour la gestion des essais et les essais en laboratoire.
Évolution récente
en mars 2026, iqvia a annoncé un partenariat stratégique avec un registre français des patients atteints de maladies rares afin de fournir des tests génétiques et des données d'histoire naturelle pour les maladies neurologiques ultra-rares. la collaboration vise à accélérer l'identification des patients et les évaluations de faisabilité des essais pour les sponsors développant des thérapies pour des conditions affectant moins de 500 patients français. https://www.iqvia.com (iqvia)
en février 2026, labcorp a élargi ses activités de laboratoire central français avec de nouvelles capacités de tests biomarqueurs pour les essais de thérapie cellulaire et génique. l'établissement traite des échantillons pharmacodynamiques et des tests diagnostiques complémentaires pour les sponsors de thérapie avancée menant des études cliniques françaises. https://www.labcorp.com (labcorp)
Quelles perspectives stratégiques définissent l'avenir du marché pharmaceutique france ?
Au cours des cinq à sept prochaines années, l'avantage concurrentiel sur le marché français des cro passera des capacités d'exécution opérationnelle aux plateformes de données et de technologies qui permettent de nouvelles méthodologies d'essai. le marché actuel récompense les cros qui peuvent enrôler les patients rapidement et fournir des données propres à temps, mais ces capacités deviennent commoditisées comme des outils électroniques de capture de données et de surveillance à distance standardiser dans l'ensemble de l'industrie. La prochaine frontière concurrentielle est l'intégration des données factuelles dans le monde réel, l'exécution décentralisée des essais et l'identification assistée des patients, qui nécessitent tous des investissements technologiques substantiels et des accords d'accès aux données qui créent des obstacles à l'entrée pour les concurrents qui n'ont pas d'échelle.
le risque que les projections du marché sous-estiment est le calendrier d'acceptation réglementaire des nouvelles méthodes d'essai. ansm a publié des lignes directrices sur les essais décentralisés et les preuves réelles, mais l'examen réglementaire réel des présentations utilisant ces approches demeure limité. Si les autorités de régulation se montrent plus conservatrices dans la pratique que ne le suggèrent les documents d'orientation, les promoteurs peuvent retarder l'adoption de ces méthodes, ce qui réduirait la demande de capacités de cro dans ces domaines et favoriserait l'exécution d'essais traditionnels sur place lorsque le précédent réglementaire est bien établi. Cela profiterait aux cros titulaires dotés de réseaux de sites solides tout en défavorisant les nouveaux venus qui ont beaucoup investi dans des plateformes d'essai décentralisées.
l'opportunité qui reste sous-évaluée est post-approbation des services de données factuelles du monde réel qui combinent la gestion des essais de phase IV avec des études d'observation utilisant des bases de données de santé françaises. Les payeurs ont de plus en plus besoin de données sur l'efficacité du monde réel pour appuyer les décisions de remboursement, et les promoteurs ont besoin de cros capables de concevoir des programmes intégrés qui répondent à la fois aux exigences réglementaires post-commercialisation et aux besoins en preuve des payeurs. le segment est actuellement petit, mais offre des marges plus élevées que le travail de phase IV traditionnel parce qu'il nécessite des capacités spécialisées en économie de la santé, en épidémiologie et en analyse de base de données que la plupart des cros ne maintiennent pas. les entreprises qui renforcent ces capacités saisiront la demande croissante des promoteurs de programmes de production de données probantes qui servent plusieurs intervenants plutôt que de satisfaire simplement aux obligations réglementaires.
Foire aux questions
Trouvez des réponses rapides aux questions les plus courantes.
le marché des cro pharmaceutiques france devrait atteindre 2,358,7 millions d'ici 2033.
les principaux segments du marché pharmaceutique france sont par type (recherche clinique, recherche préclinique, services de laboratoire, autres); par application (développement de médicaments, essais cliniques, études toxicologiques, gestion des données, autres); par utilisateur final (entreprises pharmaceutiques, entreprises de biotechnologie, instituts de recherche, autres); par phase (phase i, phase ii, phase iii, phase iv, autres).
les principaux acteurs du marché pharmaceutique france sont iqvia, labocorp, syneos health, parexel, icon plc, charles rivier, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat.
la taille actuelle du marché pharmaceutique de cro france est de 1.295,8 millions en 2025.
le marché pharmaceutique france cro est de 7,82 % de 2026 à 2033.
Rapports récemment publiés
-
Apr 2026
Marché des Services bancaires du sang de cordon
services bancaires de sang de cordon taille du marché, part et rapport d'analyse par type de service (collecte, traitement, stockage), par type de banque (banques privées, banques publiques et banques hybrides), par composante (sang de cordon et tissus de cordon), par utilisateur final (hôpitaux, instituts de recherche, entreprises de biotechnologie, etc.) et par géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 - 2031
-
Apr 2026
Marché des Processeurs ELISA
elisa transformateurs taille du marché, part et rapport d'analyse par type (analyseur de filtre optique elisa, et analyseur de grille optique elisa), par mode (analyseur automatique elisa, et analyseur semi-automatisé elisa), par applications (immunologie, mise au point de vaccins, surveillance des médicaments, etc.), par utilisateurs finals (entreprises de biotechnologie, sociétés pharmaceutiques, organisme de recherche sous contrat et laboratoires de diagnostic) et par géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 - 2031
-
Apr 2026
Marché des Scanner de diapositives au microscope
scanner de diapositives de microscope taille du marché, part et rapport d'analyse par type (scanner de diapositives de microscope portable, et scanner de diapositives de microscope de bureau), par application (recherche biologique, médecine, vétérinaire et autres) et géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 - 2031
-
Apr 2026
Marché des Cuisinières à micro-ondes
rapport sur la taille du marché, la part et l'analyse des appareils de cuisson à micro-ondes, par type de matériau (plastique, verre, céramique, silicone et métal), par application (cuisson, réchauffage et dégivrage), par utilisateur final (ménage, commercial (restaurants, hôtels et cafés) et industrie des services alimentaires), par chaîne de vente (commerce de détail en ligne, commerce de détail hors ligne (supermarchés, hypermarchés, magasins spécialisés) et vente directe (commerces d'entreprises) et géographique (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et amérique centrale), 2021 - 2031


