Europe santé contrat organisme de recherche taille du marché & prévisions:
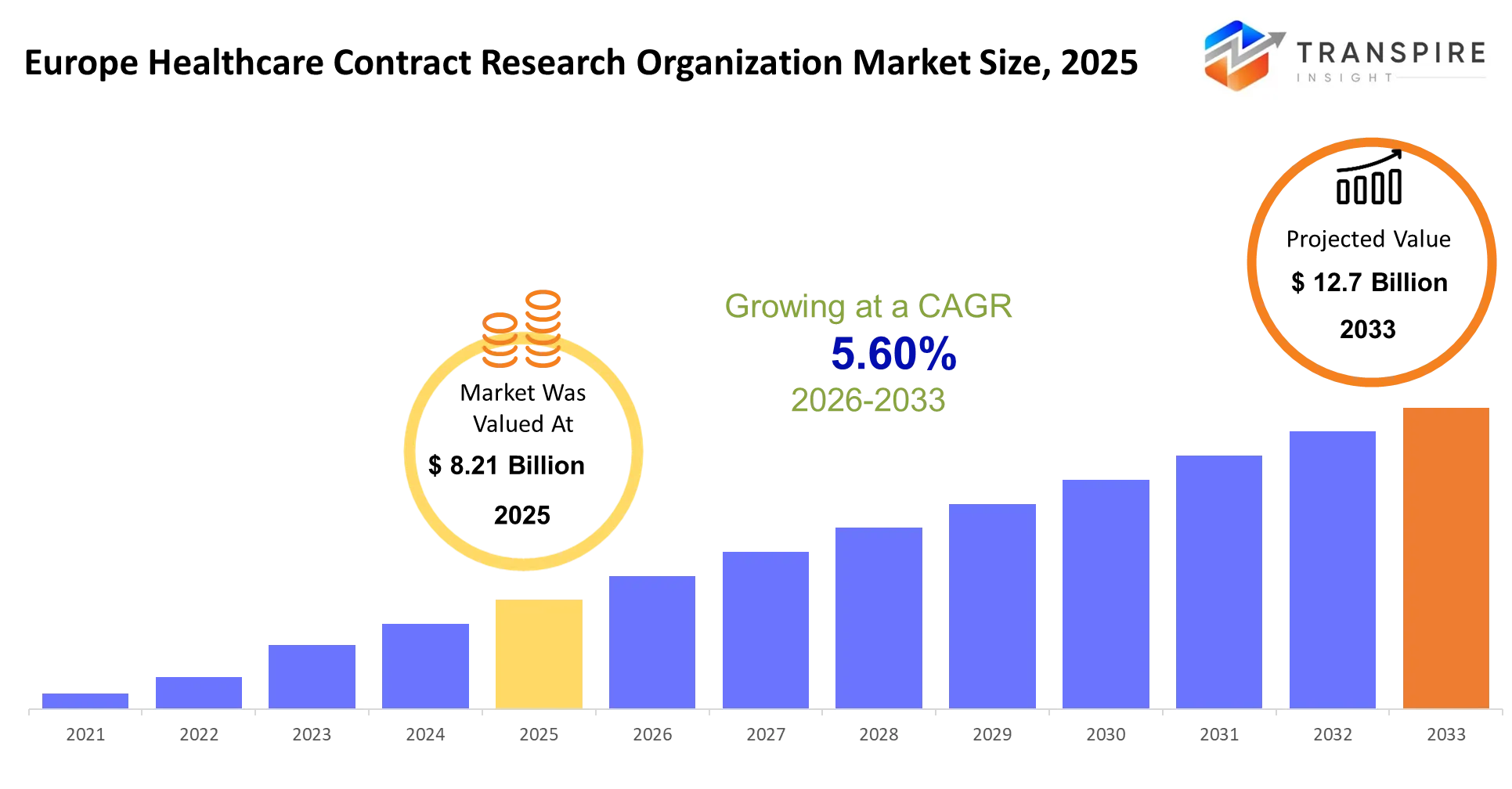
- Europe santé contrat organisation de recherche taille du marché 2025: usd 8,21 milliards
- Europe santé contrat organisme de recherche taille du marché 2033: usd 12,7 milliards
- Europe santé contrat organisme de recherche marché cagr: 5,60%
- les segments de marché des organismes de recherche sous contrat de soins de santé européens: par type (services de recherche clinique, services précliniques, services de laboratoire, autres), par application (développement de médicaments, essais cliniques, essais d'instruments médicaux, services de réglementation, autres), par utilisateur final (entreprises pharmaceutiques, entreprises de biotechnologie, entreprises d'instruments médicaux, instituts de recherche, autres), par phase (phase i, phase ii, phase iii, phase iv, autres)
pour en savoir plus sur ce rapport, télécharger gratuitement l'exemple de rapport
Europe santé contrat recherche organisation résumé du marché:
la taille du marché de l'organisation de recherche en contrats de soins de santé en Europe est estimée à 8,21 milliards d'euros en 2025 et devrait atteindre 12,7 milliards d'euros d'ici 2033, avec une croissance de 5,60 % entre 2026 et 2033. les organismes européens de recherche sous contrat de soins de santé fonctionnent comme des laboratoires de développement de médicaments sous-traités qui traitent tous les aspects de l'exécution d'essais cliniques pour les clients pharmaceutiques et biotech. les organisations permettent aux sponsors de développer des thérapies, depuis les tests de laboratoire jusqu'à la mise en marché, en fournissant les ressources opérationnelles essentielles et l'expertise spécialisée dont ils ont besoin.
Les modèles d'essais décentralisés et hybrides qui utilisent des outils de surveillance numérique et des méthodes d'engagement à distance des patients sont devenus la principale approche de recherche au cours des trois à cinq dernières années. le changement permet aux équipes de recherche de travailler avec plus de patients parce qu'il réduit leur besoin d'utiliser des installations de recherche spécifiques. La pandémie de covid-19 a été le principal catalyseur parce qu'elle nécessitait la poursuite des essais malgré les restrictions à la circulation et a entraîné une acceptation plus rapide des méthodes virtuelles par les organismes de réglementation.
l'exigence croissante de solutions rapides et flexibles est apparue comme le principal moteur derrière les sponsors qui utilisent maintenant des services d'externalisation à des taux plus élevés. la combinaison de l'analyse des données et des preuves réelles et des capacités d'essais adaptatifs a permis à cros de créer des flux de revenus évolutives à partir de leurs complexités opérationnelles.
principales perspectives du marché
- les pays d'Europe occidentale contrôlent le marché européen des organismes de recherche en contrats de soins de santé parce qu'ils détiennent plus de 65% de parts de marché que l'Allemagne, le royaume uni, et la France plomb en 2024.
- l'Europe orientale est la zone la plus en expansion rapide jusqu'en 2030 en raison de sa capacité à mener des essais rentables et à recruter rapidement des participants et de ses progrès vers la conformité des exigences réglementaires de l'Union européenne.
- le secteur des services d'essais cliniques mène le marché avec une part de 70% parce que les pays européens choisissent d'externaliser leurs études de phase ii et iii.
- la deuxième part de marché de l'industrie appartient aux services précliniques qui bénéficient du soutien d'entreprises de biotechnologie développant de nouveaux produits et de leurs activités de recherche et développement en expansion.
- le segment de la gestion des données et des services de données factuelles dans le monde réel connaît une croissance rapide parce que la mise en œuvre d'essais numériques entraîne une expansion de 2025 à 2030.
- le domaine de l'oncologie détient la plus grande part du marché des applications qui a atteint 30% en 2024 parce que les chercheurs médicaux mènent des études d'essai complexes et les chercheurs sur le cancer développent de nombreux médicaments contre le cancer.
- le développement de la médecine personnalisée et le soutien réglementaire aux maladies rares créent les zones de traitement médical les plus en développement rapide qui développent des thérapies ciblées.
- Les sociétés pharmaceutiques contrôlent environ 60 % du marché parce qu'elles s'associent avec des cros pour réduire leurs dépenses opérationnelles tout en accélérant leur processus de développement de médicaments.
- Les petites et moyennes entreprises de biotechnologie représentent le segment d'utilisateurs le plus en développement, qui dépend désormais de solutions complètes d'externalisation des services pour répondre à leurs besoins de croissance.
Quels sont les principaux moteurs, contraintes et opportunités du marché européen de la recherche sur les contrats de soins de santé?
l'élément principal qui stimule la croissance du marché européen de l'organisation de recherche sous contrat de soins de santé résulte de l'externalisation accrue de travaux de développement clinique compliqués qui sont nés de l'augmentation des dépenses de recherche et de développement qui dépassent aujourd'hui les 2 milliards d'euros par médicament approuvé. Les entreprises pharmaceutiques doivent réduire les délais de développement de leurs produits tout en répondant aux exigences réglementaires complexes qui existent dans divers pays européens. les organisations pratiquent maintenant des taux d'externalisation plus élevés parce que leurs essais cliniques en retard contiennent les travaux d'exécution les plus difficiles et les difficultés d'inscription des patients. les commanditaires qui dépensent plus d'argent pour les dépenses d'essai externes créent des contrats plus précieux qui mènent à des relations de service élargies avec les cros.
le système réglementaire européen reste divisé entre les différentes réglementations nationales en dépit de l'existence de régulations ema qui contrôlent les activités de recherche. Chaque pays exploite ses propres systèmes pour obtenir des approbations en matière d'éthique, gérer les données sur les patients et faire respecter la conformité dans les établissements de recherche. le modèle opérationnel existant pour les organismes de recherche clinique (cros) est confronté à des défis parce qu'il doit maintenir des opérations normalisées qui entraînent des délais de préparation plus longs et des dépenses administratives accrues. le processus conduit à étudier les retards qui rendent certains marchés moins attrayants, limitant ainsi les possibilités de revenus et limitant la croissance des modèles de recherche à l'échelle européenne.
Le potentiel de croissance des essais cliniques décentralisés est prometteur, car les systèmes de santé numériques sont plus avancés dans des pays comme l'Allemagne et la région nordique. La surveillance à distance et les technologies de saisie de données econsentables permettent à un plus grand nombre de patients de participer à des études qui permettent de s'inscrire plus rapidement.
Quel a été l'impact de l'intelligence artificielle sur le marché européen des organismes de recherche sous contrat de soins de santé?
Les organismes européens de recherche sous contrat utilisent désormais l'intelligence artificielle avec des outils numériques avancés pour transformer leur processus de conception d'essais cliniques par l'exécution automatisée de tâches opérationnelles essentielles. Les systèmes motorisés utilisent désormais le traitement du langage naturel ainsi que l'automatisation des processus robotiques pour exécuter le processus d'identification des patients et les évaluations de faisabilité du site et les tâches de nettoyage des données. le système établit un processus d'essai et de surveillance qui nécessite moins de travail manuel pour réaliser entre 20 et 20 % d'économies de temps tout en produisant des résultats de données plus précis grâce à des études multipays. les couches de contrôle numérique permettent aux organisations de surveiller la conformité parce qu'elles vérifient continuellement les données d'essai en fonction de l'évolution des normes réglementaires.
les modèles d'apprentissage automatique ajoutent des capacités prédictives qui ont une incidence directe sur la performance des essais. sponsors et cros utilisent des algorithmes pour prévoir les taux de recrutement des patients, prédire les risques d'abandon et optimiser la sélection des sites en fonction des ensembles de données historiques et réelles. le processus se traduit par une meilleure efficacité des inscriptions, ce qui réduit les retards coûteux, certaines études signalant des cycles de recrutement plus rapides de 15 à 25 %. ai soutient les conceptions d'essais adaptatifs en simulant les changements de protocole avant la mise en oeuvre, ce qui améliore la prise de décision dans des conditions incertaines.
les technologies permettent aux organisations d'obtenir de meilleurs résultats opérationnels grâce à trois principaux avantages, dont des taux de réussite des essais plus élevés, une réduction des modifications des protocoles et une réduction des dépenses totales de développement. le processus est confronté à des défis de mise en œuvre parce que les écosystèmes de données restent fragmentés et les coûts d'intégration restent élevés, en particulier pour unifier les systèmes cliniques traditionnels dans divers cadres réglementaires européens.
principales tendances du marché
- le domaine des essais décentralisés et hybrides a connu une croissance rapide depuis 2020 parce que plus de 40 pour cent des études européennes de recherche ont adopté des méthodes de test à distance pour poursuivre leurs opérations pendant les limitations de voyage.
- l'industrie pharmaceutique a augmenté ses activités d'externalisation de 45 pour cent en 2018 à plus de 55 pour cent en 2024, ce qui indique que l'industrie préfère externaliser ses travaux de recherche clinique à des partenaires externes.
- l'Europe orientale est devenue l'endroit le plus populaire pour les essais cliniques après 2021 parce que les processus de recrutement des patients dans cette région ont exigé 15 à 20 pour cent moins de temps que sur les marchés européens occidentaux.
- la période de 2019 à 2024 a apporté une complexité croissante aux essais en oncologie, ce qui a conduit les organismes de recherche clinique à avoir besoin de solutions de service complètes pour leurs tests biomarqueurs et leurs besoins de développement d'essais flexibles.
- Les entreprises de biotechnologie qui opèrent à l'échelle moyenne ont commencé à établir des partenariats stratégiques avec les cros après 2020 parce que cette approche leur a permis de réduire leur besoin de capacités opérationnelles internes tout en accélérant leurs premiers essais sur l'homme.
- la pandémie covid-19 a créé de nouvelles règles réglementaires qui ont permis aux agences d'utiliser la surveillance à distance et l'econsentement, modifiant ainsi les normes de conformité dans toute l'Europe.
- L'intégration des données probantes dans le monde réel s'est accélérée après 2022 en tant que commanditaires ayant utilisé des données extérieures pour appuyer leurs applications réglementaires et leurs travaux de recherche post-commercialisation.
- Cros a transformé leur modèle d'affaires en devenant des partenaires stratégiques de développement en investissant dans les technologies de santé numérique et les capacités du réseau de sites.
Europe santé contrat organisme de recherche segmentation du marché
par type
la catégorie des services de recherche clinique primaire conserve une position dominante sur le marché parce que les entreprises sous-traitent leurs opérations d'essais complexes qui nécessitent une expertise spécialisée, en particulier lors d'essais en phase terminale qui impliquent un maximum de dépenses et un examen réglementaire. Les services précliniques maintiennent une part stable parce que les entreprises de biotechnologie européennes élargissent leurs activités de recherche en début de carrière tandis que les services de laboratoire connaissent une croissance continue en raison des exigences croissantes pour les tests biomarqueurs et les services de diagnostic centralisés. Les commanditaires préfèrent maintenant des solutions de service complètes parce qu'ils considèrent les modèles de service intégrés comme plus efficaces que l'utilisation de multiples partenariats de fournisseurs distincts.
Les entreprises qui offrent des services cliniques combinés à des analyses de données avancées et à des capacités factuelles réelles connaissent actuellement la plus forte demande selon les tendances du marché. la prochaine période de croissance exigera des fournisseurs qu'ils développent des paquets d'outils numériques qu'ils peuvent combiner avec leurs services existants pour créer des contrats plus précieux tout en maintenant l'efficacité opérationnelle tout au long des différentes phases des essais cliniques.
pour en savoir plus sur ce rapport, télécharger gratuitement l'exemple de rapport
par demande
les essais cliniques constituent la plus grande partie de la recherche grâce à leur financement continu qui appuie médicament les pipelines de développement et les études de recherche multinationales basées sur l'Europe qui nécessitent une exécution complexe. le secteur des services de développement des médicaments maintient sa position parce que les grappes de biotechnologie bénéficient d'un financement accru du capital de risque qui appuie leurs travaux de recherche en début de carrière. La réglementation sur les instruments médicaux de l'Union européenne exige désormais davantage de travail de conformité et de procédures d'essai, ce qui a entraîné une demande accrue de services d'essai d'instruments médicaux.
Les promoteurs cherchent maintenant des services de réglementation parce qu'ils ont besoin d'aide pour naviguer dans les processus d'approbation multiples qui existent dans leurs activités commerciales. le domaine de la recherche montre une attention croissante à la médecine de précision et aux études sur les maladies rares qui exigent des méthodes d'essais cliniques distinctes et des techniques spécifiques pour sélectionner les participants à la recherche. À l'avenir, les partenaires et les promoteurs collaboreront plus étroitement grâce à une gestion adaptative des exigences réglementaires et à des essais expérimentaux qui utilisent des techniques fondées sur les données pour accélérer les processus d'approbation des essais.
par utilisateur final
le marché de l'utilisateur final soutient les entreprises pharmaceutiques parce que leurs programmes de recherche clinique étendus et leurs besoins permanents pour minimiser les dépenses opérationnelles. Les entreprises de biotechnologie représentent le groupe qui croît le plus rapidement, ce qui dépend de l'externalisation parce qu'elles manquent de capacités internes suffisantes et ont besoin de processus de développement adaptables. Les entreprises de matériel médical maintiennent la demande continue en raison d'exigences de conformité plus strictes, tandis que les établissements de recherche font progresser les connaissances grâce à leurs projets de recherche universitaires et financés par le gouvernement.
les différents groupes présentent des modes de participation uniques parce que les entreprises pharmaceutiques préfèrent établir des partenariats permanents tandis que les entreprises de biotechnologie doivent développer des opérations qui peuvent se développer rapidement. l'orientation future de la recherche établira des liens plus étroits entre les capacités des cro et la taille de l'organisation commanditaire, car les ensembles de services personnalisés et les ententes de partage des risques détermineront la concurrence sur le marché et les méthodes de rétention des clients.
par phase
les trois phases d'essai établissent la phase iii comme principale source de revenus pour les cros en raison de sa grande taille et de ses opérations coûteuses et de sa fonction essentielle pour obtenir l'approbation réglementaire. la nécessité croissante d'études de preuve de conception et de recherches sur l'optimisation des doses permet aux études de phase II de maintenir leur part de marché substantielle. le nombre d'essais de phase i ne cesse d'augmenter parce que plus d'entreprises de biotechnologie créent de nouveaux produits et effectuent leurs premiers tests humains. La demande de services de phase IV augmente parce que les entreprises doivent effectuer une surveillance post-commercialisation en vertu de nouveaux règlements de surveillance de la sécurité.
Les tendances de la demande montrent que les essais ultérieurs nécessitent des services plus complexes, ce qui conduit les entreprises à sous-traiter leur travail et à rechercher des compétences spécialisées. l'avenir apportera de nouvelles conceptions d'essais adaptatifs ainsi que des méthodes décentralisées qui changeront la façon dont les essais cliniques répartissent leurs phases tout en cherchant des moyens plus rapides de terminer toutes les phases d'essais et d'améliorer leur performance opérationnelle.
Quels sont les principaux cas d'utilisation à l'origine du marché européen des organismes de recherche sous contrat de soins de santé?
l'application primaire des centres d'essais cliniques sur leur exécution parce que les grandes entreprises pharmaceutiques exploitent des études de phase ii et iii multipays selon les exigences réglementaires européennes. l'exigence la plus exigeante découle de ce cas d'utilisation parce qu'il implique des activités opérationnelles entre plusieurs juridictions, y compris le recrutement des patients, la gestion du site et les besoins de conformité.
l'entreprise a développé ses capacités pour soutenir les essais d'instruments médicaux selon la réglementation eu des instruments médicaux et fournir des services de consultation réglementaires pour les entreprises de biotechnologie qui entreprennent des essais de premier en-humain. les petites et moyennes entreprises de biotechnologie se tournent maintenant vers les cros à deux fins, qui comprennent la recherche de leurs voies d'approbation et la réalisation d'une croissance efficace au cours de leur processus de développement initial.
les nouveaux cas d'utilisation des essais décentralisés impliquent l'application d'outils de surveillance à distance, tandis que les études factuelles fonctionnent comme des méthodes de surveillance post-commercialisation. les modèles sont devenus plus populaires parce que les organismes de réglementation ont commencé à accepter les paramètres numériques, tandis que les commanditaires cherchent maintenant à accéder plus rapidement à des données substantielles grâce à des méthodes de recherche clinique avancées.
les paramètres du rapport | détails |
Valeur de la taille du marché en 2025 | 8,21 milliards |
valeur de la taille du marché en 2026 | 8,67 milliards |
recettes prévues en 2033 | 12,7 milliards |
taux de croissance | de 5,60 % entre 2026 et 2033 |
année de référence | 2025 |
données historiques | 2021 - 2024 |
période de prévision | 2026 - 2033 |
couverture du rapport | prévisions de recettes, paysage concurrentiel, facteurs de croissance et tendances |
portée régionale | europe (allemagne, royaume uni, france, italie, espagne et reste de l'europe) |
entreprise clé | iqvia, labcorp, parexel, icône, syneos santé, charles rivière, medpace, ppd, covance, wuxi apptec, pra sciences de la santé, sgs, eurofins, envigo, clinipace |
personnalisation | personnalisation gratuite des rapports (pays, région et segment). utilisez des options d'achat personnalisées pour répondre à vos besoins de recherche exacts. |
segmentation du rapport | par type (services de recherche clinique, services précliniques, services de laboratoire, autres), par application (développement de médicaments, essais cliniques, essais d'instruments médicaux, services de réglementation, autres), par utilisateur final (entreprises pharmaceutiques, entreprises de biotechnologie, entreprises d'instruments médicaux, instituts de recherche, autres), par phase (phase i, phase ii, phase iii, phase iv, autres) |
Quelles sont les régions qui sont à l'origine de la croissance du marché de l'organisation européenne de recherche en contrats de soins de santé?
l'Europe occidentale contrôle le marché européen des organismes de recherche sous contrat de soins de santé parce que son système de réglementation fonctionne par l'intermédiaire de l'agence européenne des médicaments et que ses installations de recherche clinique fonctionnent à des niveaux avancés. les pays de la france allemande et du royaume uni maintiennent de vastes réseaux de sites d'essais et d'hôpitaux universitaires ainsi que des enquêteurs qualifiés. le système établi qui comprend le siège pharmaceutique et biotechnologie les grappes ainsi que les plateformes de santé numériques maintiennent une demande continue d'externalisation. la combinaison de systèmes robustes de protection des données et de réseaux de soins de santé avancés permet aux organisations de mener des essais cliniques internationaux complexes qui exigent la participation de nombreux pays.
l'Europe du Nord fonctionne comme une région fiable qui sweden denmark et finland utilisent pour prioriser l'intégration du registre des patients et le contrôle de la qualité des données. Cette région diffère de l'Europe de l'Ouest en mettant l'accent sur des essais plus petits mais très efficaces soutenus par des bases de données nationales sur la santé et des systèmes numériques unifiés. Les entreprises connaissent des conditions opérationnelles stables en raison de la conformité régulière à la réglementation et des initiatives de développement de la recherche parrainées par le gouvernement. le système maintient sa croissance grâce à un accès transparent aux données des patients et à une forte participation des services de santé publique, ce qui permet de se développer sans les exigences opérationnelles fondamentales dont les autres systèmes ont besoin.
l'Europe orientale démontre son taux de développement le plus rapide grâce à ses investissements récents dans l'infrastructure clinique et à sa conformité aux normes réglementaires européennes. les pays de poland hongrois et de la Roumanie ont amélioré les capacités du site et réduit les délais d'approbation depuis 2020. Les sponsors mondiaux ont choisi de travailler à l'exécution des procès parce que la combinaison de coûts opérationnels moins élevés et d'un recrutement plus rapide des patients leur procure des gains d'efficacité. l'élan actuel crée de multiples points d'entrée pour les cros et les investisseurs qui veulent renforcer leurs capacités tout en prenant en compte la nouvelle demande du marché entre 2026 et 2033.
qui sont les principaux acteurs du marché européen de la recherche sur les contrats de soins de santé et comment sont-ils compétitifs?
l'europe organisation de recherche contrat de soins de santé connaît la concurrence qui existe entre deux tendances de marché opposées de consolidation et de spécialisation. Les cros mondiaux maintiennent leur leadership sur le marché grâce à leurs vastes opérations et à leurs offres de services complètes et à leurs relations établies avec les entreprises pharmaceutiques, tandis que les entreprises de taille moyenne et de créneau utilisent leurs connaissances thérapeutiques spécifiques et leur expertise régionale pour rivaliser. Les entreprises sont aujourd'hui compétitives grâce à des services basés sur la technologie qui offrent de meilleurs résultats que leurs méthodes antérieures fondées sur les coûts parce que l'intégration des données et les systèmes d'essai décentralisés et les méthodes d'exécution rapide déterminent leur capacité à obtenir des contrats. la plate-forme numérique et l'expansion complète du service maintiennent une part de marché pour les entreprises établies, tandis que les nouveaux arrivants perturbent les marchés qui se concentrent sur les maladies rares et les essais précoces grâce à leurs opérations flexibles et leurs connaissances spécialisées.
les plateformes avancées d'analyse et de données réelles développées par iqvia fournissent aux sponsors les outils dont ils ont besoin pour créer des essais prédictifs adaptatifs. les organismes qui investissent dans des idées éclairées et développent des partenariats avec les organismes de soins de santé améliorent leur capacité d'accéder aux données, ce qui mène à de meilleurs résultats d'essais. icon plc fournit des solutions de service complètes qui relient le développement clinique à l'intelligence de la santé, grâce à ses multiples acquisitions, pour obtenir un meilleur contrôle sur les calendriers de projet et les dépenses opérationnelles. parexel aide les sponsors à naviguer sur les exigences réglementaires européennes grâce à ses services spécialisés de conseil et d'assistance à l'exécution.
l'organisme de développement de médicaments Labcorp utilise ses installations de laboratoire pour lier les tests diagnostiques aux opérations d'essais cliniques, ce qui permet une meilleure conception des études biomarqueurs et du regroupement des patients. syneos health fournit un modèle économique complet qui relie ses services de développement clinique à l'accès au marché, grâce à un système unique, qui offre des solutions d'exécution d'essais et d'entrée sur le marché sans faille.
liste des entreprises
- iqvia
- laboratoire
- parexel
- icône
- synéos santé
- Rivière Charles
- rythme
- pd
- avance
- L'application
- sciences de la santé
- sgs
- eurofins
- envigo
- clinipacées
récents développement
en octobre 2025, le thermopêcheur étend ses services d'essais cliniques par l'intégration de l'acquisition de clario: thermo-pêcheur progresse activement son acquisition de Exploitations de clario, renforçant son empreinte européenne des données d'essais cliniques et des services d'analyse. clario se spécialise dans la capture et la gestion des données d'essais cliniques – infrastructure de base utilisée par les cros dans toute l'Europe pour les essais en phase terminale. L'accord devrait être conclu au début de 2026.
Source: https://www.reuters.com
en avril 2026, le thermopêcheur de céder les activités de microbiologie à astorg: thermochercheur scientifique a accepté de vendre son activité de microbiologie à la société européenne de capital-investissement astrorg dans un marché de 1 075 milliards de dollars. l'unité prend en charge les flux de travail des essais cliniques et pharmaceutiques, qui sont étroitement liés aux services de laboratoire en Europe. le déménagement reflète la consolidation continue des capacités de soutien clinique externalisées dans la région.
Source: https://www.wsj.com
Quelles perspectives stratégiques définissent l'avenir du marché européen de la recherche sur les contrats de soins de santé?
le marché européen des organismes de recherche sous contrat de soins de santé suit un virage structurel vers des systèmes basés sur des plateformes qui utilisent l'infrastructure numérique et les données réelles et l'exécution d'essais décentralisés pour créer des avantages concurrentiels. le moteur fondamental derrière ce mouvement exige des organisations de raccourcir leur temps de développement pendant qu'elles développent des thérapies complexes qui nécessitent de grandes quantités de données pour créer des traitements tels que les produits biologiques et la médecine personnalisée. le marché progressera vers une collaboration stratégique à mesure que les organisations développeront leurs capacités pour servir de partenaires complets en matière de données et d'exécution, ce qui les aidera à obtenir davantage de financement auprès des commanditaires.
Le risque caché de fragmentation des données ainsi que les différentes réglementations relatives à l'utilisation des données sur les patients créent un danger que les modèles d'essai pilotés par l'ai peinent à fonctionner dans différents pays. Cette limitation créera des obstacles aux efforts internationaux de normalisation qui diminueront les avantages d'efficacité que les organisations s'attendent à obtenir grâce à leurs initiatives de transformation numérique.
l'Europe de l'Est offre une opportunité émergente d'expansion des essais hybrides, car son infrastructure et son cadre réglementaire en développement permettent de faciliter le recrutement des patients, qui peut être étendu. Les participants au marché doivent développer des plateformes numériques qui permettent l'interopérabilité des systèmes ainsi que la création de réseaux régionaux de sites pour atteindre leurs objectifs de maintien de l'accès aux données tout en assurant la conformité réglementaire et la flexibilité opérationnelle.
Europe santé contrat recherche organisation marché rapport segmentation
par type
- services de recherche clinique
- Services précliniques
- services de laboratoire
- autres
par demande
- développement des médicaments
- essais cliniques
- tests médicaux
- services réglementaires
- autres
par utilisateur final
- sociétés pharmaceutiques
- Entreprises de biotechnologie
- entreprises de matériels médicaux
- instituts de recherche
- autres
par phase
- phase i
- phase ii
- phase iii
- phase iv
- autres
Foire aux questions
Trouvez des réponses rapides aux questions les plus courantes.
la taille approximative du marché de l'organisation de recherche en contrats de soins de santé pour le marché sera de 12,7 milliards en 2033.
les segments clés du marché européen des organismes de recherche sous contrat de soins de santé sont par type (services de recherche clinique, services précliniques, services de laboratoire, autres), par application (développement de médicaments, essais cliniques, essais d'instruments médicaux, services de réglementation, autres), par utilisateur final (entreprises pharmaceutiques, entreprises de biotechnologie, entreprises de dispositifs médicaux, instituts de recherche, autres), par phase (phase i, phase ii, phase iii, phase iv, autres).
iqvia, labcorp, parexel, icon, syneos health, charles river, medpace, ppd, covance, wuxi apptec, pra health sciences, sgs, eurofins, envigo, clinipace.
la taille actuelle du marché des organismes de recherche sous contrat de soins de santé est de 8,21 milliards en 2025.
le marché european health contract research organization est de 5,60 %.
- iqvia
- laboratoire
- parexel
- icône
- synéos santé
- Rivière Charles
- rythme
- pd
- avance
- L'application
- sciences de la santé
- sgs
- eurofins
- envigo
- clinipacées
Rapports récemment publiés
-
Apr 2026
Marché des Services bancaires du sang de cordon
services bancaires de sang de cordon taille du marché, part et rapport d'analyse par type de service (collecte, traitement, stockage), par type de banque (banques privées, banques publiques et banques hybrides), par composante (sang de cordon et tissus de cordon), par utilisateur final (hôpitaux, instituts de recherche, entreprises de biotechnologie, etc.) et par géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 - 2031
-
Apr 2026
Marché des Processeurs ELISA
elisa transformateurs taille du marché, part et rapport d'analyse par type (analyseur de filtre optique elisa, et analyseur de grille optique elisa), par mode (analyseur automatique elisa, et analyseur semi-automatisé elisa), par applications (immunologie, mise au point de vaccins, surveillance des médicaments, etc.), par utilisateurs finals (entreprises de biotechnologie, sociétés pharmaceutiques, organisme de recherche sous contrat et laboratoires de diagnostic) et par géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 - 2031
-
Apr 2026
Marché des Scanner de diapositives au microscope
scanner de diapositives de microscope taille du marché, part et rapport d'analyse par type (scanner de diapositives de microscope portable, et scanner de diapositives de microscope de bureau), par application (recherche biologique, médecine, vétérinaire et autres) et géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 - 2031
-
Apr 2026
Marché des Cuisinières à micro-ondes
rapport sur la taille du marché, la part et l'analyse des appareils de cuisson à micro-ondes, par type de matériau (plastique, verre, céramique, silicone et métal), par application (cuisson, réchauffage et dégivrage), par utilisateur final (ménage, commercial (restaurants, hôtels et cafés) et industrie des services alimentaires), par chaîne de vente (commerce de détail en ligne, commerce de détail hors ligne (supermarchés, hypermarchés, magasins spécialisés) et vente directe (commerces d'entreprises) et géographique (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et amérique centrale), 2021 - 2031


