Résumé du marché
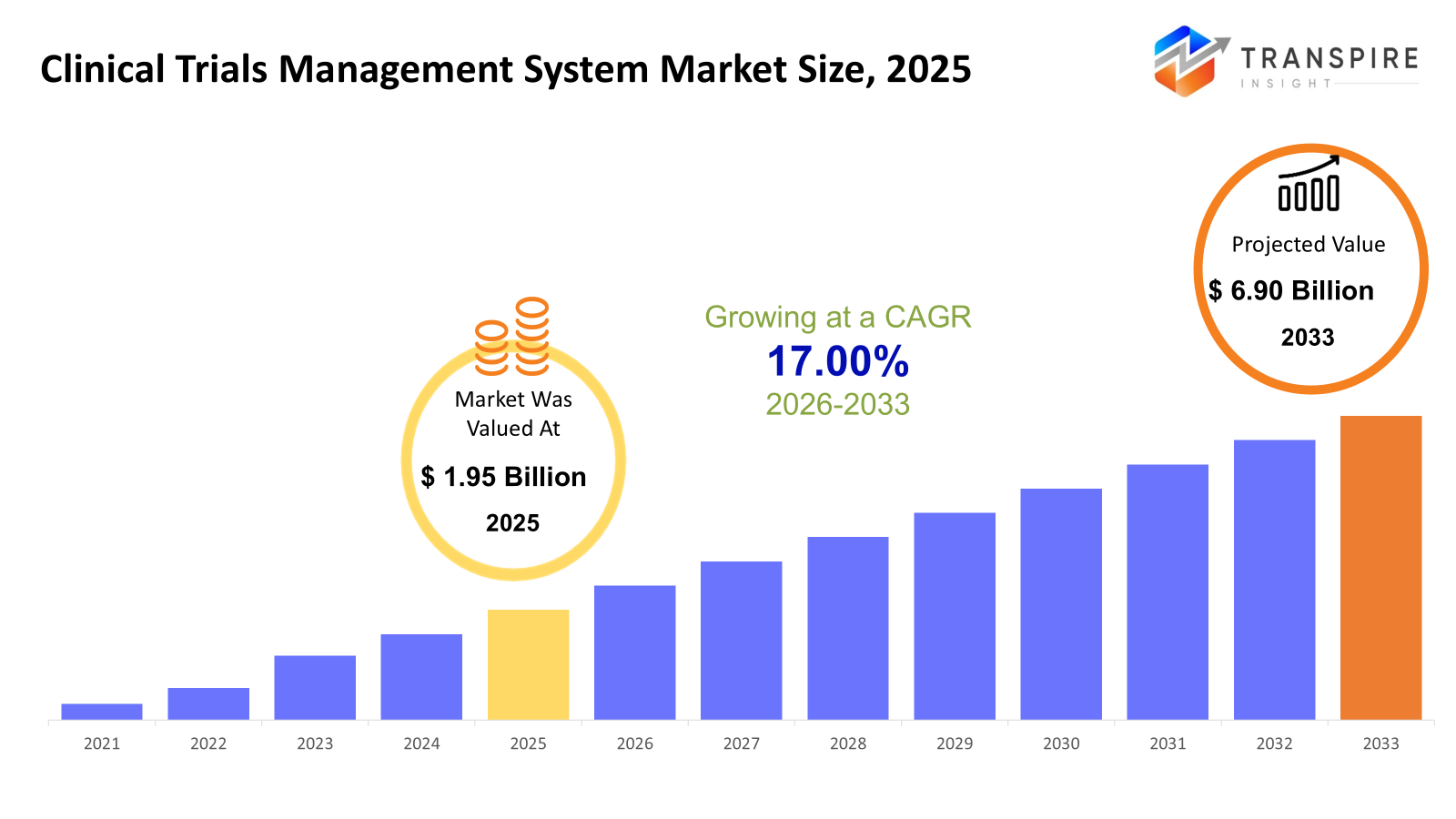
la taille du marché du système mondial de gestion des essais cliniques a été estimée à 1,95 milliard d'euros en 2025 et devrait atteindre 6,90 milliards d'euros d'ici 2033, en croissance à un cagr de 17,00 % de 2026 à 2033. le marché des ctms connaît un taux de croissance constant au fil du temps en raison de facteurs comme l'augmentation des dépenses de R&D dans les industries pharmaceutiques et de biotechnologie, l'augmentation du nombre d'essais cliniques et l'adoption de la technologie numérique pour effectuer des essais cliniques. il a été observé que la conformité réglementaire et les essais cliniques rentables et gérés dans le temps sont aussi les moteurs du marché pour l'industrie des ctms. La technologie basée sur le cloud dans les ctms offre un meilleur accès et une plus grande collaboration sur plusieurs sites, avec son intégration avec ai contribuant à sa croissance du marché
Taille du marché et prévisions
- Taille du marché en 2025: 1,95 milliard d'euros
- 2033 taille projetée du marché: 6,90 milliards d'euros
- cagr (2026-2033) : 17,00 %
- Amérique du Nord : plus grand marché en 2026
- asia pacific: marché en croissance rapide
pour en savoir plus sur ce rapport, télécharger gratuitement l'exemple de rapport
Analyse des principales tendances du marché
- l'Amérique du Nord fonctionne comme un centre important pour la mise en œuvre des ctms, en raison santé l'infrastructure, les dépenses de R&D par les sociétés pharmaceutiques, et la présence de cros pour gérer les essais à divers endroits au sein de nous, au Canada et au Mexique
- les États-Unis sont le marché clé dans la région nord-américaine en raison de la tendance croissante à adopter la technologie, un système réglementaire difficile dans le pays, et la pratique d'externaliser les données d'essais cliniques pour raccourcir le calendrier et améliorer l'efficacité opérationnelle
- le marché pacifique asiatique représente un marché en croissance résultant d'environnements réglementaires favorables, d'activités d'externalisation croissantes vers des pays à faible coût, et des essais cliniques en hausse réalisés en Inde, en Chine, au Japon et en Corée du Sud
- Le modèle de déploiement basé sur le cloud est perçu comme étant en hausse car les organisations cherchent à déployer des solutions qui offrent une évolutivité et permettent ainsi d'économiser des coûts tout en facilitant le travail à distance, en réduisant les coûts et en accédant aux données d'essai en temps réel dans des environnements géographiquement répartis
- il dirige également les demandes car il assure l'exactitude, l'intégrité et la conformité réglementaire des données d'essai, un élément clé qui assure une approbation plus rapide des médicaments ainsi qu'une surveillance efficace des essais en plusieurs phases
- pharmaceutique et les entreprises de biotechnologie sont considérées comme les utilisateurs finals de ctms en raison de leur investissement élevé dans la R&D, la culture novatrice et la nécessité d'une solution intégrée de ctms pour mener efficacement des essais cliniques complexes à l'échelle mondiale.
donc, marché du système de gestion des essais cliniques est destiné à simplifier le processus de planification, d'exécution et de suivi des essais cliniques pour les entités pharmaceutiques, de biotechnologie et de recherche. le champ d'application du logiciel et des services de gestion des essais cliniques soutient la gestion des données des essais cliniques, la conformité juridique, l'inscription et la gestion du site, en vue d'optimiser le processus et d'économiser du temps. la complexité croissante des essais cliniques et la nécessité d'une exploitation efficace dans divers sites du monde ont conduit à la popularité croissante du logiciel de gestion des essais cliniques pour assurer l'exactitude du processus. l'utilisation du cloud computing a été reconnue comme la technologie la plus favorisée pour déployer le système de gestion des essais cliniques en raison de son efficacité, de son accessibilité et de ses avantages en termes de coûts, en particulier dans le cas des cros et des multinationales pharmaceutiques. La pression croissante exercée sur les patients pour qu'ils soient maintenus dans les essais cliniques et accélérer le processus d'approbation des médicaments a contribué à la popularité croissante du système de gestion des essais cliniques. l'importance du système de gestion des essais cliniques est démontrée par son utilisation comme outil essentiel dans le processus d'optimisation des efforts de recherche clinique mondiale.
marché du système de gestion des essais cliniquessegmentation
par composante
- logiciel
le logiciel le plus dominant dans ce segment est les ctms, car cela aide à gérer efficacement les essais cliniques, la collecte de données et la conformité aux exigences réglementaires. elle contribue à une prise de décision efficace en utilisant l'analyse et rend les rapports disponibles en temps réel, augmentant ainsi la productivité.
- services
Les services de mise en œuvre, de formation et d'appui complètent l'adoption de logiciels en assurant une meilleure intégration avec l'infrastructure existante. l'importance des services gérés et des services de conseil ne saurait être surestimée, en particulier pour les entreprises qui manquent d'expertise interne, favorisant ainsi la croissance de ce secteur.
par mode de déploiement
- sur site
Les solutions sur site restent privilégiées parmi les grandes entreprises pharmaceutiques et les cros qui ont besoin d'un contrôle complet sur la sécurité et la personnalisation des données. Bien qu'ils aient des coûts initiaux plus élevés, ils sont associés à des intégrations impliquant des systèmes existants et offrent le respect de règlements régionaux rigoureux en matière de données.
- nuageux
L'évolutivité, l'investissement initial plus faible et l'accessibilité à distance sont des caractéristiques clés de la croissance rapide des solutions ctms basées sur le cloud. ils permettent une collaboration en temps réel sur plusieurs sites d'essai. Il est donc idéal pour les essais cliniques mondiaux, en particulier lorsque des études de recherche multirégionales et des marchés émergents sont envisagés.
pour en savoir plus sur ce rapport, télécharger gratuitement l'exemple de rapport
par demande
- gestion des données cliniques
il s'agit d'une section essentielle parce qu'elle sert à valider l'exactitude de la collecte et du stockage des données des essais cliniques. la gestion efficace des données cliniques non seulement minimise les erreurs, mais facilite également l'approbation rapide des médicaments.
- gestion de la conformité réglementaire
Les outils de gestion de la conformité réglementaire permettent aux organisations de maintenir des normes et des règlements internationaux, tels que fda, ema et ich-gcp. L'automatisation des rapports et de la surveillance des risques liés à la conformité a rendu cela indispensable, en particulier pour les essais cliniques mondiaux.
- planification et gestion des essais :
Ce sous-segment permet une planification et une programmation efficaces sur différents sites. les capacités d'analyse aident à prévoir les coûts et le temps nécessaires, ce qui augmente l'efficacité et réduit les coûts d'exploitation.
- Gestion du site
solutions dans la gestion du site aident à la coordination du site, l'optimisation de l'inscription des patients, ainsi que la surveillance de la performance. Cela permet de sensibiliser les sponsors et les cros à l'amélioration des résultats des essais et au maintien du protocole du site.
- recrutement et rétention des patients
Ce segment traite de certains des plus grands défis auxquels font face les essais cliniques aujourd'hui, à savoir l'inscription en temps opportun aux essais et la conformité des patients. ces outils d'analyse, d'engagement et de stratégie de recrutement aident grandement non seulement à réduire les taux d'abandon, mais aussi à assurer le succès des essais.
par utilisateur final
- sociétés pharmaceutiques et de biotechnologie
Ces organisations favorisent l'adoption de ctms en raison de dépenses élevées en R&D et de la nécessité d'effectuer des essais efficaces. ces organisations ont des normes élevées en matière d'innovation et de conformité, ce qui nécessite un système ctms efficace et innovant qui aide à réaliser des essais complexes et en plusieurs phases.
- Organismes de recherche contractuels (cros)
Cros s'appuie sur des ctms pour gérer efficacement divers essais pour les clients. Les solutions basées sur le cloud et évolutives aident les cros à normaliser divers processus dans différentes régions, à assurer des rapports précis et à maintenir des normes élevées à des fins réglementaires.
- instituts universitaires et de recherche
Les instituts universitaires et de recherche utilisent des systèmes de ctms pour effectuer des essais financés par des subventions ainsi que des essais entrepris par des chercheurs. ctms systèmes qui mettent l'accent sur la rentabilité, la simplicité et la précision permettent de réaliser des essais à plus petite échelle tout en respectant les directives institutionnelles ou nationales.
- hôpitaux et cliniques
ctms est utilisé par les hôpitaux et les cliniques pour gérer les essais cliniques parallèlement à leurs opérations régulières. l'intégration des dossiers des patients et des outils d'engagement des patients facilite la gestion et la réduction du fardeau administratif.
perspectives régionales
l'Amérique du Nord est la première sur le marché. les États-Unis d'Amérique, du Canada et du Mexique sont les principaux pays contributeurs au marché en raison des dépenses pharmaceutiques favorables, de l'environnement réglementaire et de la présence de cros importants. l'europe comprend de grands segments de pays comme l'Allemagne, le uk, la France, l'Espagne et l'Italie. Ces segments de pays connaissent une croissance constante, qui est prescrite par la conformité à la réglementation, la numérisation et la modernisation de leur infrastructure respective. asia pacific émerge comme un marché en croissance rapide alimenté par des segments de pays comme l'Inde, la Chine, le Japon, la Corée du Sud et l'Australie en raison d'essais cliniques à faible coût, d'activités d'externalisation accrues et d'initiatives gouvernementales à l'échelle du pays pour promouvoir les activités de recherche. l'Amérique du Sud comprend des segments de pays comme le Brésil et l'argentina. Ces segments de pays adoptent lentement des ctms avec des motifs pour optimiser les coûts tout en menant des essais cliniques. le Moyen-Orient & Afrique comprend des segments de pays comme saudi arabia, les uae, Afrique du Sud. ces segments de pays sont considérés comme étant à venir sur le marché en raison de la croissance des dépenses en infrastructures et des activités de recherche clinique. ctms semble être favorisé par eux pour gérer des essais cliniques multi-site à l'aide de l'infrastructure nuageuse en raison de la contrainte géographique d'avoir dispersé les équipes.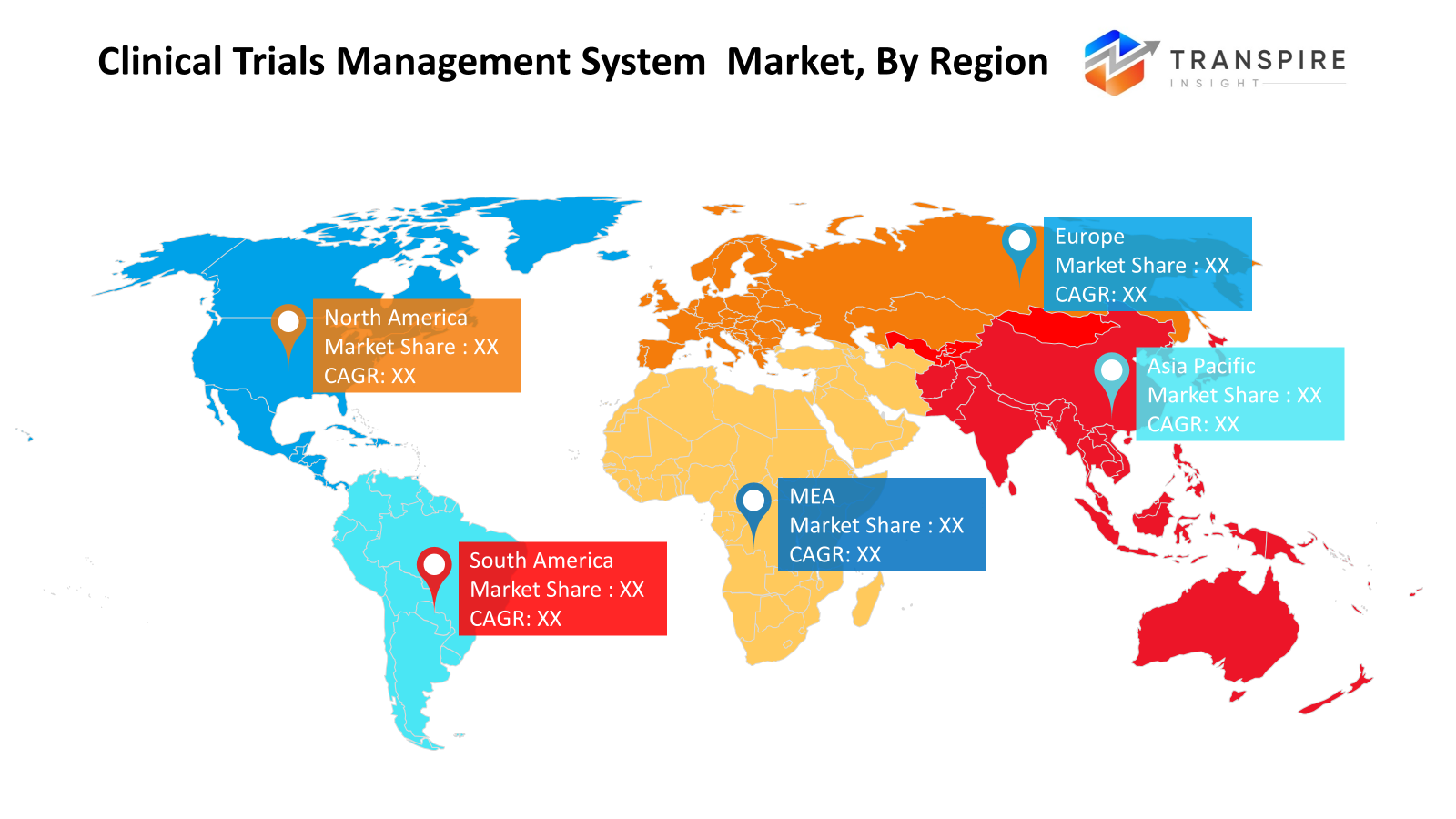
pour en savoir plus sur ce rapport, télécharger gratuitement l'exemple de rapport
récents développement
- août 2025, Tant les systèmes iqvia que veeva ont annoncé un partenariat clinique et commercial mondial à long terme qui règle tous les différends juridiques en suspens entre les parties et assure l'intégration transparente des offres de logiciels, de données et de services des deux entreprises à leurs clients en sciences de la vie. cela permet aux clients d'utiliser les applications et les services de la société avec des solutions dans l'espace clinique et commercial offert par l'autre pour permettre des améliorations dans l'efficacité clinique et commerciale.
- en janvier 2025, Veeva systems, inc. a signalé que plus de 200 entreprises, dont 17 des 20 premières entreprises biopharmaceutiques, utilisent maintenant les ctms veeva pour effectuer des essais cliniques plus rapides et plus efficaces. Le communiqué de presse dit qu'il devrait permettre une centralisation accrue des données, des flux de travail simplifiés, des transferts automatisés entre les cros et les sponsors, et de nouvelles innovations de produits régulièrement fournies par le biais de communiqués axés sur le client afin de soutenir les modèles d'exploitation des essais cliniques insources et externalisées.
(source:https://www.veeva.com/ressources/plus-que-200-entreprises-advance-trial-management-with-veeva-ctms)
les paramètres du rapport | détails |
Valeur de la taille du marché en 2025 | 1,95 milliard |
valeur de la taille du marché en 2026 | 2,30 milliards d'euros |
recettes prévues en 2033 | 6,90 milliards |
taux de croissance | cagr de 17,00 % de 2026 à 2033 |
année de référence | 2025 |
données historiques | 2021 – 2024 |
période de prévision | 2026 – 2033 |
couverture du rapport | prévisions de recettes, paysage concurrentiel, facteurs de croissance et tendances |
portée régionale | Amérique du Nord; Europe; Asie Pacifique; Amérique latine; Moyen-Orient & Afrique |
champ d'application | États-Unis; canada; Mexique; Royaume-Uni; Allemagne; France; Italie; Espagne; Danemark; Suède; Norvège; Chine; Japon; Inde; Australie; Corée du Sud; Thailand; Brésil; Argentine; Afrique du Sud; arabia saudi; Émirats arabes unis |
entreprise clé | medidata solutions, oracle corporation, veeva systems, iqvia inc., dassault systèmes, parexel international, ibm watson health, clario, revvity, wcg clinical, bioclinica, arisglobal llc, datatrak international, mastercontrol inc., mednet solutions inc. |
personnalisation | personnalisation gratuite des rapports (pays, région et segment). utilisez des options d'achat personnalisées pour répondre à vos besoins de recherche exacts. |
segmentation du rapport | par composante (logiciel, services), par mode de déploiement (sur site, cloud), par application (gestion des données cliniques, gestion de la conformité réglementaire, planification et gestion des essais, gestion du site, recrutement et rétention des patients) et par utilisateur final (entreprises pharmaceutiques et de biotechnologie, organismes de recherche contractuels (cros), instituts universitaires et de recherche, hôpitaux et cliniques) |
système de gestion des essais cliniques clés
Les solutions de medidata sont bien considérées comme l'un des principaux fournisseurs de ctms ainsi que de systèmes ecliniques intégrés basés sur le cloud pour les essais cliniques menés dans le monde entier. Il offre à ses utilisateurs des fonctionnalités de bout en bout telles que la planification, la gestion des données en temps opportun, l'analyse et les rapports qui peuvent simplifier les processus décisionnels. L'intégration des données avec de nombreux systèmes, y compris les systèmes edc ainsi que les systèmes axés sur le patient, est assez large. Cela revêt une importance considérable car il assure une meilleure qualité des données ainsi que des délais plus rapides. En outre, l'innovation grâce à des capacités d'action et à des outils de surveillance sophistiqués a fait de la médicat l'un des principaux acteurs. ses solutions sont recherchées par les grandes entreprises pharmaceutiques et de biotechnologie en raison de leur accent mis sur la rapidité et l'innovation.
clé entreprises du système de gestion des essais cliniques:
- les solutions de medidata
- société
- systèmes veeva
- iqvia inc.
- dassault systèmes
- parexel international
- ibm watson santé
- clario
- la revité
- wcg clinique
- bioclinique
- arisglobal lc
- datatrak international
- contrôle maître inc.
- solutions mednet inc.
segmentation du rapport de marché du système mondial de gestion des essais cliniques
par composante
- logiciel
- services
par mode de déploiement
- sur site
- nuageux
par demande
- gestion des données cliniques
- gestion de la conformité réglementaire
- planification et gestion des essais
- Gestion du site
- recrutement et rétention des patients
par utilisateur final
- sociétés pharmaceutiques et de biotechnologie
- Organismes de recherche contractuels (cros)
- Instituts universitaires et de recherche
- hôpitaux et cliniques
perspectives régionales
- Amérique du Nord
- États-Unis
- Canada
- Mexique
- Europe
- Allemagne
- Royaume uni
- france
- espagne
- italiques
- le reste de l'Europe
- Asie pacifique
- japon
- Chine
- australia & nouveau zèle
- Corée du Sud
- indie
- le reste du Pacifique asiatique
- Amérique du Sud
- Brésil
- l'argentine
- le reste de l'Amérique du Sud
- Moyen-Orient & Afrique
- saudi arabia
- Emirats arabes unis
- Afrique du Sud
- reste du Moyen-Orient & Afrique
Foire aux questions
Trouvez des réponses rapides aux questions les plus courantes.
la taille approximative du marché du système de gestion des essais cliniques sera de 6,90 milliards d'euros en 2033.
segments clés du marché des systèmes de gestion des essais cliniques par composante (logiciels, services), par mode de déploiement (sur site, cloud), par application (gestion des données cliniques, gestion de la conformité réglementaire, planification et gestion des essais, gestion des sites, recrutement et rétention des patients) et par utilisateur final (sociétés pharmaceutiques et de biotechnologie, organismes de recherche contractuels (cros), instituts universitaires et de recherche, hôpitaux et cliniques).
les principaux acteurs du marché des systèmes de gestion des essais cliniques sont les solutions de médicaments, la société d'oracle, les systèmes veeva, iqvia inc., parexel international.
la région nord de l'amérique dirige le marché du système de gestion des essais cliniques.
le cagr du marché du système de gestion des essais cliniques est de 17,00 %.
- les solutions de medidata
- société
- systèmes veeva
- iqvia inc.
- dassault systèmes
- parexel international
- ibm watson santé
- clario
- la revité
- wcg clinique
- bioclinique
- arisglobal lc
- datatrak international
- contrôle maître inc.
- solutions mednet inc.
Rapports récemment publiés
-
Apr 2026
Marché des AI dans la rétinopathie diabétique
ai dans la rétinopathie diabétique taille du marché, rapport de part et d'analyse par type (systèmes d'ai de dépistage, systèmes d'ai de diagnostic et modèles d'ai de prévision), par segment d'application (hôpitaux, cliniques d'ophtalmologie, centres de diagnostic, et recherche et développement), et géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 - 2031
-
Apr 2026
Marché des Essais psychométriques
tests psychométriques, taille du marché, rapport de partage et d'analyse par type (tests de personnalité, tests d'aptitude/d'aptitude, tests de compétence/de connaissance, etc.), par application (acquisition de talents et gestion des talents), et géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 – 2031
-
Apr 2026
Marché des Collecte d'échantillons biologiques rares
rare collecte d'échantillons biologiques taille du marché, part et rapport d'analyse par type (kits d'isolation et réactif, tubes de collecte de sang, etc.), par application (oncologie, transcriptomique, pharmacogénomique, etc.), et géographie (amérique du nord, europe, asie-pacifique, moyen-orient et afrique, amérique du sud et centre), 2021 – 2031
-
Apr 2026
Marché des Pendentif de levage du patient
marché des pendentifs de levage de patients par type de produit (pendents câblés, sans fil, programmables), par type d'opération (manuel, électrique), par utilisateurs finaux (professionnels de la santé, patients), par application (hôpitaux, soins à domicile, centres de réadaptation, autres), par analyse de l'industrie, taille, part, croissance, tendances et prévisions 2021-2033
Nos clients
.jpg)









