Pronóstico del tamaño del mercado "
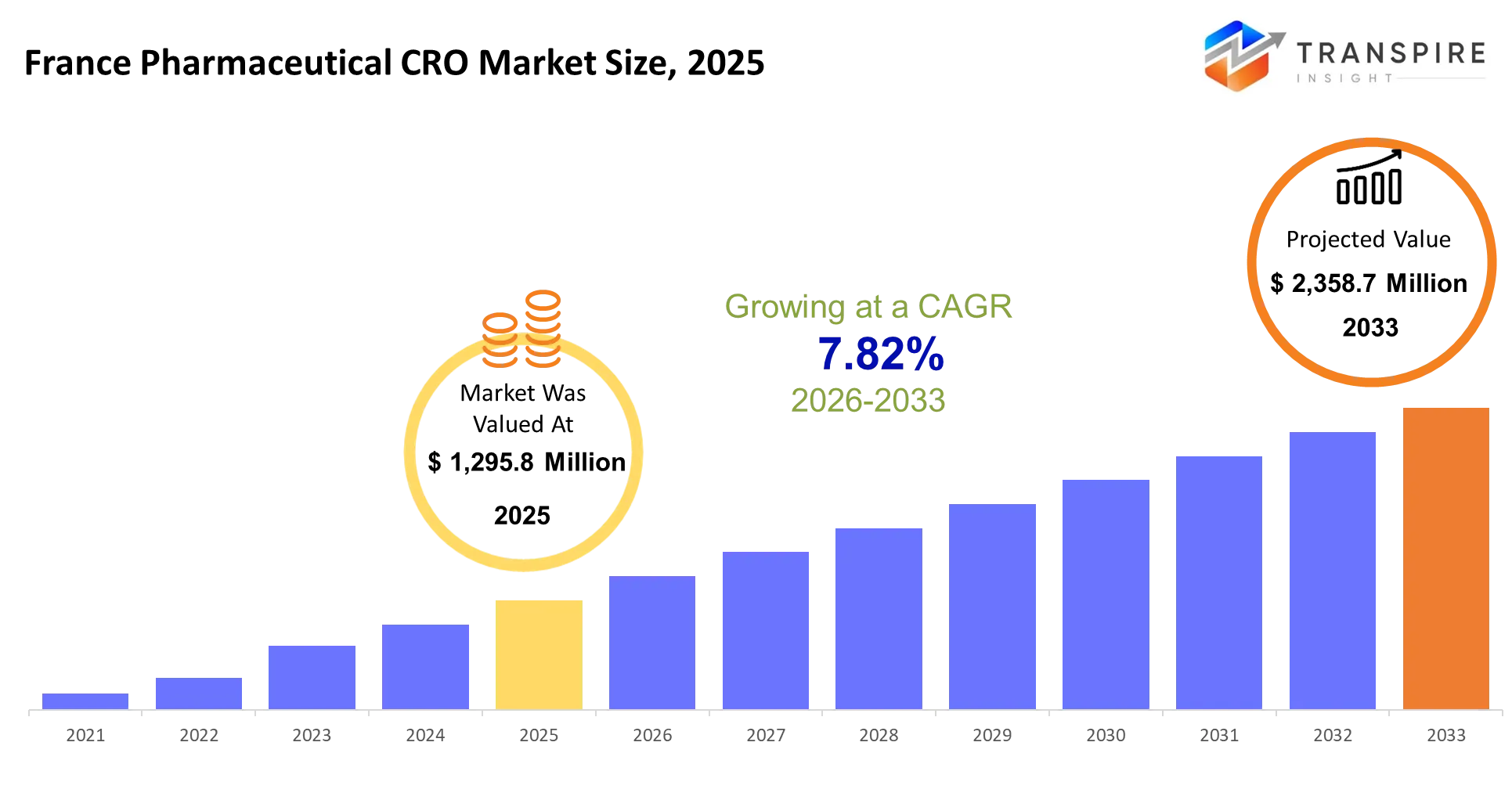
- franquicia farmacéutica cro tamaño 2025: usd 1.295,8 millones
- franque farmacéutico cro tamaño del mercado 2033: usd 2.358,7 millones
- franquicia farmacéutica cro mercado cagr: 7.82%
- franquicias farmacéuticas cro segmentos de mercado: por tipo (investigación clínica, investigación preclínica, servicios de laboratorio, otros); por aplicación (desarrollo de drogas, ensayos clínicos, estudios toxicológicos, gestión de datos, otros); por usuario final (empresas farmacéuticas, empresas biotecnológicas, institutos de investigación, otros); por fase (fase i, fase ii, fase III, fase iv, otros)
para aprender más sobre este informe, descargar informe de muestra gratis
france Pharma cro market summary
el mercado farmacéutico cro france fue valorado en el usd 1.295.8 millones en 2025. se espera que llegue a 2.358,7 millones de dólares en 2033, creciendo en un cagr de 7,82%. Las organizaciones de investigación de contratos prestan servicios de investigación externos a las empresas farmacéuticas y biotecnológicas, manejando todo desde estudios preclínicos hasta la vigilancia posterior al mercado de fase iv. Los servicios de investigación clínica representan el 65% del mercado francés porque los patrocinadores prefieren transferir la gestión compleja de los ensayos a proveedores especializados en lugar de mantener las capacidades internas en múltiples áreas terapéuticas y jurisdicciones regulatorias.
tres cambios regulatorios entre 2020 y 2025 reen forma de cómo funcionan los cros franceses. En primer lugar, la regulación de ensayos clínicos eu introdujo procesos armonizados de aprobación en todos los estados miembros, que redujeron la variabilidad del plazo pero aumentaron los requisitos de documentación inicial. En segundo lugar, la plataforma nacional de datos sobre salud de Franco abrió el acceso a conjuntos de datos de pruebas reales que los patrocinadores pueden vincular ahora con los resultados del ensayo clínico, creando demanda de cros con capacidades bioinformáticas. Tercero, el ansma comenzó a aceptar protocolos descentralizados de ensayo que permiten el monitoreo remoto de pacientes, que desplazaron la selección de sitios de investigadores de las redes tradicionales de hospitales hacia proveedores de salud doméstica y plataformas de telemedicina.
la expansión actual del mercado es impulsada por empresas biotecnológicas que externalizan el trabajo de desarrollo tardío que anteriormente manejaban internamente. pequeñas y medianas empresas de biotecnología carecen de la experiencia regulatoria para navegar por las sumisiones de ema y la red del sitio para ejecutar los ensayos de fase iii de varios países de manera eficiente. cros ofrecen a estas empresas acceso a relaciones de investigadores establecidas, experiencia en área terapéutica y especialistas en asuntos regulatorios sobre una base de proyecto en lugar de como topcount permanente. Este modelo de negocio permite a los patrocinadores de la biotecnología preservar el efectivo a la vez que se aceleran los plazos de desarrollo, lo que importa cuando los ciclos de financiación de riesgo requieren un progreso clínico demostrable cada 18 a 24 meses.
clave france farmacéutica cro market insights
- Los servicios de investigación clínica dominan el mercado farmacéutico cro con una participación del 65% en 2024, impulsado por el aumento de la externalización de la fase ii y la fase III de la gestión de ensayos.
- los servicios de investigación preclínica representan el 22% del mercado en 2024, apoyando a los candidatos de drogas de primera etapa que requieren pruebas toxicológicas y estudios farmacocinéticos.
- Las aplicaciones de desarrollo de drogas representan el 41,3% de la demanda de servicios cro en 2024, ya que las empresas farmacéuticas subcontratan el desarrollo de la formulación y las pruebas de estabilidad.
- Las aplicaciones de ensayos clínicos tienen un 38,7% de cuota de mercado en 2024, concentrada en oncología, inmunología y raras áreas terapéuticas de enfermedades donde el reclutamiento de pacientes es difícil.
- Las empresas farmacéuticas constituyen el 52,8% de la demanda de usuarios finales en 2024, subcontratando actividades de desarrollo clínico no básico para centrar los recursos internos en el descubrimiento y la comercialización.
- Las empresas biotecnológicas representan el 31,4% del mercado en 2024 y representan el segmento de usuarios finales de mayor crecimiento, que se expande en un 9,1% hasta 2033.
- ensayos de fase III generan 43,2% de los ingresos de investigación clínica en 2024, requiriendo grandes poblaciones de pacientes y períodos de monitoreo prolongados que favorezcan a los cros de servicio completo.
- los ensayos de fase II contribuyen el 28,6% de los ingresos en 2024, con creciente demanda de diseños de ensayos adaptativos que requieren capacidades especializadas en estadística y gestión de datos.
- iqvia tiene aproximadamente 15-18% del mercado cro francés en 2025, aprovechando sus análisis de datos integrados y servicios de ensayo clínico en múltiples áreas terapéuticas.
- Labcorp amplió sus operaciones de desarrollo clínico francés en un 20% en 2024, añadiendo sitios de investigación y especialistas en área terapéutica para atender la creciente demanda biotecnológica.
¿Cuáles son los principales conductores, restricciones y oportunidades en el mercado farmacéutico cro?
el principal factor de crecimiento es que las compañías farmacéuticas pasan de la contratación externa selectiva a asociaciones estratégicas donde los cros administran programas de desarrollo completos en lugar de estudios individuales. grandes empresas farmacéuticas ahora adjudican contratos multianuales que abarcan el trabajo preclínico a través de fase iii para áreas terapéuticas específicas, lo que proporciona a los cros visibilidad de los ingresos y les permite invertir en capacidades especializadas como registros de pacientes de enfermedad rara o plataformas biomarcadores oncología. iqvia, syneos health, and parexel have all structured their french operations around these strategic partnerships, dedicating teams to specific sponsor accounts rather than operating as transactional service providers. el impacto financiero es sustancial: los contratos de asociación estratégica suelen durar de tres a cinco años y cubren carteras de desarrollo por valor de cientos de millones de euros, en comparación con los contratos de estudios únicos que duran de 18 a 36 meses.
la restricción más importante es la limitación de la capacidad del sitio de investigadores en áreas terapéuticas de alta demanda. los centros de oncología francés y los especialistas en inmunología se subscriben con protocolos de prueba, lo que crea cuellos de botella de reclutamiento de pacientes que retrasan los plazos de estudio independientemente de la eficacia del cro administra otros aspectos de la ejecución del ensayo. cros no puede simplemente abrir nuevos sitios para resolver este problema porque investigadores calificados requieren años de capacitación y certificación regulatoria. la restricción es particularmente aguda en ensayos de enfermedades raras donde la franquicia podría tener sólo cinco a diez centros con poblaciones de pacientes relevantes, y esos centros ya están comprometidos con múltiples protocolos competidores. Esto obliga a los cros a ampliar los plazos de contratación o ampliarlos a sitios de investigadores menos experimentados, cualquiera de los cuales aumenta los costos y riesgos para estudiar la calidad.
la oportunidad más clara reside en los servicios de evidencia del mundo real que conectan los datos del ensayo clínico a la base de datos de salud nacional de Franco. ansm ahora acepta evidencias reales para apoyar propuestas regulatorias para ciertas indicaciones, y los patrocinadores necesitan cros que pueden diseñar estudios híbridos que combinan la metodología tradicional de ensayo controlado aleatorizada con datos de observación de registros electrónicos de salud. Esto requiere capacidades que la mayoría de los cros no poseen actualmente: científicos de datos que entienden la analítica sanitaria, especialistas regulatorios que saben estructurar las presentaciones de evidencias del mundo real, y establecer relaciones con las autoridades de datos de salud francesas. cros que construyen estas capacidades capturará trabajo de alto nivel que no puede ser fácilmente replicado por los competidores que carecen de la infraestructura técnica y la experiencia regulatoria para ejecutar estos diseños de estudio híbridos.
¿Cuál ha sido el impacto de la inteligencia artificial en el mercado farmacéutico cro france?
Los sistemas de identificación de pacientes impulsados por los ai ahora analizan los registros electrónicos de salud para encontrar candidatos que cumplan criterios específicos de inclusión de ensayos, lo que acelera los plazos de contratación identificando pacientes elegibles antes de que los sitios revisen manualmente los gráficos. iqvia y labcorp han implementado modelos de aprendizaje automático en sistemas de salud francés que marcan pacientes basados en códigos de diagnóstico, valores de laboratorio, historias de medicamentos y otros marcadores clínicos. Estos sistemas reducen el tiempo de detección mediana de semanas a días en sitios con registros electrónicos de salud integrados, aunque la adopción se limita a redes hospitalarias más grandes con datos de pacientes digitalizados. el beneficio operativo es más visible en ensayos de enfermedades raras, donde la revisión manual de la gráfica requería meses de tiempo de investigador para identificar incluso un puñado de pacientes elegibles.
procesamiento de lenguaje natural automatiza el monitoreo de seguridad extrayendo eventos adversos de notas clínicas, informes de laboratorio y diarios de pacientes sin requerir entrada manual de datos por los coordinadores del sitio. syneos health and icon have implemented nlp systems that continuously scan trial documentation for safety signals, flagging potential serious adverse events that require immediate reporting to regulatory authorities. Esta automatización redujo la mediana de tiempo de presentación de eventos adversos de 48 a 72 horas a menos de 24 horas en sitios que utilizan la tecnología, lo que importa cuando los requisitos regulatorios exigen la presentación de eventos adversos graves dentro de las 24 horas de conciencia del investigador. la limitación es que la precisión de la nlp depende de la calidad de la documentación, y las notas clínicas francesas a menudo incluyen terminología médica corta y no estandarizada que reduce la fiabilidad de extracción automatizada.
la barrera principal a la adopción de ai más amplia es la fragmentación de datos entre los proveedores de atención médica franceses. Los registros de pacientes permanecen en los sistemas hospitalarios individuales, las redes regionales de salud y las prácticas privadas, lo que evita que los cros entrenen modelos de ai sobre conjuntos de datos completos que reflejen las poblaciones de pacientes del mundo real. Además, las normas de protección de datos francesas requieren el consentimiento explícito del paciente para el uso secundario de los datos de salud en contextos de investigación, lo que agrega el cumplimiento general que muchos cros encuentran prohibitivo para proyectos de desarrollo de ai. Esto crea una paradoja donde las aplicaciones de ai más valiosas requieren conjuntos de datos grandes y diversos que los marcos regulatorios franceses hacen difícil de reunir legalmente.
principales tendencias del mercado
- Los patrocinadores farmacéuticos pasaron de la compra de servicios transaccionales a asociaciones estratégicas multianuales entre 2022 y 2024, consolidando relaciones entre cro de cinco o seis proveedores a dos o tres proveedores preferidos.
- La adopción de un juicio descentralizado se aceleró en 2023 cuando el ansm publicó la orientación aceptando la vigilancia remota de los pacientes y las visitas de salud en el hogar como alternativas válidas a las evaluaciones basadas en el sitio.
- Las empresas de biotecnología aumentaron la subcontratación de cro de un promedio del 60% de los gastos de desarrollo en 2021 a más del 75% en 2024, impulsado por la presión de capital de riesgo para reducir al mínimo los costos fijos.
- iqvia y syneos salud ampliaron sus especialistas en área terapéutica francesa en 25-30% entre 2023 y 2025, contratando oncología y expertos en enfermedades raras para apoyar contratos de asociación estratégica.
- Los servicios de evidencia del mundo real surgieron como una oferta distinta en 2024, con cros estableciendo equipos dedicados para diseñar estudios híbridos que combinan datos de prueba y registros de salud observacionales.
- Los plazos de contratación de pacientes para los juicios de oncología aumentaron de 12 meses a 16-18 meses entre 2022 y 2024 debido a las limitaciones de capacidad de los investigadores y los protocolos competidores.
- chinese cros entró en el mercado francés en 2024, ofreciendo servicios fase i y fase inicial ii a 20-25% por debajo de los precios titulares para establecer operaciones europeas.
- Los servicios de gestión de datos crecieron más rápido que el monitoreo clínico entre 2023 y 2025, lo que refleja una mayor demanda de patrocinadores para análisis avanzados y visualización de datos en tiempo real durante los ensayos.
frane farmacéutica cro market segmentation
por tipo
Los servicios de investigación clínica dominan el mercado francés cro al 65% de los ingresos totales. Este segmento cubre el reclutamiento de pacientes, el monitoreo del sitio, la recopilación de datos y el soporte regulatorio de sumisión para la fase i a través de ensayos clínicos de fase iv. el dominio refleja un cambio estructural donde los patrocinadores farmacéuticos y biotecnológicos externalizan la gestión de ensayos a los cros en lugar de mantener equipos de operaciones clínicas internas. cros de servicio completo como iqvia, labcorp y syneos la salud funcionan como el brazo de desarrollo clínico del patrocinador, administrando relaciones de investigadores, interacciones regulatorias y supervisión de calidad de datos en varios ensayos simultáneos. la proposición de valor es la transferencia de riesgo: los patrocinadores pagan cros para entregar los pacientes inscritos y limpiar los datos según el calendario, mientras que el cro absorbe la complejidad operativa y la variabilidad del cro.
los servicios de investigación preclínica representan el 22% del mercado, que abarca estudios de toxicología, análisis farmacocinético y desarrollo de formulaciones que ocurren antes de los ensayos humanos. Este segmento sirve a empresas de biotecnología de primera etapa y equipos de descubrimiento farmacéutico que necesitan capacidades especializadas de laboratorio sin construir instalaciones dedicadas. charles river, covance, and eurofins dominan los servicios preclínicos franceses mediante la propiedad de laboratorios certificados de glp equipados para estudios de toxicología regulatoria. el segmento es técnicamente exigente porque los estudios preclínicos deben cumplir normas regulatorias estrictas para la calidad y reproducibilidad de los datos, que requieren métodos analíticos validados y experimentados laboratorio científicos. márgenes son superiores a la investigación clínica porque los costos de conmutación son sustanciales una vez que un patrocinador califica un laboratorio específico para un programa de desarrollo.
servicios de laboratorio y otras ofertas especializadas representan el 13% del mercado. Esto incluye pruebas bioanalíticas, servicios centrales de laboratorio para ensayos clínicos y capacidades de nicho como pruebas de dispositivos médicos o validación de salud digital. el segmento creció más rápido que la investigación clínica básica entre 2023 y 2025 porque los patrocinadores requieren cada vez más servicios integrados que combinan la gestión de ensayos clínicos con análisis de laboratorio especializado. por ejemplo, los ensayos de oncología a menudo necesitan desarrollo de diagnóstico compañero junto con drogas pruebas, que requiere cros que pueden coordinar validación de biomarcadores, recogida de muestras clínicas y desarrollo de ensayos diagnóstico como un programa unificado. cros que ofrecen estos servicios integrados captan mayores ingresos por proyecto que los que proporcionan sólo la gestión de ensayos clínicos.
para aprender más sobre este informe, descargar informe de muestra gratis
por solicitud
Las aplicaciones de desarrollo de drogas conducen a un 41,3% de la demanda de mercado, que abarca el desarrollo de la formulación, las pruebas de estabilidad, el desarrollo de métodos analíticos y los servicios de apoyo a la fabricación. Las empresas farmacéuticas subcontratan estas actividades a los cros cuando las funciones de desarrollo interno carecen de capacidad o conocimientos especializados para retos específicos de formulación. Por ejemplo, el desarrollo de formulaciones estables para los productos biológicos requiere equipo especializado y experiencia que la mayoría de los patrocinadores no mantienen internamente. cros como catalent, patheon y Lonza proporcionan estas capacidades sobre una base contractual, permitiendo a los patrocinadores avanzar a los candidatos mediante el desarrollo sin inversión de capital en laboratorios de formulación. la aplicación es márgen-acretiva porque el trabajo de desarrollo de la formulación es técnicamente complejo y requiere científicos experimentados que ordenan tasas de facturación premium.
Las aplicaciones de ensayos clínicos representan el 38,7% de la demanda, centradas específicamente en la inscripción de pacientes, la gestión del sitio y los servicios de ejecución de ensayos en lugar de un mayor apoyo al desarrollo. este segmento difiere de los servicios de investigación clínica, ya que captura sólo el componente de ejecución del ensayo, excluyendo la estrategia regulatoria, el análisis de datos y las actividades posteriores al juicio. la aplicación creció entre 2022 y 2024, ya que las empresas biotecnológicas buscaban cros que pudieran manejar el reclutamiento de pacientes y el monitoreo de sitios mientras retenían otras actividades de desarrollo internamente. Este desglose permitió a los patrocinadores externalizar los aspectos más complejos y sensibles al tiempo del desarrollo clínico, preservando al mismo tiempo el control sobre decisiones estratégicas como la selección de puntos finales y el diseño de ensayos.
Estudios toxicológicos, gestión de datos y otras aplicaciones juntos representan el 20% del mercado. Los estudios de toxicología son obligatorios para las presentaciones reglamentarias y requieren instalaciones con certificación de glp que la mayoría de los patrocinadores no operan internamente. Los servicios de gestión de datos han aumentado rápidamente a medida que los ensayos generan volúmenes crecientes de datos electrónicos procedentes de dispositivos de desgaste, dispositivos de control remoto y resultados reportados por los pacientes que requieren plataformas de bases de datos especializadas y capacidades de análisis estadístico. cros que invirtió en plataformas de datos basadas en la nube y análisis en tiempo real entre 2020 y 2025 capturó la creciente demanda de patrocinador para monitorización de ensayos transparentes y diseños de ensayos adaptativos que requieren análisis de datos continuos en lugar de bases de datos tradicionales bloqueadas revisadas sólo al finalizar el estudio.
por usuario final
Las empresas farmacéuticas constituyen el 52,8% de la demanda cro en franquicia. grandes empresas farmacéuticas subcontratan programas de desarrollo específicos donde la capacidad interna es limitada o falta experiencia en área terapéutica. por ejemplo, una empresa con fuertes capacidades de oncología podría externalizar el desarrollo de enfermedades raras a cros con registros de pacientes establecidos y redes de investigadores en esas indicaciones. la decisión de subcontratación es económicamente impulsada: mantener operaciones clínicas internas para áreas terapéuticas donde la empresa ejecuta sólo uno o dos ensayos al año es costoso-prohibitivo en comparación con la participación de cros sobre una base de proyecto. Esto crea una demanda estable para los cros en áreas terapéuticas donde el interés patrocinador es sostenido pero las carteras individuales de la empresa son limitadas.
Las empresas biotecnológicas representan el 31,4% del mercado y representan el segmento de crecimiento más rápido del 9,1% de los cagr hasta 2033. estas empresas suelen carecer de capacidades internas de desarrollo clínico y externalizar la mayoría del trabajo de desarrollo de estudios preclínicos a través de ensayos de fase III. el controlador de crecimiento es la dinámica de financiación de capital de riesgo: se espera que las empresas de biotecnología demuestren un progreso clínico rápidamente al minimizar la quemadura de efectivo, lo que hace que la subcontratación a cros sea más atractiva financieramente que la creación de capacidades internas que requieren un contador fijo. cros proporciona a los patrocinadores de biotecnología una capacidad flexible que escala con las necesidades del programa, facturando sólo para proyectos activos en lugar de requerir pagos continuos de los retenedores o personal asalariado.
institutos de investigación y otros usuarios finales contribuyen el 15,8% de la demanda. Centros médicos académicos y organizaciones de investigación gubernamentales se dedican a los exámenes iniciados por investigadores y estudios de salud pública que requieren recopilación y seguimiento de datos de grado regulatorio. Estos clientes suelen operar con financiamiento de donaciones con presupuestos fijos y plazos definidos, lo que requiere que los cros ofrezcan servicios dentro de limitaciones de costes rígidos. el segmento ofrece márgenes más bajos que el trabajo farmacéutico comercial, pero proporciona a los cros acceso a nuevos enfoques terapéuticos y poblaciones de pacientes de enfermedades raras que luego se traducen en oportunidades de desarrollo comercial cuando los descubrimientos académicos avanzan hacia la aprobación y comercialización regulatorias.
por fase
Los ensayos de fase III generan 43,2% de los ingresos de investigación clínica debido a sus grandes poblaciones de pacientes, períodos de monitoreo prolongados y requisitos regulatorios complejos. un ensayo de oncología de fase III típico en franquicia podría inscribir a 300-500 pacientes en 25-40 sitios de investigadores durante tres a cuatro años, lo que requeriría monitoreo del sitio, gestión de datos, reporte de seguridad y coordinación regulatoria durante todo el período de estudio. cros proporciona valor mediante la gestión de esta complejidad operacional, al tiempo que permite a los patrocinadores centrarse en las decisiones estratégicas en torno al diseño de juicios y las propuestas reglamentarias. la concentración de ingresos en la fase iii refleja tanto el costo directo de la ejecución de juicios a gran escala como los patrocinadores de prima de riesgo pagan a los cros para cumplir los plazos de inscripción agresivos que determinan las fechas de lanzamiento del producto.
Los ensayos de fase II contribuyen al 28,6% de los ingresos, centrados en estudios de determinación de dosis y evaluaciones de la eficacia inicial en poblaciones de pacientes más pequeñas. Estos ensayos utilizan cada vez más diseños adaptables que modifican criterios de inscripción o calendarios de dosificación basados en resultados provisionales, lo que requiere cros con sólidas capacidades estadísticas y de gestión de datos. la complejidad técnica de los ensayos adaptativos crea barreras a la entrada para los cros más pequeños que carecen de conocimientos especializados, lo que permite a los proveedores de servicios completos más grandes para ordenar precios premium. fase ii trabajo es estratégicamente importante para los cros porque los patrocinadores que completan exitosamente la fase ii normalmente continúan con el mismo cro en la fase iii, creando tuberías de ingresos plurianuales de compromiso en fase temprana.
fase i, fase IV y otras fases de ensayo juntas representan el 28,2% de los ingresos. Los ensayos de fase i son relativamente pequeños pero técnicamente exigentes, que requieren instalaciones especializadas para estudios de seguridad de primer nivel y monitoreo intensivo de pacientes. estudios de post-marketing fase iv están creciendo a medida que los reguladores requieren cada vez más evidencia real para complementar los datos clínicos pre-aprobación. cros that offer both traditional phase iv trial management and real-world evidence capabilities combination trial data with observational health records are capturing growing sponsor demand for integrated post-marketing surveillance programs that satisfy regulatory requirements while generating evidence for payer recycling negotiations and Clinic guideline development.
¿Cuáles son los casos de uso clave que impulsan el mercado farmacéutico cro de la franja?
la aplicación primaria es la gestión de ensayos de fase III de servicio completo para empresas biotecnológicas que carecen de capacidad de operación clínica interna. Estos patrocinadores comprometen a los cros a manejar todos los aspectos de la ejecución de juicios desde la selección del sitio mediante el bloqueo de bases de datos, la presentación reglamentaria y la vigilancia de la seguridad posterior a la aprobación. un compromiso típico podría implicar una rara indicación de enfermedad donde el patrocinador de biotecnología ha completado los estudios de prueba de contacto de fase ii y necesita un cro para ejecutar el programa de fase III pivotal requerido para la aprobación de ema. el cro proporciona redes de sitios de investigadores, experiencia regulatoria, estrategias de reclutamiento de pacientes y la infraestructura de gestión de datos de forma llave en mano, permitiendo a la empresa de biotecnología avanzar hacia la comercialización sin construir sede de operaciones clínicas permanentes.
demanda adyacente proviene de grandes compañías farmacéuticas que subcontratan programas de desarrollo terapéuticos específicos de área. por ejemplo, una empresa con experiencia en inmunología limitada podría involucrar a un cro para gestionar todo el desarrollo clínico para un activo inmunológico adquirido, aprovechando las relaciones establecidas por el cro con investigadores de reumatología francesa y dermatología. Estas alianzas estratégicas suelen abarcar varios ensayos a lo largo de varios años, proporcionando al cro ingresos predecibles al mismo tiempo que da acceso al patrocinador a los conocimientos de área terapéutica sin una ampliación permanente del personal. la lógica comercial es la especialización: cros que se centran en áreas terapéuticas específicas desarrollan profundas relaciones de investigación y experiencia de diseño de protocolo que los equipos de desarrollo interno generalistas no pueden replicar.
Casos de uso emergentes se centran en diseños de ensayos híbridos que combinan ensayos controlados tradicionalmente aleatorizados con evidencia real de bases de datos de salud francesas. Los patrocinadores comprometen a los cros a diseñar estudios donde el brazo de control utiliza pacientes emparejados de registros electrónicos de salud en lugar de inscribir un cohorte placebo separado, que reduce los costos de ensayo y acelera los plazos de inscripción. iqvia y syneos salud han establecido equipos dedicados para ejecutar estos estudios híbridos, que requieren científicos de datos, epidemiólogos y especialistas reguladores que entienden tanto la metodología de ensayo clínico como los estándares de evidencia del mundo real. la aplicación es técnicamente exigente pero ofrece a los patrocinadores ahorros de costos sustanciales, con algunos diseños híbridos reduciendo los costos de fase III en 30-40% en comparación con los ensayos tradicionales totalmente inscritos.
report metrics | detalles |
valor de tamaño del mercado en 2025 | 1.295,8 millones de dólares |
valor de tamaño del mercado en 2026 | usd 1,392,6 millones |
pronóstico de ingresos en 2033 | usd 2.358,7 millones |
Tasa de crecimiento | de 2026 a 2033 |
año base | 2025 |
datos históricos | 2021 – 2024 |
Ejercicio previsto | 2026 – 2033 |
cobertura de informes | pronóstico de ingresos, paisaje competitivo, factores de crecimiento y tendencias |
alcance regional | Franco |
empresas clave perfiladas | iqvia, labcorp, syneos health, parexel, icono plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat |
alcance de personalización | personalización de los informes libres (de alcance regional). aprovechar las opciones de compra personalizadas para satisfacer sus necesidades de investigación exactas. |
de los informes | por tipo (investigación clínica, investigación preclínica, servicios de laboratorio, otros); por aplicación (desarrollo de drogas, ensayos clínicos, estudios toxicológicos, gestión de datos, otros); por usuario final (empresas de cine, empresas biotecnológicas, institutos de investigación, otros); por fase (fase i, fase ii, fase iii, fase iv, otros) |
¿Qué impulsa el crecimiento en el mercado farmacéutico cro de la franja?
france ofrece tres ventajas estructurales que otros mercados europeos no pueden reproducir a escala equivalente. En primer lugar, el país opera un sistema de salud centralizado con registros electrónicos completos de salud que abarcan a más de 65 millones de ciudadanos, proporcionando a los cros capacidades de identificación de pacientes y acceso a pruebas reales que los sistemas sanitarios fragmentados no pueden coincidir. Segundo, la franquicia mantiene concentraciones densas de investigadores especializados en paris, lion y marseille donde centros médicos académicos, hospitales docentes e institutos de investigación se agrupan en proximidad geográfica, lo que simplifica la logística de los ensayos y reduce los costos de vigilancia en comparación con las redes de sitios geográficamente dispersos. En tercer lugar, el ansma ha establecido plazos predecibles de revisión reglamentaria y directrices claras sobre metodologías de ensayos emergentes como protocolos descentralizados y pruebas reales, lo que reduce la incertidumbre para los patrocinadores de la planificación de programas multianuales de desarrollo.
la dinámica competitiva en franquicia difiere de otros mercados europeos porque los requisitos lingüísticos y regulatorios crean barreras naturales a la entrada para los no-eu cros. protocolos de prueba, documentos de consentimiento informado y presentaciones regulatorias deben estar en francés, lo que requiere personal local dedicado en lugar de equipos europeos centralizados que operan en inglés. Además, las normas de protección de datos francesas imponen requisitos específicos en el manejo de datos de salud que difieren de las disposiciones generales de gdpr, lo que requiere que los cros mantengan programas de cumplimiento específicos de franquicia. Estas barreras protegen a los jugadores establecidos como iqvia, labcorp y syneos de salud que han operado en franquicia durante décadas e invertido en infraestructura local, al tiempo que crean mayores costos de entrada para nuevos competidores que intentan establecer operaciones francesas.
el segmento de demanda de mayor crecimiento es ensayos de enfermedades raras donde la base de datos de salud nacional de franquicia permite la rápida identificación del paciente para indicaciones ultra-raras. en condiciones que afectan a menos de 1.000 pacientes franceses, el reclutamiento tradicional basado en el sitio puede tardar años porque los investigadores deben revisar manualmente los registros médicos para identificar candidatos elegibles. cros que han establecido acuerdos de acceso a datos con las autoridades de salud francesas pueden analizar electrónicamente toda la población nacional de pacientes, identificando pacientes elegibles en semanas en vez de meses. esta capacidad ha hecho de franquicia un lugar preferido para los ensayos europeos de enfermedades raras, con patrocinadores cada vez más eligiendo sitios franceses como países líderes para estudios multinacionales en indicaciones ultra-raras donde la velocidad de identificación de pacientes determina los plazos generales del programa.
¿Quiénes son los actores clave en el mercado farmacéutico cro y cómo compiten?
el mercado cro francés funciona como una estructura de dos niveles. iqvia, labcorp, syneos health, parexel, and icon collectively hold approximately 55-60% market share and compete as full-service providers offering integrated capabilities from preclinical through phase iv. these companies compete on therapeutic area expertise, investigator site networks, and technology platforms that provide sponsors with real-time trial visibility. cros de nivel medio y más pequeño ocupan nichos especializados basados en enfoque terapéutico, tipo de servicio o presencia regional, típicamente asociando con mayores cros en programas complejos en lugar de competir directamente para contratos de servicio completo.
iqvia compite a través de su plataforma de datos integrados y servicios clínicos que combina la gestión de ensayos con capacidades de evidencia en el mundo real. la compañía opera la mayor base de datos de salud comercial de franquicia que cubre los datos de prescripción, los registros de descargas hospitalarias y la información de reclamos, que utiliza para identificación de pacientes, selección de sitios y evaluaciones de viabilidad. iqvia amplió sus operaciones clínicas francesas en un 25% entre 2023 y 2025, añadiendo especialistas en área terapéutica en oncología, enfermedades raras e inmunología para apoyar contratos de asociación estratégica con grandes patrocinadores de pharma. la empresa diferencia las capacidades de análisis, proporcionando a los patrocinadores modelos de inscripción predictiva y análisis comparativos de eficacia que los cros más pequeños no pueden replicar sin activos de datos equivalentes.
Labcorp compite a través de la integración vertical de los servicios de laboratorio y la gestión de ensayos clínicos, permitiendo a la empresa ofrecer a los patrocinadores programas unificados que combinan la ejecución de ensayos con pruebas centrales de laboratorio, análisis de biomarcadores y desarrollo diagnóstico compañero. esta integración importa en ensayos oncología y enfermedad rara donde la selección de pacientes impulsados por biomarcadores y evaluaciones farmacodinámicas requieren coordinación entre sitios clínicos y laboratorios especializados. Labcorp opera laboratorios certificados de glp en franquicia que sirven tanto a patrocinadores de ensayos clínicos como a mercados de diagnóstico de rutina, creando economías de escala que los cros de juego puro no pueden coincidir. la empresa se dirige a patrocinadores de biotecnología que desarrollan candidatos de medicina de precisión donde los servicios clínicos y de laboratorio integrados reducen la coordinación y aceleran los plazos de desarrollo en comparación con la participación de proveedores separados para la gestión de ensayos y pruebas de laboratorio.
recientes acontecimientos
en marzo 2026, iqvia anunció una asociación estratégica con un registro de pacientes de enfermedad rara francesa para proporcionar pruebas genéticas y datos de historia natural para las condiciones neurológicas ultra-raras. la colaboración tiene como objetivo acelerar la identificación de pacientes y evaluaciones de viabilidad de ensayos para patrocinadores desarrollando terapias para condiciones que afectan a menos de 500 pacientes franceses. https://www.iqvia.com (iqvia)
en febrero de 2026, labcorp amplió sus operaciones de laboratorio central francés con nuevas capacidades de prueba de biomarcadores para ensayos de terapia celular y genética. la instalación procesa muestras farmacodinámicas y ensayos de diagnóstico compañero para patrocinadores de terapia avanzada que realizan estudios clínicos franceses. https://www.labcorp.com (labcorp)
¿Qué ideas estratégicas definen el futuro del mercado farmacéutico cro de la franja?
en los próximos cinco a siete años, la ventaja competitiva en el mercado francés cro pasará de las capacidades de ejecución operacional a las plataformas de datos y tecnología que permiten nuevas metodologías de ensayo. el mercado actual premia a los cros que pueden inscribir a los pacientes rápidamente y proporcionar datos limpios a su debido tiempo, pero estas capacidades se están volviendo mercantilizadas como herramientas electrónicas de captura de datos y monitoreo remoto estandarizan en toda la industria. la próxima frontera competitiva es la integración de evidencias en el mundo real, la ejecución de juicios descentralizados y la identificación de pacientes impulsados por los ai, todo lo cual requiere inversiones tecnológicas sustanciales y acuerdos de acceso a datos que crean barreras para la entrada de competidores sin escala.
el riesgo de que las proyecciones del mercado puedan subestimar es un plazo de aceptación reglamentaria para metodologías de ensayo novedosas. ansm ha publicado orientaciones sobre los juicios descentralizados y las pruebas del mundo real, pero el examen reglamentario real de las presentaciones utilizando estos enfoques sigue siendo limitado. si las autoridades reguladoras prueban más conservadoras en la práctica que los documentos de orientación sugieren, los patrocinadores pueden retrasar la adopción de estas metodologías, lo que reduciría la demanda de capacidades cro en estas áreas y favorecería la ejecución tradicional de juicio basado en el sitio donde se establezca un precedente regulador. esto beneficiaría a los cros titulares con redes de sitios fuertes mientras que los nuevos participantes desventajosos que invirtieron fuertemente en plataformas de prueba descentralizadas.
la oportunidad que sigue siendo infravalorada es los servicios de pruebas del mundo real posteriores a la aprobación que combinan la gestión del ensayo de fase iv con estudios de observación utilizando bases de datos de salud francesas. Los beneficiarios necesitan cada vez más datos de eficacia del mundo real para apoyar las decisiones de reembolso, y los patrocinadores necesitan cros que puedan diseñar programas integrados que satisfagan tanto los requisitos reglamentarios de post-marketing como las necesidades de pruebas de los beneficiarios. el segmento es actualmente pequeño pero ofrece márgenes más altos que el trabajo tradicional de fase iv porque requiere capacidades especializadas en economía de salud, epidemiología y análisis de bases de datos que la mayoría de los cros no mantienen. compañías que construyen estas capacidades capturarán creciente demanda de patrocinadores de programas de generación de evidencias que sirven a múltiples interesados en lugar de satisfacer obligaciones regulatorias.
Preguntas frecuentes
Encuentre respuestas rápidas a las preguntas más comunes.
se espera que el mercado farmacéutico cro franquicia alcance 2.358,7 millones de dólares para 2033.
segmentos clave para el mercado farmacéutico cro france son por tipo (investigación clínica, investigación preclínica, servicios de laboratorio, otros); por aplicación (desarrollo de fármacos, ensayos clínicos, estudios toxicológicos, gestión de datos, otros); por usuario final (empresas farmacéuticas, empresas biotecnológicas, institutos de investigación, otros); por fase (fase i, fase ii, fase iii, fase iv, otros).
los principales jugadores de mercado farmacéutica de franjas son iqvia, labcorp, syneos health, parexel, icono plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat.
la franquicia actual farmacéutica cro tamaño del mercado es usd 1,295.8 millones en 2025.
la franquicia farmacéutica cro mercado cagr es 7.82% de 2026 a 2033.
Informes publicados recientemente
-
Apr 2026
Mercado de Cord Blood Banking Services
servicios bancarios de sangre de cordón tamaño del mercado, compartir informe de análisis por tipo de servicio (colección, procesamiento, almacenamiento), por tipo de banco (bancos privados, bancos públicos y bancos híbridos), por componente (sangre de disco, y tejido de cordón), por usuario final (hospitales, instituciones de investigación, empresas de biotecnología y otros) y geografía (norteamérica, europa, asiapacifico, oriente medio y áfrica, sur y centro), 2021 america), 2021
-
Apr 2026
Mercado de ELISA Processors
elisa processors market size, share ' analysis report by type (optical filter elisa analysisr, and óptico grating elisa analysisrs), by mode (automated elisa analysisrs, and semi-automated elisa analysisrs), by applications (inmunology, vaccine development, drug monitoring, and others), by end users (biotechnology companies, pharmaceutical companies, contract research organization, and diagnostic laboratories) and geography (north america, europesia
-
Apr 2026
Mercado de Microscopio escáner de diapositivas
microscopio deslizante tamaño del mercado, informe de análisis de acciones por tipo (escáner de diapositivas de microscopio portátil y escáner de diapositivas de microscopio), por aplicación (investigación biológica, medicina, veterinaria y otros) y geografía (norteamérica, europe, asia-pacifico, medio este y áfrica, sur y centroamericano), 2021 - 2031
-
Apr 2026
Mercado de Microondas Cookware
micrococina tamaño del mercado, compartir " informe de análisis por tipo material (plásico, vidrio, cerámica, silicona y metal), por aplicación (cooking, recalentado y descongelación), por usuario final (lote, comercial (restaurantes, hoteles y cafés), y la industria de servicios alimentarios), por canal de ventas (en línea, venta al por menor sin conexión (supermercados, hipermercados, tiendas especializadas) y ventas directas


