europe Health contract research organization market size & previsión:
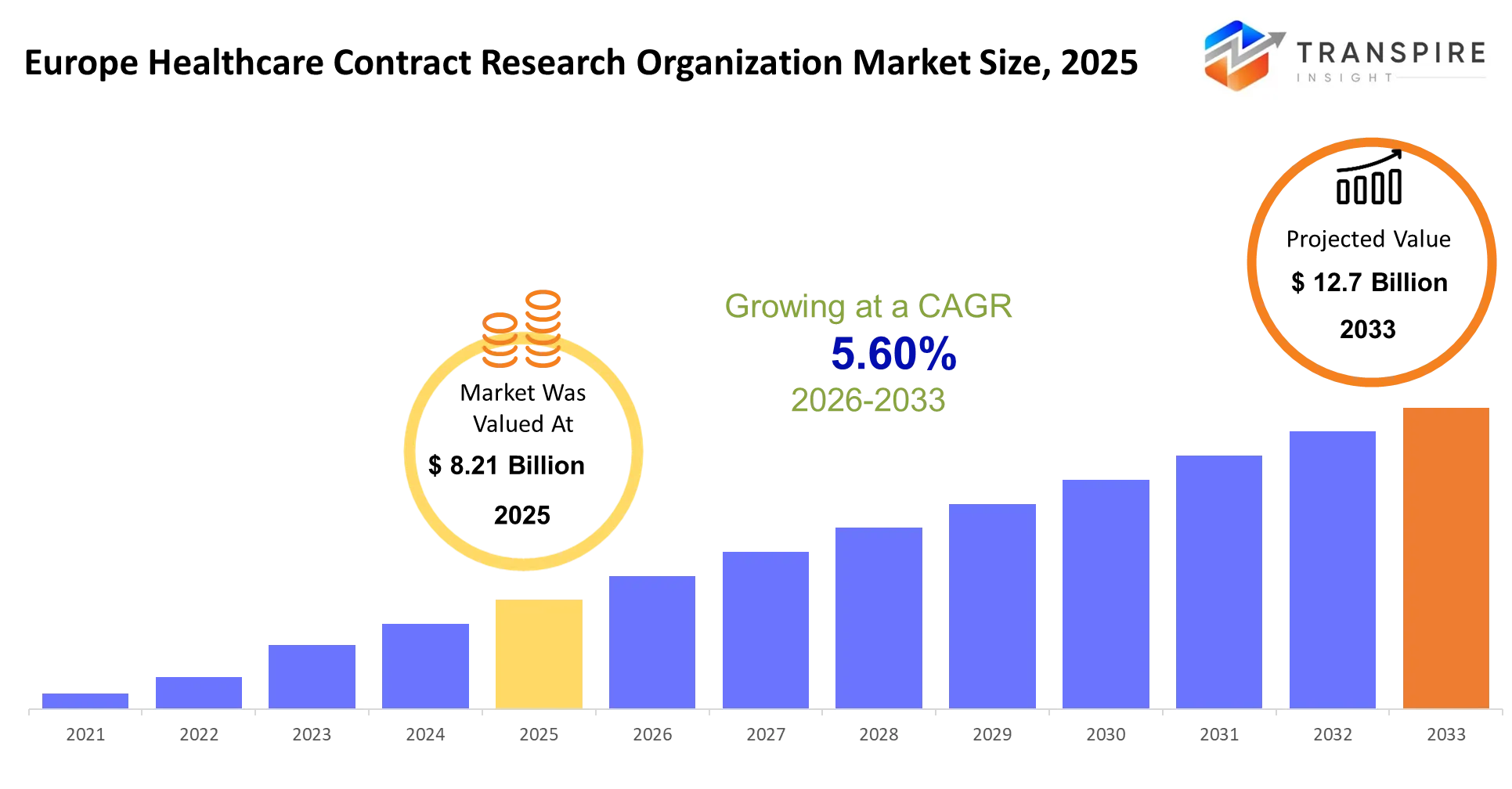
- europe Health contract research organization market size 2025: usd 8.21 billion
- europe Health contract research organization market size 2033: usd 12.7 billion
- europe Health contract research organization market cagr: 5.60%
- segmentos de mercado de la organización de investigación de contratos de salud europe: por tipo (servicios de investigación clínicos, servicios preclínicos, servicios de laboratorio, otros), por aplicación (desarrollo de fármacos, ensayos clínicos, pruebas de dispositivos médicos, servicios regulatorios, otros), por usuario final (empresas de cine, biotecnología, empresas de dispositivos médicos, institutos de investigación, otros), por fase (fase i, fase ii, fase III, fase iv, fase iv, otros)
para aprender más sobre este informe, descargar informe de muestra gratis
Resumen del mercado de la organización de investigación del contrato de salud europe:
el tamaño del mercado de la organización de investigación del contrato de salud de la europa se estima en 8.21 mil millones de dólares en 2025 y se prevé que alcanzará 12.700 millones de dólares en 2033, creciendo en un cagr de 5.60% de 2026 a 2033. Las organizaciones europeas de investigación de contratos de salud funcionan como laboratorios de desarrollo de drogas subcontratados que manejan todos los aspectos de la ejecución de ensayos clínicos para clientes farmacéuticos y biotecnológicos. las organizaciones permiten a los patrocinadores llevar a cabo el desarrollo de la terapia desde pruebas de laboratorio hasta la liberación del mercado proporcionando recursos operacionales esenciales y conocimientos especializados que carecen.
Los modelos de prueba descentralizados e híbridos que utilizan herramientas de monitoreo digital y métodos remotos de compromiso de pacientes se han convertido en el enfoque de investigación principal durante los últimos tres a cinco años. el cambio permite a los equipos de investigación trabajar con más pacientes porque reduce su necesidad de utilizar instalaciones específicas de investigación. la pandemia covid-19 sirvió como catalizador principal porque exigía que los ensayos continuaran a pesar de las restricciones a la circulación y dio lugar a una aceptación más rápida de los métodos virtuales por los organismos reguladores.
el creciente requisito de soluciones rápidas y flexibles ha surgido como el principal impulsor detrás de los patrocinadores que ahora utilizan servicios externos a tasas más altas. la combinación de análisis de datos y pruebas del mundo real y capacidades de prueba adaptativas ha permitido a los cros crear flujos de ingresos escalables de sus complejidades operativas.
información clave del mercado
- países europeos occidentales controlan el mercado europeo de la organización de investigación de contratos de salud porque tienen más del 65% de cuota de mercado que Alemania, el reino unido y la franquicia lideran en 2024.
- europe oriental es la zona más rápida de expansión hasta 2030 debido a su capacidad para realizar ensayos rentables y contratar a los participantes rápidamente y su progreso hacia la adecuación de los requisitos regulatorios sindicales europeos.
- el sector de servicios de ensayo clínico lidera el mercado con una cuota del 70% porque los países europeos eligen subcontratar sus estudios de fase ii y iii.
- la segunda cuota de mercado más grande de la industria pertenece a servicios preclínicos que reciben apoyo de empresas biotecnológicas que desarrollan nuevos productos y sus actividades de investigación y desarrollo en expansión.
- el segmento de la gestión de datos y los servicios de pruebas del mundo real experimentan un crecimiento rápido porque la implementación de los ensayos digitales impulsa la expansión de 2025 a 2030.
- el campo oncológico mantiene la mayor cuota de mercado de aplicaciones que alcanzó el 30% en 2024 porque los investigadores médicos realizan estudios complejos de ensayo y los investigadores del cáncer desarrollan numerosos medicamentos contra el cáncer.
- el desarrollo de la medicina personalizada junto con el apoyo regulatorio para enfermedades raras crea las áreas de tratamiento médico más rápidas que desarrollan terapias específicas.
- Las compañías farmacéuticas controlan alrededor del 60% del mercado porque se asocian con cros para disminuir sus gastos operativos mientras agilizan su proceso de desarrollo de drogas.
- pequeñas y medianas empresas biotecnológicas representan el segmento de usuarios más rápido en desarrollo que ahora depende de soluciones completas de servicios externos para apoyar sus necesidades de crecimiento.
¿Cuáles son los principales impulsores, restricciones y oportunidades en el mercado de la organización de investigación de contratos de salud europe?
el elemento principal que impulsa el crecimiento en el mercado de la organización de investigación de contratos de salud europe se debe al aumento de la contratación externa de trabajos complejos de desarrollo clínico que surgió de los crecientes gastos de investigación y desarrollo que ahora superan los 2.000 millones de dólares por fármaco aprobado. Las empresas farmacéuticas necesitan reducir sus plazos de desarrollo de productos mientras se ocupan de requisitos regulatorios complicados que existen en diversos países europeos. Actualmente las organizaciones ejercen mayores tasas de subcontratación porque sus ensayos clínicos atrasados contienen las dificultades de ejecución más difíciles y de inscripción de pacientes. patrocinadores que gastan más dinero en gastos de prueba externa crean contratos más valiosos que conducen a relaciones de servicio prolongadas con cros.
el sistema regulador europeo sigue dividido entre diferentes regulaciones nacionales a pesar de la existencia de regulaciones ema que controlan las actividades de investigación. cada nación opera sus propios sistemas separados para obtener aprobaciones éticas y gestionar datos de pacientes y hacer cumplir el cumplimiento en las instalaciones de investigación. el modelo operativo existente para las organizaciones de investigación clínica (cros) enfrenta desafíos porque necesitan mantener operaciones estandarizadas que resultan en tiempos de preparación de ensayos más largos y mayores gastos administrativos. el proceso conduce a demoras de estudio que hacen que ciertos mercados menos atractivos, limitando así las oportunidades de ingresos y restringiendo el crecimiento de los modelos de investigación europeos.
el potencial de crecimiento de los ensayos clínicos descentralizados muestra una promesa significativa porque los sistemas de salud digital se vuelven más avanzados en países como Alemania y la región nórdica. Las tecnologías de monitoreo remoto y econsentimiento y captura de datos utilizables hacen posible que más pacientes participen en estudios que conducen a una inscripción de estudio más rápida.
¿Qué impacto ha tenido la inteligencia artificial en el mercado de la organización de investigación de contratos de salud europe?
Las organizaciones europeas de investigación contractual utilizan ahora inteligencia artificial junto con herramientas digitales avanzadas para transformar su proceso de diseño de ensayos clínicos mediante la ejecución automatizada de tareas operacionales esenciales. Los sistemas ai-powered utilizan ahora el procesamiento del lenguaje natural junto con la automatización del proceso robótico para ejecutar el proceso de identificación del paciente y las evaluaciones de viabilidad del sitio y tareas de limpieza de datos. el sistema establece un proceso de configuración y monitoreo de ensayos que requiere menos trabajo manual para lograr entre un 20% y un 20% de ahorro de tiempo, al tiempo que produce resultados de datos más precisos a través de estudios multinacionales. Las capas de control digital permiten a las organizaciones supervisar el cumplimiento porque verifican continuamente los datos de prueba contra el cambio de normas reglamentarias.
los modelos de aprendizaje automático añaden capacidades predictivas que impactan directamente el rendimiento de prueba. Los patrocinadores y cros utilizan algoritmos para prever las tasas de reclutamiento de pacientes, predecir los riesgos de deserción y optimizar la selección del sitio basado en conjuntos de datos históricos y reales. el proceso resulta en una mejor eficiencia de inscripción que disminuye costosos retrasos, con algunos estudios que reportan 15-25% ciclos de reclutamiento más rápidos. ai apoya los diseños de ensayo adaptables simulando cambios de protocolo antes de la implementación, lo que mejora la toma de decisiones en condiciones inciertas.
las tecnologías permiten a las organizaciones lograr mejores resultados operacionales mediante tres principales beneficios que incluyen tasas de éxito de los juicios más altas, menos enmiendas de protocolo y reducir los gastos totales de desarrollo. el proceso enfrenta retos de implementación porque los ecosistemas de datos siguen siendo fragmentados y los costos de integración siguen siendo altos, especialmente para unificar los sistemas clínicos tradicionales en diversos marcos regulatorios europeos.
principales tendencias del mercado
- el campo de ensayos descentralizados e híbridos experimentó un rápido crecimiento desde 2020 porque más del 40% de los estudios europeos de investigación adoptaron métodos de prueba remota para continuar sus operaciones durante las limitaciones de viaje.
- la industria farmacéutica ha incrementado sus actividades externas del 45 por ciento en 2018 a más del 55 por ciento en 2024, lo que indica que la industria ahora prefiere subcontratar su trabajo de investigación clínica a socios externos.
- europe oriental se convirtió en la ubicación más popular para los ensayos clínicos después de 2021 porque los procesos de reclutamiento de pacientes en esta región requerían entre 15 y 20 por ciento menos tiempo que en los mercados europeos occidentales.
- el período de 2019 a 2024 trajo mayor complejidad a los ensayos oncológicos que dieron lugar a organizaciones de investigación clínica que necesitan soluciones completas de servicio para sus pruebas de biomarcadores y necesidades flexibles de desarrollo de ensayos.
- Las empresas biotecnológicas que operan a escala media comenzaron a establecer alianzas estratégicas con los cros después de 2020 porque este enfoque les permitió disminuir su necesidad de capacidad operacional interna a la vez que acelerar sus primeros juicios en humanos.
- la pandemia covid-19 creó nuevas normas reglamentarias que permitían a los organismos utilizar el control remoto y el econsentimiento, cambiando así las normas de cumplimiento en toda Europa.
- La integración de pruebas en el mundo real se aceleró después de 2022 cuando los patrocinadores utilizaron datos externos para respaldar sus aplicaciones reglamentarias y trabajos de investigación post-mercado.
- cros transformó su modelo de negocio de ser proveedores de servicios para convertirse en socios de desarrollo estratégico mediante la inversión en tecnologías de salud digital y capacidades de red de sitios.
segmento del mercado de la organización de investigación del contrato de salud europe
por tipo
la categoría principal de servicios de investigación clínica mantiene el liderazgo del mercado porque las empresas subcontratan sus complejas operaciones de ensayo que requieren especialización, especialmente durante los ensayos atrasados que implican el máximo gasto y el escrutinio regulatorio. Los servicios preclínicos mantienen una cuota estable porque las empresas europeas de biotecnología amplían sus actividades de investigación en fase temprana, mientras que los servicios de laboratorio experimentan un crecimiento continuo debido al aumento de los requisitos para las pruebas de biomarcadores y los servicios de diagnóstico centralizados. Los patrocinadores prefieren ahora soluciones completas de servicios porque consideran que los modelos de servicios integrados son más eficaces que utilizar múltiples asociaciones de proveedores separados.
cros que ofrecen servicios clínicos combinados con análisis avanzados de datos y capacidades de evidencia del mundo real experimentan actualmente la mayor demanda según las tendencias del mercado. el próximo período de crecimiento requerirá que los proveedores desarrollen paquetes de herramientas digitales que puedan combinar con sus servicios existentes para crear contratos más valiosos manteniendo al mismo tiempo la eficiencia operativa en varias fases de ensayos clínicos.
para aprender más sobre este informe, descargar informe de muestra gratis
por aplicación
ensayos clínicos constituyen la mayor parte de la investigación a través de su financiación en curso que apoya drogas tuberías de desarrollo y estudios multinacionales de investigación basados en la europa que necesitan una ejecución compleja. el sector de los servicios de desarrollo de drogas mantiene su posición porque los grupos de biotecnología experimentan un aumento de la financiación del capital de riesgo que apoya su labor de investigación en etapas tempranas. la regulación de dispositivos médicos de eu ahora requiere más procedimientos de cumplimiento de trabajo y pruebas que ha llevado a aumentar la demanda de servicios de pruebas de dispositivos médicos.
Los patrocinadores buscan ahora servicios regulatorios porque necesitan ayuda para navegar por múltiples procesos de aprobación que existen en sus operaciones comerciales. el campo de la investigación muestra un enfoque creciente en medicina de precisión y estudios de enfermedades raras que demandan métodos de ensayo clínico distintos y técnicas específicas para seleccionar a los participantes de la investigación. La evolución futura dará lugar a que los cros y patrocinadores trabajen juntos más estrechamente mediante la gestión adaptativa de los requisitos reglamentarios y las pruebas de prueba que utilicen técnicas basadas en datos para procesos de aprobación de ensayos más rápidos.
por usuario final
el mercado de usuarios finales apoya a las empresas farmacéuticas porque sus amplios programas de investigación clínica y necesidades en curso para minimizar los gastos operativos. Las empresas biotecnológicas representan el grupo de mayor crecimiento, que depende de la subcontratación porque carecen de suficientes capacidades internas y necesitan procesos de desarrollo adaptables. Las empresas de dispositivos médicos mantienen una demanda continua debido a requisitos de cumplimiento más estrictos, mientras que las instituciones de investigación promueven el conocimiento a través de sus proyectos de investigación académicos y financiados por el gobierno.
los diferentes grupos presentan patrones únicos de participación porque las empresas farmacéuticas prefieren establecer asociaciones permanentes mientras que las empresas biotecnológicas necesitan desarrollar operaciones que puedan expandirse rápidamente. la futura dirección de investigación establecerá conexiones más fuertes entre las capacidades cro y el tamaño de la organización patrocinadora porque paquetes de servicios personalizados y acuerdos de participación en el riesgo determinarán la competencia del mercado y los métodos de retención de clientes.
por fase
las tres fases de prueba establecen la fase III como la principal fuente de ingresos para los cros debido a su gran tamaño y operaciones costosas y su función vital en la obtención de la aprobación reglamentaria. la creciente necesidad de estudios de prueba de conceptos y de optimización de dosis permite que los estudios de fase ii mantengan su cuota de mercado sustancial. el número de ensayos de fase i sigue aumentando porque más empresas de biotecnología crean nuevos productos y realizan sus pruebas humanas iniciales. la demanda de servicios de fase iv aumenta porque las empresas deben realizar vigilancia post-marketing bajo nuevas normas de vigilancia de la seguridad.
las pautas de demanda muestran que las pruebas de fase posterior necesitan servicios más complejos que conducen a empresas subcontratando su trabajo y buscando conocimientos especializados. el futuro traerá nuevos diseños de ensayo adaptativo junto con métodos descentralizados que cambiarán cómo los ensayos clínicos distribuyen sus fases mientras buscan maneras más rápidas de completar todas las fases de prueba y mejorar su rendimiento operativo.
¿Cuáles son los casos clave de uso que impulsan el mercado de la organización de investigación de contratos de salud europe?
la aplicación primaria de los centros de ensayos clínicos en su ejecución porque las grandes compañías farmacéuticas operan la fase ii y iii multipaís según los requisitos regulatorios europeos. el requisito más exigente surge de este caso de uso porque implica actividades operacionales entre múltiples jurisdicciones que incluyen el reclutamiento de pacientes y la gestión del sitio y las necesidades de cumplimiento.
la empresa ha desarrollado sus capacidades para apoyar las pruebas de dispositivos médicos de acuerdo con la regulación de dispositivos médicos eu y proporcionar servicios de consultoría regulatoria para empresas biotecnológicas que entran en ensayos de primera en humanos. las pequeñas y medianas empresas de biotecnología ahora recurren a los cros para dos propósitos, que incluyen encontrar sus vías de aprobación y lograr un crecimiento eficiente durante su proceso de desarrollo en etapas tempranas.
los casos de uso emergente de ensayos descentralizados implican la aplicación de herramientas de monitoreo remoto, mientras que los estudios de evidencia del mundo real funcionan como métodos para la vigilancia posterior al mercado. los modelos se han vuelto más populares porque los reguladores han comenzado a aceptar puntos finales digitales, mientras que los patrocinadores ahora buscan un acceso más rápido a datos sustanciales mediante métodos avanzados de investigación clínica.
report metrics | detalles |
valor de tamaño del mercado en 2025 | usd 8.21 mil millones |
valor de tamaño del mercado en 2026 | usd 8.67 billion |
pronóstico de ingresos en 2033 | usd 12.700 millones |
Tasa de crecimiento | cagr de 5.60% de 2026 a 2033 |
año base | 2025 |
datos históricos | 2021 - 2024 |
Ejercicio previsto | 2026 - 2033 |
cobertura de informes | pronóstico de ingresos, paisaje competitivo, factores de crecimiento y tendencias |
alcance regional | europe (germanía, reino unido, franquicia, italia, españa y resto de europe) |
empresa clave perfilada | iqvia, labcorp, parexel, icon, syneos health, charles river, medpace, ppd, covance, wuxi apptec, pra health sciences, sgs, eurofins, envigo, clinipace |
alcance de personalización | personalización de los informes libres (papel de país, región " ). aprovechar las opciones de compra personalizadas para satisfacer sus necesidades de investigación exactas. |
de los informes | por tipo (servicios de investigación clínicos, servicios preclínicos, servicios de laboratorio, otros), por aplicación (desarrollo de fármacos, ensayos clínicos, pruebas de dispositivos médicos, servicios regulatorios, otros), por usuario final (empresas de cine, empresas de biotecnología, empresas de dispositivos médicos, institutos de investigación, otros), por fase (fase i, fase ii, fase iii, fase iv, otros)) |
¿Qué regiones están impulsando el crecimiento del mercado de la organización de investigación del contrato de salud europe?
Europa occidental controla el mercado de la organización de investigación de contratos de salud europe porque su sistema regulatorio funciona a través de la agencia europea de medicamentos y sus instalaciones de investigación clínica funcionan a niveles avanzados. los países de la franja alemana y el reino unido mantienen extensas redes de sitios de prueba y hospitales académicos junto con investigadores cualificados. el sistema establecido que incluye la sede farmacéutica y biotecnología clusters así como plataformas de salud digital mantiene una demanda continua de externalización. la combinación de sistemas robustos de protección de datos y redes avanzadas de salud permite a las organizaciones realizar ensayos clínicos internacionales complejos que requieren la participación de numerosos países.
La europa norte funciona como una región confiable que sueñe el uso denmark y finland para priorizar la integración del registro de pacientes y el control de calidad de los datos. esta región difiere de la Europa occidental a través de su enfoque en ensayos más pequeños pero altamente eficientes apoyados por bases de datos nacionales de salud y sistemas digitales unificados. los cros experimentan condiciones operacionales estables debido al cumplimiento reglamentario regular y las iniciativas de desarrollo de la investigación patrocinadas por el Gobierno. el sistema mantiene el crecimiento a través del acceso transparente a los datos de los pacientes y la alta participación en la salud pública que permite el desarrollo sin los requisitos operativos fundamentales que necesitan otros sistemas.
europe oriental demuestra su velocidad de desarrollo más rápida a través de sus recientes inversiones en infraestructura clínica junto con su cumplimiento a los estándares regulatorios europeos. los países de pólago y romania han mejorado las capacidades del sitio y han reducido los plazos de aprobación desde 2020. Los patrocinadores mundiales han optado por trabajar en la ejecución de los juicios porque la combinación de costos operacionales más bajos y un reclutamiento más rápido de pacientes aumenta la eficiencia. el impulso actual crea múltiples puntos de entrada para cros e inversores que quieren crear capacidad mientras capturan la nueva demanda de mercado entre 2026 y 2033.
¿Quiénes son los actores clave en el mercado de la organización de investigación de contratos de salud europe y cómo compiten?
la organización de investigación de contratos de salud europe experimenta competencia de mercado que existe entre dos tendencias opuestas del mercado de consolidación y especialización. global cros mantiene su liderazgo de mercado con sus vastas operaciones y ofertas de servicios completas y sus relaciones establecidas con las compañías farmacéuticas mientras que las empresas de tamaño mediano y nicho utilizan sus conocimientos terapéuticos específicos y conocimientos regionales para competir. Ahora las empresas compiten a través de servicios basados en tecnología que ofrezcan mejores resultados que sus métodos basados en costos anteriores porque la integración de datos y los sistemas de prueba descentralizados y los métodos de ejecución rápida determinan su capacidad de ganar contratos. la plataforma digital y la expansión completa de los servicios mantienen cuota de mercado para las empresas establecidas, mientras que los recién llegados perturban los mercados que se centran en las enfermedades raras y los ensayos en etapas tempranas mediante sus operaciones flexibles y conocimientos especializados.
las avanzadas plataformas de análisis y datos del mundo real desarrolladas por iqvia proporcionan a los patrocinadores las herramientas que necesitan para crear ensayos predictivos adaptativos. organizaciones que invierten en ideas impulsadas por los ai y desarrollan asociaciones con organizaciones de salud aumentan su capacidad de acceder a los datos, lo que conduce a mejores resultados de juicio. icono plc proporciona soluciones de servicio completas que conectan el desarrollo clínico con la inteligencia sanitaria, a través de sus múltiples adquisiciones, para obtener un mejor control sobre los horarios de proyectos y los gastos operativos. parexel ayuda a los patrocinadores a navegar por los requisitos regulatorios europeos a través de sus servicios de consultoría especializados y asistencia para la ejecución.
la organización de desarrollo de fármacos labcorp utiliza sus instalaciones de laboratorio para vincular las pruebas de diagnóstico con las operaciones de ensayo clínico, lo que permite un mejor diseño de estudios basados en biomarcadores y la agrupación de pacientes. syneos health proporciona un modelo de negocio integral que conecta sus servicios para el desarrollo clínico con el acceso al mercado, a través de un sistema único, que proporciona soluciones de ejecución de ensayos sin problemas y de entrada de mercado.
lista de empresas
- iqvia
- Labcorp
- parexel
- icono
- sineos de salud
- charles river
- medpace
- ppd
- covance
- wuxi apptec
- pra health sciences
- sgs
- eurofinas
- envigo
- clinipace
noticias recientes sobre desarrollo
en octubre 2025, la pesca termo expande los servicios de ensayo clínico a través de la integración de la adquisición clario: thermo fisher está progresando activamente en su adquisición de holdings clario, fortaleciendo sus datos de ensayo clínico europeo y la huella de los servicios de análisis. clario se especializa en captura y gestión de datos de ensayos clínicos — infraestructura básica utilizada por cros a través de europe para ensayos atrasados. se espera que el acuerdo cierre a principios de 2026.
fuente: https://www.reuters.com
en abril 2026, termo pescador para el negocio de microbiología de buceo a astorg: thermo fisher scientific has agreed to sell its microbiology business to european private equity firm astorg en un acuerdo de ~$1.075 mil millones. la unidad soporta flujos de trabajo de pruebas clínicas y farmacéuticas, que están estrechamente vinculados a servicios de laboratorio cro-enable en europe. el movimiento refleja la continua consolidación de capacidades de apoyo clínico subcontratados en la región.
fuente: https://www.wsj.com
¿Qué ideas estratégicas definen el futuro del mercado de la organización de investigación de contratos de salud europe?
el mercado de la organización de investigación de contratos de salud de la europa está siguiendo un cambio estructural hacia sistemas basados en plataformas que utilizan infraestructura digital y datos del mundo real y ejecución de pruebas descentralizada para crear ventajas competitivas. el impulsor fundamental detrás de este movimiento requiere que las organizaciones acortan sus tiempos de desarrollo mientras desarrollan terapias complejas que requieren grandes cantidades de datos para crear tratamientos como los biológicos y la medicina personalizada. el mercado avanzará hacia la colaboración estratégica a medida que las organizaciones desarrollen sus capacidades para servir como socios completos de datos y ejecución que les ayuden a obtener más financiación de los patrocinadores.
el peligro oculto de la fragmentación de datos junto con diferentes regulaciones sobre el uso de datos de los pacientes crea un peligro que los modelos de prueba impulsados por los ai lucharán por operar en varios países. Esta limitación creará obstáculos para los esfuerzos internacionales de normalización que disminuyan los beneficios de eficiencia que las organizaciones esperan lograr mediante sus iniciativas de transformación digital.
europe oriental presenta una oportunidad emergente para la expansión de los ensayos híbridos porque su infraestructura de desarrollo y su marco regulatorio facilitan el reclutamiento de pacientes que pueden ampliarse. Los participantes en el mercado deben desarrollar plataformas digitales que permitan la interoperabilidad del sistema junto con el establecimiento de redes de sitios regionales para alcanzar sus objetivos de mantener el acceso a los datos y garantizar el cumplimiento reglamentario y la flexibilidad operacional.
Serie de informes del mercado de la organización de investigación del contrato de salud europe
por tipo
- Servicios de investigación clínica
- servicios preclínicos
- servicios de laboratorio
- otros
por solicitud
- desarrollo de las drogas
- ensayos clínicos
- pruebas de dispositivo médico
- servicios reglamentarios
- otros
por usuario final
- farmacéuticas
- biotecnológicas
- compañías de dispositivos médicos
- institutos de investigación
- otros
por fase
- fase i
- fase ii
- fase iii
- fase iv
- otros
Preguntas frecuentes
Encuentre respuestas rápidas a las preguntas más comunes.
el tamaño del mercado de la organización de investigación del contrato de salud europe aproximado para el mercado será usd 12.700 millones en 2033.
los segmentos clave del mercado de la organización de investigación del contrato de salud de la europa son por tipo (servicios de investigación clínicos, servicios preclínicos, servicios de laboratorio, otros), por aplicación (desarrollo de fármacos, ensayos clínicos, pruebas de dispositivos médicos, servicios regulatorios, otros), por usuario final (empresas de cine, empresas de biotecnología, empresas de dispositivos médicos, institutos de investigación, otros), por fase (fase i, fase ii, fase iii, fase iii, fase iv, fase).
los principales jugadores en el mercado de la organización de investigación del contrato de salud europe son iqvia, labcorp, parexel, icono, syneos health, charles river, medpace, ppd, covance, wuxi apptec, pra health sciences, sgs, eurofins, envigo, clinipace.
el actual tamaño de mercado del mercado de la organización de investigación de contratos de salud europe es usd 8.21 mil millones en 2025.
el mercado de la organización de investigación del contrato de salud europe es 5.60%.
- iqvia
- Labcorp
- parexel
- icono
- sineos de salud
- charles river
- medpace
- ppd
- covance
- wuxi apptec
- pra health sciences
- sgs
- eurofinas
- envigo
- clinipace
Informes publicados recientemente
-
Apr 2026
Mercado de Cord Blood Banking Services
servicios bancarios de sangre de cordón tamaño del mercado, compartir informe de análisis por tipo de servicio (colección, procesamiento, almacenamiento), por tipo de banco (bancos privados, bancos públicos y bancos híbridos), por componente (sangre de disco, y tejido de cordón), por usuario final (hospitales, instituciones de investigación, empresas de biotecnología y otros) y geografía (norteamérica, europa, asiapacifico, oriente medio y áfrica, sur y centro), 2021 america), 2021
-
Apr 2026
Mercado de ELISA Processors
elisa processors market size, share ' analysis report by type (optical filter elisa analysisr, and óptico grating elisa analysisrs), by mode (automated elisa analysisrs, and semi-automated elisa analysisrs), by applications (inmunology, vaccine development, drug monitoring, and others), by end users (biotechnology companies, pharmaceutical companies, contract research organization, and diagnostic laboratories) and geography (north america, europesia
-
Apr 2026
Mercado de Microscopio escáner de diapositivas
microscopio deslizante tamaño del mercado, informe de análisis de acciones por tipo (escáner de diapositivas de microscopio portátil y escáner de diapositivas de microscopio), por aplicación (investigación biológica, medicina, veterinaria y otros) y geografía (norteamérica, europe, asia-pacifico, medio este y áfrica, sur y centroamericano), 2021 - 2031
-
Apr 2026
Mercado de Microondas Cookware
micrococina tamaño del mercado, compartir " informe de análisis por tipo material (plásico, vidrio, cerámica, silicona y metal), por aplicación (cooking, recalentado y descongelación), por usuario final (lote, comercial (restaurantes, hoteles y cafés), y la industria de servicios alimentarios), por canal de ventas (en línea, venta al por menor sin conexión (supermercados, hipermercados, tiendas especializadas) y ventas directas


