Franchise Pharma cro Marktgröße & Wettervorhersage
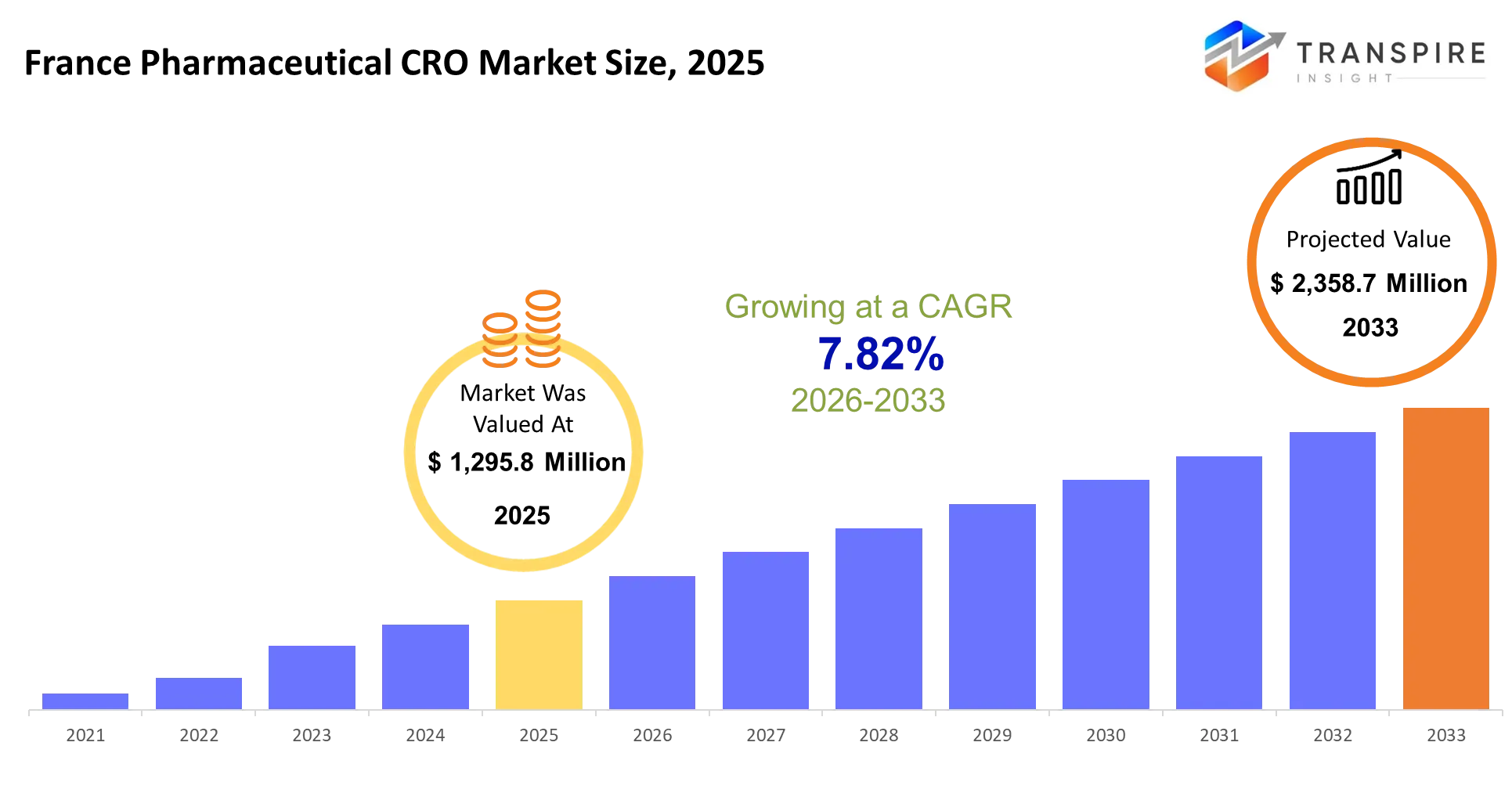
- france pharmazeutisch cro market size 2025: usd 1,295.8 million
- france Pharmaceutical cro market size 2033: usd 2.358.7 million
- Franchise Pharma Cro Markt cagr: 7,82%
- France Pharma cro Marktsegmente: nach Typ (klinische Forschung, präklinische Forschung, Labordienstleistungen, andere); durch Anwendung (Drogenentwicklung, klinische Studien, Toxikologiestudien, Datenmanagement, andere); durch Endverbraucher (Apotheken, Biotech-Unternehmen, Forschungsinstitute, andere); durch Phase (Phase i, Phase ii, Phase iii, Phase iv, andere)
mehr über diesen Bericht erfahren, kostenlos herunterladen
Franchise Pharma Cro Markt Zusammenfassung
Der France Pharma-Kro-Markt wurde 2025 auf uns 1,295,8 Millionen geschätzt. Es wird voraussichtlich bis 2033 2,358,7 Millionen erreichen, was bei einem cagr von 7,82% wächst. Forschungsorganisationen bieten außergelagerte Forschungsdienstleistungen für Pharma- und Biotechnologie-Unternehmen an, die alles von präklinischen Studien bis zur Phase iv postmarket Überwachung verarbeiten. Die klinischen Forschungsleistungen machen 65% des französischen Marktes aus, da Sponsoren es vorziehen, komplexes Testmanagement auf spezialisierte Anbieter zu übertragen, anstatt hausinterne Fähigkeiten in mehreren therapeutischen Bereichen und regulatorischen Zuständigkeiten zu erhalten.
drei regulatorische Veränderungen zwischen 2020 und 2025 neu gestaltet, wie französisch cros arbeiten. Erstens führte die eu-Klinische Studienverordnung harmonisierte Zulassungsverfahren in den Mitgliedsstaaten ein, die die Variabilität der Zeitleiste verringerten, aber die Anforderungen an die Dokumentation an die Front erhöht. Zweitens eröffnete die nationale Gesundheitsdatenplattform von France den Zugang zu realen Beweisdatensätzen, die Sponsoren jetzt mit klinischen Testergebnissen verknüpfen können, wodurch die Nachfrage nach Cros mit bioinformatischen Fähigkeiten entsteht. Drittens begann Ansm, dezentrale Testprotokolle zu akzeptieren, die eine Remote-Patienten-Überwachung erlauben, die die Ermittler-Site-Auswahl weg von traditionellen Krankenhausnetzen zu Heim-Gesundheits-Anbietern und Telemedizin-Plattformen verschoben.
Die aktuelle Markterweiterung wird von Biotech-Unternehmen getrieben, die die in der letzten Phase bearbeiteten Entwicklungsarbeiten extern durchführen. kleine und mittlere Biotech-Firmen fehlen dem regulatorischen Know-how, um Ema-Einreichungen und das Website-Netzwerk zu navigieren, um Multi-Land-Phase iii-Tests effizient durchzuführen. cros bieten diesen Unternehmen Zugang zu etablierten Ermittlerbeziehungen, therapeutischen Bereichsexpertise und regulatorischen Angelegenheiten Spezialisten auf Projektbasis und nicht als permanente Headcount. Dieses Geschäftsmodell ermöglicht es Biotech-Sponsoren, Bargeld zu erhalten, während die Entwicklungszeitlinien beschleunigt werden, was wichtig ist, wenn Risikofinanzierungszyklen alle 18 bis 24 Monate einen nachweisbaren klinischen Fortschritt erfordern.
Schlüssel France Pharma cro Markt Einsichten
- Die klinischen Forschungsleistungen dominieren den Franchise-Parfümmarkt mit einem Anteil von 65 % im Jahr 2024, der durch eine zunehmende Externalisierung von Phase ii und Phase iii-Studienmanagement angetrieben wird.
- Präklinische Forschungsleistungen machen 2024 22% des Marktes aus und unterstützen in der Frühphase Drogenkandidaten, die Toxikologietests und pharmakokinetische Studien erfordern.
- Die Anwendungen für die Arzneimittelentwicklung stellen im Jahr 2024 41,3 % des Cro-Service-Anforderungen dar, da Pharmaunternehmen die Formulierungsentwicklung und die Stabilitätsprüfung auslagern.
- klinische Studien Anwendungen halten 38,7% Marktanteil in 2024, konzentriert sich auf Onkologie, Immunologie und seltene Krankheiten therapeutische Bereiche, wo Patientenrekrutierung ist herausfordernd.
- Pharmaunternehmen stellen im Jahr 2024 52,8% der Endverbrauchernachfrage dar, die nicht-Kern-Klinik-Entwicklungsaktivitäten auslagern, um interne Ressourcen auf Entdeckung und Kommerzialisierung zu konzentrieren.
- Biotech-Firmen machen im Jahr 2024 31,4 % des Marktes aus und stellen das am schnellsten wachsende Endverbrauchersegment dar, das sich bis 2033 um 9,1 % weiter ausdehnt.
- Phase iii-Studien erzeugen 43,2% der klinischen Forschungseinnahmen im Jahr 2024, erfordern große Patientenpopulationen und erweiterte Überwachungsperioden, die Full-Service Cros begünstigen.
- Phase ii-Studien tragen im Jahr 2024 28,6% des Umsatzes bei, wobei die Nachfrage nach adaptiven Test-Designs, die spezialisierte statistische und Datenmanagement-Funktionen erfordern, zunimmt.
- iqvia hält im Jahr 2025 ca. 15-18% des französischen Cro-Marktes und nutzt seine integrierten Datenanalyse- und klinischen Testdienste in mehreren therapeutischen Bereichen.
- Labcorp erweiterte seine französisch klinischen Entwicklungsoperationen um 20% in 2024, fügte Ermittlerstandorte und therapeutische Bereich Spezialisten zur wachsenden Biotech-Anforderung hinzu.
Was sind die wichtigsten Treiber, Einschränkungen und Möglichkeiten im France Pharma-Kro-Markt?
der primäre Wachstumstreiber ist Pharmaunternehmen, die sich vom selektiven Outsourcing zu strategischen Partnerschaften bewegen, in denen cros ganze Entwicklungsprogramme verwalten und nicht einzelne Studien. Großapotheken vergeben jetzt mehrjährige Verträge über präklinische durch Phase iii Arbeit für bestimmte therapeutische Bereiche, die Cros mit Umsatzsicht bietet und ermöglicht es ihnen, in spezialisierte Fähigkeiten wie seltene Patientenregistrierungen oder Onkologie Biomarker-Plattformen zu investieren. iqvia, syneos health und parexel haben alle ihre französischen Operationen um diese strategischen Partnerschaften strukturiert, Teams auf spezifische Sponsorkonten zu widmen, anstatt als Transaktionsdienstleister zu arbeiten. Die finanziellen Auswirkungen sind beträchtlich: strategische Partnerschaftsverträge laufen in der Regel drei bis fünf Jahre und decken Entwicklungsportfolios im Wert von Hunderten von Millionen Euro im Vergleich zu Einzelstudienverträgen, die 18 bis 36 Monate dauern.
die bedeutendste Zurückhaltung ist der Ermittler Standort Kapazität Einschränkungen in High-Demand-Therapiebereichen. french Onkologie-Zentren und Immunologie-Spezialisten werden mit Testprotokollen überschrieben, wodurch Patientenrekrutierungsengpässe entstehen, die Zeitlinien verzögern, unabhängig davon, wie effizient der Cro andere Aspekte der Testausführung verwaltet. Cros kann nicht einfach neue Standorte öffnen, um dieses Problem zu lösen, weil qualifizierte Ermittler jahrelange Ausbildung und Regulierungszertifizierung erfordern. die Strenge ist besonders akut bei seltenen Krankheitsstudien, bei denen France nur fünf bis zehn Zentren mit relevanten Patientenpopulationen haben könnte, und diese Zentren sind bereits mehreren konkurrierenden Protokollen verpflichtet. dies zwingt, die Rekrutierungsfristen zu verlängern oder sich in weniger erfahrene Untersuchungsstellen auszudehnen, von denen entweder Kosten und Risiken für das Studium der Qualität erhöht werden.
Die deutlichste Gelegenheit besteht in realen Beweisen, die klinische Studiendaten mit der nationalen Gesundheitsdatenbank von France verbinden. Ansm akzeptiert jetzt reale Beweise, um regulatorische Eingaben für bestimmte Indikationen zu unterstützen, und Sponsoren benötigen Cros, die Hybrid-Studien erstellen können, die traditionelle randomisierte Testmethode mit Beobachtungsdaten aus elektronischen Gesundheitsdaten kombinieren. Dies erfordert Fähigkeiten, die die meisten Cros derzeit nicht besitzen: Datenwissenschaftler, die Healthcare-Analysen verstehen, regulatorische Spezialisten, die wissen, wie man reale Beweise Vorlagen zu strukturieren, und etablierte Beziehungen mit französischen Gesundheitsdatenbehörden. Cros, die diese Fähigkeiten aufbauen, werden hochmargige Arbeit erfassen, die nicht leicht von Konkurrenten repliziert werden kann, die der technischen Infrastruktur und der regulatorischen Expertise fehlt, um diese hybriden Studiendesigns auszuführen.
was hat die Auswirkungen der künstlichen Intelligenz auf den Franchise Pharma-Kro-Markt?
ai-powered Patienten-Identifikationssysteme überwachen jetzt elektronische Gesundheitsakte, um Kandidaten zu finden, die bestimmte Test-Inklusion-Kriterien erfüllen, die die Rekrutierungs-Zeitlinien beschleunigen, indem förderfähige Patienten identifiziert werden, bevor Standorte manuell Diagramme überprüfen. iqvia und labcorp haben maschinelle Lernmodelle in französischen Gesundheitssystemen eingesetzt, die Patienten auf Basis von Diagnose-Codes, Labor-Werten, Medikamentenhistorikern und anderen klinischen Markern markieren. Diese Systeme reduzierten die Median-Screening-Zeit von Wochen auf Tage an Standorten mit integrierten elektronischen Gesundheitsdaten, obwohl die Adoption auf größere Krankenhausnetze mit digitalisierten Patientendaten beschränkt bleibt. der operative Nutzen ist am sichtbarsten in seltenen Krankheitsstudien, bei denen die manuelle Chart-Bewertung vorher Monate der Ermittlerzeit erforderte, um sogar eine Handvoll förderfähiger Patienten zu identifizieren.
Die natürliche Sprachverarbeitung automatisiert die Sicherheitsüberwachung, indem sie unerwünschte Ereignisse aus klinischen Noten, Laborberichten und Patiententagebüchern extrahiert, ohne dass eine manuelle Dateneingabe durch Standortkoordinatoren erforderlich ist. syneos Gesundheit und Icon haben nlp-Systeme implementiert, die ständig Testdokumentation für Sicherheitssignale scannen, potenzielle ernsthafte negative Ereignisse, die sofortige Berichterstattung an Regulierungsbehörden erfordern. Diese Automatisierung reduzierte die mediane schädliche Ereignismeldezeit von 48-72 Stunden auf unter 24 Stunden an Standorten, die die Technologie nutzen, was darauf ankommt, wenn die regulatorischen Anforderungen ernsthafte schädliche Ereignisse innerhalb von 24 Stunden nachweisen müssen. die Einschränkung ist, dass nlp Genauigkeit von der Dokumentationsqualität abhängt, und französische klinische Noten enthalten oft medizinische Kurzhand und nicht standardisierte Terminologie, die die automatisierte Extraktionssicherheit reduzieren.
die primäre Barriere für die breitere ai-Adoption ist die Datenfragmentierung über französische Gesundheitsdienstleister. Patientenakte bleiben innerhalb einzelner Krankenhaussysteme, regionaler Gesundheitsnetzwerke und privater Praktiken versöhnt, die verhindern, dass Cros ai-Modelle auf umfassenden Datensätzen trainieren, die reale Patientenpopulationen reflektieren. Darüber hinaus erfordern französische Datenschutzbestimmungen eine ausdrückliche Einwilligung des Patienten für die sekundäre Nutzung von Gesundheitsdaten in Forschungskontexten, was die Compliance-Überleitung ergänzt, dass viele Cros für ai-Entwicklungsprojekte verbieten. Dies schafft ein Paradox, wo die wertvollsten ai-Anwendungen große, vielfältige Datensätze erfordern, die französisch-rechtliche Rahmenbedingungen schwierig machen, rechtlich zusammenzustellen.
Schlüsselmarkttrends
- Pharma-Sponsoren verlagerten sich zwischen 2022 und 2024 von Transaktionsdienstkauf zu mehrjährigen strategischen Partnerschaften, die Cro-Beziehungen von fünf oder sechs Anbietern zu zwei oder drei bevorzugten Anbietern festigen.
- Eine dezentrale Testannahme beschleunigte sich im Jahr 2023, als ansm veröffentlichte Anleitung, die Remote-Patientenüberwachung und Heimgesundheitsbesuche als gültige Alternativen zu ortsbasierten Bewertungen akzeptierte.
- Biotech-Unternehmen steigerten Cro Outsourcing von durchschnittlich 60% der Entwicklungsausgaben im Jahr 2021 auf über 75% bis 2024, angetrieben durch Risikokapitaldruck, um feste Kosten zu minimieren.
- iqvia und syneos Gesundheit erweiterten ihre französischen therapeutischen Bereich Spezialisten um 25-30% zwischen 2023 und 2025, Einstellung Onkologie und seltene Krankheit Experten strategische Partnerschaftsverträge zu unterstützen.
- real-world-Beweise-Dienste entstanden als ein ausgeprägtes Angebot in 2024, mit Cros Gründung engagierten Teams zu entwickeln hybride Studien kombinieren Testdaten und Beobachtungs-Gesundheitsrekorde.
- Die Patientenrekrutierungszeiträume für Onkologie-Studien stiegen von 12 Monaten auf 16-18 Monate zwischen 2022 und 2024 aufgrund von Kapazitätsengpässen und konkurrierenden Protokollen.
- Im Jahr 2024 traten chinesische Cros in den französischen Markt ein, die die Dienstleistungen der Phase i und der frühen Phase ii mit 20 bis 25 % unter den geltenden Preisen für die Errichtung europäischer Betriebe anbieten.
- Datenmanagement-Dienste wuchsen schneller als die klinische Überwachung zwischen 2023 und 2025, was eine erhöhte Sponsor-Anforderung für fortgeschrittene Analytik und Echtzeit-Datenvisualisierung während der Versuche widerspiegelt.
France Pharma cro Marktsegmentierung
Typ
Die klinischen Forschungsleistungen dominieren den französischen Cro-Markt mit 65 % des Gesamtumsatzes. Dieses Segment umfasst Patientenrekrutierung, Standortüberwachung, Datenerhebung und regulatorische Einreichungsunterstützung für Phase i durch klinische Studien. die Dominanz spiegelt eine strukturelle Verschiebung wider, in der Pharma- und Biotech-Sponsoren das Testmanagement auf Cros aussetzen und nicht interne klinische Operationsteams aufrecht erhalten. Full-Service Cros wie iqvia, Labcorp und Syneos Gesundheit fungieren als der klinische Entwicklungsarm des Sponsors, Management von Ermittlerbeziehungen, regulatorische Interaktionen und Datenqualitätsübersicht über mehrere gleichzeitige Studien. die Wertvorstellung ist Risikoübertragung: Sponsoren zahlen Cros, um eingeschriebene Patienten und saubere Daten im Zeitplan zu liefern, während der Cro die operative Komplexität und die Zeitleiste Variabilität absorbiert.
Präklinische Forschungsleistungen machen 22 % des Marktes aus, darunter Toxikologiestudien, pharmakokinetische Analyse und Formulierungsentwicklung, die vor menschlichen Versuchen auftreten. Dieses Segment dient den frühesten Biotech-Unternehmen und Pharma-Entdeckungsteams, die spezialisierte Laborfähigkeiten benötigen, ohne eigene Einrichtungen zu bauen. charles River, covance und eurofins dominieren french preklinische Dienstleistungen durch das Eigentum von glp-zertifizierten Labors, die für regulatorische Toxikologie Studien ausgestattet sind. das Segment ist technisch anspruchsvoll, weil präklinische Studien strenge Regulierungsstandards für die Datenqualität und Reproduzierbarkeit erfüllen müssen, die validierte Analysemethoden erfordert und erfahren Laboratorien Wissenschaftler. Margen sind höher als die klinische Forschung, da die Schaltkosten beträchtlich sind, wenn ein Sponsor ein bestimmtes Labor für ein Entwicklungsprogramm qualifiziert.
Labordienstleistungen und andere Spezialangebote stellen zusammen 13 % des Marktes dar. Dazu gehören bioanalytische Tests, zentrale Labordienstleistungen für klinische Studien und Nischenfähigkeiten wie medizinische Gerätetests oder digitale Gesundheitsvalidierung. das Segment wuchs zwischen 2023 und 2025 schneller als Kern klinische Forschung, da Sponsoren zunehmend integrierte Dienstleistungen benötigen, die das klinische Studienmanagement mit spezialisierter Laboranalyse kombinieren. z.B. Onkologie-Studien benötigen häufig eine Begleitdiagnostikentwicklung neben Drogen Tests, die Cros erfordert, die Biomarker Validierung, klinische Probensammlung und diagnostische Assayentwicklung als einheitliches Programm koordinieren können. Cros, die diese integrierten Dienstleistungen anbieten, erfassen höhere pro-Projekt-Einnahmen als diejenigen, die nur klinische Studienmanagement bieten.
mehr über diesen Bericht erfahren, kostenlos herunterladen
durch Anwendung
Drogenentwicklungsanwendungen führen zu 41,3 % der Marktnachfrage, die Formulierungsentwicklung, Stabilitätstests, analytische Methodenentwicklung und Produktionsunterstützung abdeckt. Pharmaunternehmen überlagern diese Aktivitäten, wenn interne Entwicklungsfunktionen keine Kapazität oder spezialisierte Expertise für spezifische Formulierungsprobleme haben. z.B. die Entwicklung stabiler Formulierungen für Biologik erfordert spezialisierte Ausrüstung und Know-how, die die meisten Sponsoren nicht im eigenen Betrieb halten. Cros wie catalent, patheon und lonza bieten diese Fähigkeiten auf Vertragsbasis, so dass Sponsoren Kandidaten durch Entwicklung ohne Kapitalanlage in Formulierungslabors zu fördern. die Anwendung ist Margenakkretiv, weil die Formulierungsentwicklungsarbeit technisch komplex ist und erfahrene Wissenschaftler benötigt, die Prämienrechnungssätze beauftragen.
Die klinischen Studien-Anwendungen machen 38,7% der Nachfrage aus, die sich speziell auf die Patienteneinschreibung, das Standortmanagement und die Testausführung konzentrierten und nicht auf eine breitere Entwicklungsunterstützung. Dieses Segment unterscheidet sich von klinischen Forschungsdienstleistungen dadurch, dass es nur die Testausführungskomponente erfasst, ausgenommen regulatorische Strategie, Datenanalyse und Post-Trial-Aktivitäten. die Anwendung wuchs zwischen 2022 und 2024, als Biotech-Unternehmen suchten Cros, die Patientenrekrutierung und Standortüberwachung behandeln konnte, während andere Entwicklungsmaßnahmen im eigenen Haus beibehalten. Diese Entbündelung ermöglichte es den Sponsoren, die betriebsmäßig komplexesten und zeitnah sensiblen Aspekte der klinischen Entwicklung zu externisieren und gleichzeitig die Kontrolle über strategische Entscheidungen wie Endpunktauswahl und Testdesign zu bewahren.
Toxikologiestudien, Datenmanagement und andere Anwendungen stellen zusammen 20% des Marktes dar. Toxikologiestudien sind obligatorisch für regulatorische Einreichungen und erfordern glp-zertifizierte Einrichtungen, die die meisten Sponsoren nicht intern betreiben. Datenmanagement-Dienste sind schnell gewachsen, da Versuche zunehmende Mengen elektronischer Daten von Wearables, Remote Monitoring-Geräten und geduldig gemeldeten Ergebnissen generieren, die spezialisierte Datenbankplattformen und statistische Analysemöglichkeiten benötigen. Cros, die zwischen 2020 und 2025 in Cloud-basierte Datenplattformen und Echtzeit-Analysen investierten, erfasste die wachsende Nachfrage nach Sponsoren für transparente Testüberwachung und adaptive Testdesigns, die eine kontinuierliche Datenanalyse erfordern, anstatt herkömmliche gesperrte Datenbanken, die nur am Studienabschluss geprüft wurden.
durch Endverbraucher
Pharmaunternehmen stellen 52,8% der Nachfrage nach Cro in France dar. große Pharmaunternehmen auslagern spezifische Entwicklungsprogramme, bei denen interne Kapazitäten eingeschränkt oder therapeutische Fachkompetenz fehlt. z.B. könnte ein Unternehmen mit starken Onkologie-Fähigkeiten die Entwicklung von seltenen Krankheiten auf Cros mit etablierten Patientenregistern und Untersuchungsnetzwerken in diesen Indikationen aussetzen. die Outsourcing-Entscheidung ist wirtschaftlich getrieben: die Aufrechterhaltung von hauseigenen klinischen Operationen für therapeutische Bereiche, in denen das Unternehmen nur eine oder zwei Versuche pro Jahr durchführt, ist kostenprohibitiv im Vergleich zu den projektbezogenen Cros. Dies schafft eine stabile Nachfrage nach Cros in therapeutischen Bereichen, in denen Sponsoren Interesse erhalten, aber einzelne Unternehmensportfolios sind begrenzt.
Biotech-Firmen machen 31,4% des Marktes aus und stellen das am schnellsten wachsende Segment mit 9,1% cagr bis 2033 dar. Diese Unternehmen verfügen typischerweise über interne klinische Entwicklungsfähigkeiten und äussern die meisten Entwicklungsarbeiten von präklinischen Studien über Phasen iii-Studien. der Wachstumstreiber ist Risikokapitalfinanzierungsdynamik: Biotech-Unternehmen werden erwartet, klinische Fortschritte schnell zu demonstrieren, während die Minimierung von Cash Burn, die Outsourcing zu Cros finanziell attraktiver macht als die Erstellung interner Fähigkeiten, die feste Headcount erfordern. Cros bietet Biotech-Sponsoren mit flexibler Kapazität, die mit Programmanforderungen skaliert, Abrechnung nur für aktive Projekte, anstatt laufende Retainer-Zahlungen oder Salaried-Mitarbeiter.
Forschungsinstitute und andere Endnutzer tragen 15,8% der Nachfrage bei. wissenschaftliche medizinische Zentren und staatliche Forschungsorganisationen beschäftigen sich mit cros für investigatorinitiierte Studien und öffentliche Gesundheitsstudien, die eine regulatorische Datenerhebung und -überwachung erfordern. Diese Kunden arbeiten in der Regel auf Fördermitteln mit festen Budgets und definierten Fristen, die Cros für Dienstleistungen innerhalb starrer Kostenzwänge benötigen. das Segment bietet niedrigere Margen als kommerzielle pharmazeutische Arbeit, bietet aber Cros Zugang zu neuartigen therapeutischen Ansätzen und seltenen Krankheit Patientenpopulationen, die später in kommerzielle Entwicklungsmöglichkeiten übersetzen, wenn akademische Entdeckungen in Richtung regulatorische Zulassung und Kommerzialisierung bewegen.
durch Phase
Phase iii Studien erzeugen 43,2% der klinischen Forschungseinnahmen aufgrund ihrer großen Patientenpopulationen, erweiterten Überwachungszeiten und komplexen regulatorischen Anforderungen. Eine typische Phase iii Onkologie-Studie in France könnte 300-500 Patienten in 25-40 Untersuchungsstellen über drei bis vier Jahre einschreiben, die Standortüberwachung, Datenmanagement, Sicherheitsberichterstattung und regulatorische Koordination im gesamten Studienzeitraum erfordern. cros bieten Wert durch die Verwaltung dieser operativen Komplexität und ermöglicht es Sponsoren, sich auf strategische Entscheidungen rund um das Testdesign und regulatorische Einreichungen zu konzentrieren. die Umsatzkonzentration in Phase iii spiegelt sowohl die unmittelbaren Kosten der Großversuchsausführung wider, als auch die Risikoprämiensponsoren zahlen für Cros, um auf aggressiven Einschreibungs-Zeitlinien zu liefern, die die Produktstartdaten bestimmen.
Phase ii-Studien tragen 28,6% des Umsatzes bei, konzentrierten sich auf Dosisuntersuchungen und erste Wirksamkeitsbeurteilungen in kleineren Patientenpopulationen. Diese Versuche verwenden zunehmend adaptive Designs, die Einschreibungskriterien oder Dosierpläne auf Basis von Zwischenergebnissen verändern, was Cros mit starken statistischen und Datenmanagement-Funktionen erfordert. die technische Komplexität von adaptiven Versuchen schafft Barrieren für den Einstieg für kleinere Cros, die keine spezialisierte Expertise haben, so dass größere Full-Service-Anbieter Premium-Preis zu beauftragen. Phase ii Arbeit ist für Cros strategisch wichtig, da Sponsoren, die erfolgreich Phase ii abgeschlossen haben, in der Regel mit dem gleichen Schritt in Phase iii fortfahren und Mehrjahres-Umsatz-Pipelines aus dem frühen Einsatz schaffen.
Phase i, Phase iv und andere Versuchsphasen zusammen 28,2% des Umsatzes. Phase i-Studien sind relativ klein, aber technisch anspruchsvoll, erfordern spezialisierte Einrichtungen für Erst-in-Menschen-Sicherheitsstudien und intensive Patientenüberwachung. Phase iv Post-Marketing-Studien wachsen, da Regulatoren zunehmend real-world-Anweisungen benötigen, um vorbeugende klinische Daten zu ergänzen. Cros, die sowohl traditionelle Phase iv-Studienmanagement als auch reale Nachweisfähigkeiten bieten, die Testdaten mit Beobachtungs-Gesundheitsdaten kombinieren, erfassen die steigende Nachfrage nach Sponsoren für integrierte nachvermarktende Überwachungsprogramme, die regulatorische Anforderungen erfüllen und gleichzeitig Nachweise für Auszahlungsverhandlungen und klinische Leitlinienentwicklung generieren.
Was sind die wichtigsten Anwendungsfälle, die den France Pharma Cro Markt fahren?
die primäre Anwendung ist Full-Service-Phase iii-Test-Management für Biotech-Unternehmen, die interne klinische Operationen fehlt. Diese Sponsoren beschäftigen sich mit Cros, um alle Aspekte der Testausführung von der Standortauswahl über das Datenbankschloss, die regulatorische Einreichung und die Sicherheitsüberwachung nach der Genehmigung zu behandeln. Ein typisches Engagement könnte eine seltene Krankheitsanzeige beinhalten, bei der der Biotech-Sponsor Phase abgeschlossen hat ii Nachweis-of-concept-Studien und braucht einen Schritt, um das für die ema-Zulassung erforderliche Programm zu leiten. die cro bietet Ermittler-Site-Netzwerke, regulatorische Expertise, Patientenrekrutierungsstrategien und Datenmanagement-Infrastruktur auf schlüsselfertiger Basis, so dass das Biotech-Unternehmen zu Kommerzialisierung voranzutreiben, ohne permanente klinische Operationen Headcount zu bauen.
Nebennachfrage kommt von großen Pharmaunternehmen Outsourcing therapeutischer flächenspezifischer Entwicklungsprogramme. z.B. könnte ein Unternehmen mit begrenztem Immunologie-Know-how einen Schritt zur Verwaltung aller klinischen Entwicklung für einen erworbenen Immunologie-Assistenten unternehmen, um die etablierten Beziehungen des Cro mit der französischen Rheuma und dermatologie-Ermittlern zu nutzen. Diese strategischen Partnerschaften umfassen in der Regel mehrere Studien über mehrere Jahre hinweg, so dass der Cro mit vorhersehbaren Einnahmen und geben dem Sponsor Zugang zu therapeutischen Bereichsexpertise ohne ständige Personalerweiterung. die kommerzielle Logik ist Spezialisierung: Cros, die sich auf bestimmte therapeutische Bereiche konzentrieren, entwickeln tiefe Ermittlerbeziehungen und Protokoll-Design-Erfahrung, die generalistische interne Entwicklungsteams nicht replizieren können.
neue Anwendungsfälle zentrieren sich auf Hybrid-Test-Designs, die traditionelle randomisierte kontrollierte Versuche mit realen Beweisen aus französischen Gesundheitsdatenbanken kombinieren. Sponsoren beschäftigen sich mit der Entwicklung von Studien, bei denen der Kontrollarm angepasste Patienten aus elektronischen Gesundheitsakten verwendet, anstatt ein separates Placebo-Kohort einzuschreiben, was die Testkosten reduziert und die Einschreibungszeitlinien beschleunigt. iqvia und syneos Gesundheit haben engagierte Teams gegründet, um diese Hybrid-Studien durchzuführen, die Datenwissenschaftler, Epidemiologen und regulatorische Spezialisten erfordern, die sowohl klinische Studienmethodik als auch reale Beweisstandards verstehen. die Anwendung ist technisch anspruchsvoll, bietet aber Sponsoren erhebliche Kosteneinsparungen, mit einigen Hybrid-Designs reduzieren Phase iii Kosten um 30-40% im Vergleich zu herkömmlichen voll eingeschriebenen Versuchen.
Bericht Metriken | Details |
Marktgrößenwert 2025 | usd 1,295,8 Mio |
Marktgrößenwert 2026 | usd 1.392.6 million |
Umsatzprognose 2033 | mit 2,358,7 Mio |
Wachstumsrate | 7,82% von 2026 bis 2033 |
Basisjahr | 2025 |
historische Daten | 2021 – 2024 |
Vorausschätzungszeitraum | 2026 – 2033 |
Berichterstattung | Umsatzprognose, Wettbewerbslandschaft, Wachstumsfaktoren und Trends |
Regionaler Geltungsbereich | Franken |
Schlüsselunternehmen profiliert | iqvia, labcorp, syneos health, parexel, icon plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat |
Anpassungsbereich | freier Bericht Anpassung (Regional- & Segment-Bereich). nutzen Sie kundenspezifische Kaufoptionen, um Ihren genauen Forschungsanforderungen gerecht zu werden. |
Berichtsegmentierung | nach Typ (klinische Forschung, präklinische Forschung, Labordienstleistungen, andere); durch Anwendung (Drogenentwicklung, klinische Studien, Toxikologiestudien, Datenmanagement, andere); durch Endverbraucher (Apotheken, Biotech-Unternehmen, Forschungsinstitute, andere); durch Phase (Phase i, Phase ii, Phase iii, Phase iv, andere) |
was treibt das Wachstum im France Pharma-Kro-Markt?
France bietet Cros drei strukturelle Vorteile, die andere europäische Märkte nicht in vergleichbarem Umfang nachbilden können. Erstens betreibt das Land ein zentralisiertes Gesundheitssystem mit umfassenden elektronischen Gesundheitsaufzeichnungen, die über 65 Millionen Bürgerinnen und Bürger umfassen und Cros mit Patientenidentifikationsfähigkeiten und realen Zugang zu Beweisen bieten, die fragmentierten Gesundheitssystemen nicht entsprechen können. Zweitens, France hält dichte Konzentrationen von spezialisierten Untersuchungsstellen in paris, lyon und marseille, wo akademische medizinische Zentren, Lehrkrankenhäuser und Forschungsinstitute Cluster in geographischer Nähe, die die Testlogistik vereinfacht und die Überwachungskosten im Vergleich zu geografisch verteilten Standortnetzwerken reduziert. Drittens, Ansm hat vorhersehbare regulatorische Überprüfung Zeitpläne und klare Leitlinien für aufstrebende Testmethoden wie dezentrale Protokolle und reale Welt-Beweise, die die Unsicherheit für Sponsoren, die mehrjährige Entwicklungsprogramme planen, reduziert.
die wettbewerbsfähige Dynamik in France unterscheidet sich von anderen europäischen Märkten, da Sprach- und Regulierungsanforderungen natürliche Barrieren für den Eintritt in Nicht-eu-Kroos schaffen. Testprotokolle, informierte Zustimmungsdokumente und regulatorische Einreichungen müssen in französischer Sprache sein, was engagierte lokale Mitarbeiter und nicht zentralisierte europäische Teams erfordert, die auf Englisch arbeiten. Darüber hinaus verlangen französische Datenschutzbestimmungen spezifische Anforderungen an die Behandlung von Gesundheitsdaten, die sich von allgemeinen gdpr-Bestimmungen unterscheiden, wobei Cros zur Aufrechterhaltung von françaisspezifischen Compliance-Programmen verpflichtet ist. Diese Barrieren schützen etablierte Spieler wie iqvia, Labcorp und Syneos Gesundheit, die seit Jahrzehnten in France betrieben und in lokale Infrastruktur investiert haben, und schaffen höhere Einstiegskosten für neue Konkurrenten, die versuchen, französische Operationen zu etablieren.
das am schnellsten wachsende Nachfragesegment ist seltene Krankheitsversuche, bei denen die nationale Gesundheitsdatenbank des France eine schnelle Patientenidentifizierung für ultra-rare Indikationen ermöglicht. unter Bedingungen, die weniger als 1.000 französische Patienten betreffen, kann die traditionelle ortsbasierte Rekrutierung Jahre dauern, weil die Ermittler manuell medizinische Aufzeichnungen zur Identifizierung förderfähiger Kandidaten anzeigen müssen. Cros, die Datenzugangsvereinbarungen mit französischen Gesundheitsbehörden geschlossen haben, können die gesamte nationale Patientenpopulation elektronisch abbilden und förderfähige Patienten in Wochen anstatt Monaten identifizieren. Diese Fähigkeit hat France zu einem bevorzugten Standort für europäische Seltenheitsversuche gemacht, mit Sponsoren immer mehr wählen französische Standorte als führende Länder für multinationale Studien in ultra-rassigen Indikationen, wo die Patientenidentifikation Geschwindigkeit bestimmt allgemeine Programmzeitlinien.
wer sind die Schlüsselakteure im France Pharma-Cro-Markt und wie konkurrieren sie?
der französische Cro-Markt als zweistufige Struktur arbeitet. iqvia, labcorp, syneos health, parexel, and icon kollektive halten etwa 55-60% Marktanteil und konkurrieren als Full-Service-Anbieter bietet integrierte Fähigkeiten von preklinical bis phase iv. Diese Unternehmen konkurrieren auf therapeutische Bereich Know-how, Ermittler-Site-Netzwerke und Technologie-Plattformen, die Sponsoren mit Echtzeit-Test-Sichtbarkeit bieten. Mid-Tier und kleinere Cros belegen spezialisierte Nischen auf der Grundlage von therapeutischen Fokus, Service-Typ oder regionale Präsenz, in der Regel mit größeren Cros auf komplexen Programmen, anstatt direkt für Full-Service-Kontrakte zu konkurrieren.
iqvia tritt durch seine integrierte Daten- und klinische Services-Plattform zusammen, die das Testmanagement mit realen Beweisen kombiniert. das Unternehmen betreibt die größte kommerzielle Gesundheitsdatenbank von France, die verschreibungspflichtige Daten, Krankenhaus-Entladungsdaten und Schadensinformationen abdeckt, die es zur Identifizierung, Standortauswahl und Machbarkeitsbewertung verwendet. Zwischen 2023 und 2025 erweiterte iqvia seine französisch-klinischen Operationen um 25 % und fügte den therapeutischen Bereich Spezialisten für Onkologie, seltene Krankheiten und Immunologie hinzu, um strategische Partnerschaftsverträge mit großen Pharmasponsoren zu unterstützen. das Unternehmen differenziert auf Analysefähigkeiten, bietet Sponsoren mit prädiktiven Einschreibungsmodellen und vergleichende Effektivitätsanalysen, dass kleinere Cros nicht replizieren können, ohne äquivalente Datenwerte.
labcorp tritt durch die vertikale Integration von Labordienstleistungen und klinischen Studienmanagement, so dass das Unternehmen bietet Sponsoren einheitliche Programme, die Testausführung mit zentralen Labortests, Biomarker-Analyse und Begleitdiagnostik-Entwicklung kombinieren. Diese Integration betrifft die Onkologie und seltene Krankheitsstudien, bei denen die biomarkergetriebene Patientenauswahl und die pharmakodynamischen Bewertungen eine Koordination zwischen klinischen Standorten und spezialisierten Labors erfordern. labcorp betreibt glp-zertifizierte Labore in France, die sowohl klinische Testsponsoren als auch routinemäßige diagnostische Märkte bedienen, wodurch Größenvorteile entstehen, die rein-play cros nicht übereinstimmen können. das Unternehmen zielt darauf ab, Biotech-Sponsoren zu entwickeln Präzisionsmedizin-Kandidaten, bei denen integrierte Labor- und klinische Dienstleistungen die Koordination über Kopf reduzieren und die Entwicklungszeiträume beschleunigen, verglichen mit separaten Anbietern für Testmanagement und Labortests.
aktuelle Entwicklungen
im März 2026 kündigte iqvia eine strategische Partnerschaft mit einer französischen Patientenregistrierung für seltene Krankheiten an, um genetische Tests und natürliche Geschichtsdaten für ultra-rare neurologische Bedingungen bereitzustellen. die Zusammenarbeit zielt darauf ab, die Patientenidentifikation und die Testdurchführbarkeitsbeurteilungen für Sponsoren zu beschleunigen, die Therapien für Bedingungen entwickeln, die weniger als 500 französische Patienten betreffen. http://www.iqvia.com (iqvia)
im Februar 2026 erweiterte Labcorp seine französischen zentralen Laboroperationen mit neuen Biomarker-Testmöglichkeiten für Zell- und Gentherapieversuche. die Anlage verarbeitet pharmakodynamische Proben und Begleitdiagnostik-Assays für fortgeschrittene Therapiesponsoren, die französische klinische Studien durchführen. http://www.labcorp.com (labcorp)
Welche strategischen Einsichten definieren die Zukunft des France Pharma-Kro-Marktes?
In den nächsten fünf bis sieben Jahren wird der Wettbewerbsvorteil im französischen Cro-Markt von der operativen Ausführung auf Daten- und Technologieplattformen übergehen, die neue Testmethoden ermöglichen. der aktuelle Markt belohnt Cros, die Patienten schnell einschreiben und saubere Daten über den Zeitplan liefern können, aber diese Fähigkeiten werden als elektronische Datenerfassung und Remote-Monitoring-Tools in der gesamten Industrie kommoditiert. die nächste wettbewerbsfähige Grenze ist die Integration von realen Beweisen, die dezentrale Testdurchführung und die ai-powered Patientenidentifizierung, die alle erhebliche Technologie-Investitionen und Datenzugriffsvereinbarungen erfordern, die Barrieren für den Eintritt für Wettbewerber schaffen, die keinen Umfang haben.
das Risiko, dass Marktprognosen unterschätzen können, sind regulatorische Akzeptanzzeiträume für neuartige Testmethoden. Ansm hat Leitlinien für dezentrale Studien und reale Beweise veröffentlicht, aber die tatsächliche regulatorische Überprüfung der Einreichungen, die diese Ansätze verwenden, bleibt begrenzt. Wenn die Regulierungsbehörden in der Praxis mehr Konservativ als die Leitlinien vorschlagen, können die Sponsoren die Annahme dieser Methoden verzögern, was die Nachfrage nach Cro-Fähigkeiten in diesen Bereichen verringern würde und die traditionelle ortsbasierte Testausführung bevorzugen würde, in der regulatorische Präzedenzfall begründet ist. Dies würde incumbent cros mit starken Standort-Netzwerken profitieren, während die Nachteile neuer Teilnehmer, die stark in dezentrale Testplattformen investiert.
die Möglichkeit, die noch unterpreist bleibt, ist post-zulassende real-world-Beweise-Dienste, die Phase iv-Studienmanagement mit Beobachtungsstudien mit französischen Gesundheitsdatenbanken kombinieren. Die Zahler benötigen zunehmend Echtzeit-Effizienzdaten, um Rückerstattungsentscheidungen zu unterstützen, und Sponsoren benötigen Cros, die integrierte Programme entwerfen können, die sowohl regulatorischen Post-Marketing-Anforderungen als auch den Gehaltsempfänger-Anforderungen entsprechen. das Segment ist derzeit klein, bietet aber höhere Margen als traditionelle Phase iv Arbeit, weil es spezialisierte Fähigkeiten in der Gesundheitsökonomie, Epidemiologie und Datenbankanalytik erfordert, die die meisten Cros nicht pflegen. Unternehmen, die diese Fähigkeiten aufbauen, werden die wachsende Nachfrage von Sponsoren nach Beweis-Generierungs-Programmen erfassen, die mehrere Stakeholder bedienen und nicht nur regulatorische Verpflichtungen erfüllen.
Häufig gestellte Fragen
Finden Sie schnelle Antworten auf die häufigsten Fragen.
der france pharma-kro-markt wird voraussichtlich bis 2033 2,358,7 millionen erreichen.
schlüsselsegmente für den franchise-branchenmarkt sind nach typ (klinische forschung, präklinische forschung, labordienstleistungen, andere); durch anwendung (drogenentwicklung, klinische studien, toxikologiestudien, datenmanagement, andere); durch endverbraucher (apotheken, biotech-unternehmen, forschungsinstitute, andere); durch phase (phase i, phase ii, phase iii, phase iv, andere).
die wichtigsten france pharma-kro-marktspieler sind iqvia, labcorp, syneos gesundheit, parexel, icon plc, charles river, medpace, pra health sciences, covance, eurofins, wuxi apptec, sgs, ppd, clinipace, veristat.
die aktuelle france pharma-kro-marktgröße beträgt 1,295,8 millionen in 2025.
der france pharma cro markt cagr ist 7,82% von 2026 bis 2033.
Zuletzt veröffentlichte Berichte
-
Apr 2026
Markt für Cord Blood Banking Services
cord-blut-banking-dienste marktgröße, aktien- und analysebericht nach art des dienstes (sammlung, verarbeitung, lagerung), per banktyp (private banken, öffentliche banken und hybridbanken), durch komponente (bandblut und kordelgewebe), durch endbenutzer (krankenhäuser, forschungseinrichtungen, biotechnologie-unternehmen und andere) und geographie (nordamerika, europa, asien-pazifik, mittelost und afrika, süd- und zentralamerika), 2021
-
Apr 2026
Markt für ELISA-Prozessoren
elisa-prozessoren marktgröße, aktien- und analysebericht nach typ (optischer filter elisa-analyser, optische gitter elisa-analyser), nach modus (automatisierte elisa-analyser und semi-automatisierte elisa-analyser), nach anwendungen (immunologie, impfstoffentwicklung, drogenüberwachung und andere), von endnutzern (biotechnologie-unternehmen, pharmaunternehmen, vertragsforschungsorganisation, und diagnoselabors) und geographie (nordamerika, mittelamerika, mitteleuropa
-
Apr 2026
Markt für Mikroskop Slide Scanner
mikroskopische diascanner marktgröße, aktien- und analysebericht nach typ (portable mikroskop-disaster und desktop-mikroskop-disaster), durch anwendung (biologische forschung, medizin, tierarznei und andere) und geographie (nordamerika, europa, asien-pazifik, mittelost und afrika, süd- und zentralamerika), 2021 - 2031
-
Apr 2026
Markt für Mikrowellenherd
mikrowellenherd marktgröße, aktien- und analysebericht nach materialtyp (kunststoff, glas, keramik, silikon und metall), durch anwendung (kochen, nachwärmen und abtauen), durch endverbraucher (haushalt, gewerbe (restaurants, hotels und cafés) und lebensmittel-service-industrie), durch verkaufskanal (online-einzelhandel, offline-einzelhandel (supermärkte, supermärkte, spezialgeschäfte)


