europe Healthcare Contract Research Organisation Marktgröße & Prognose:
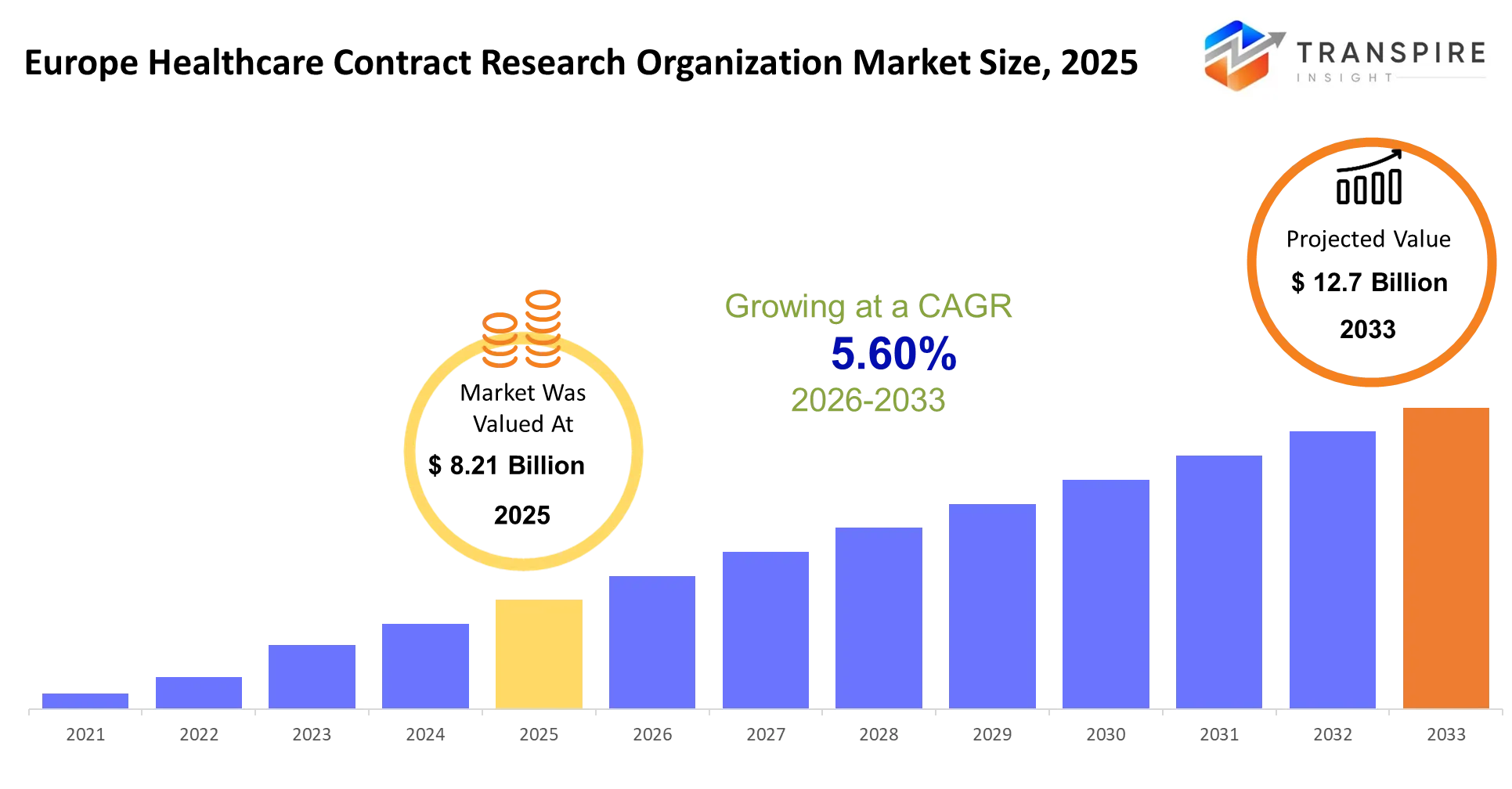
- europe Healthcare Contract Research Organisation Marktgröße 2025: usd 8.21 Milliarden
- europe Healthcare Contract Research Organisation Marktgröße 2033: usd 12,7 Milliarden
- europe Healthcare Contract Research Organisation Markt cagr: 5.60%
- europe Healthcare Contract Research Organisation Marktsegmente: nach Typ (klinische Forschungsdienstleistungen, vorklinische Dienstleistungen, Labordienstleistungen, andere), durch Anwendung (drug development, klinische Studien, medizinische Gerätetests, Regulierungsdienstleistungen, andere), durch Endbenutzer (Apotheken, Biotech-Firmen, medizinische Geräteunternehmen, Forschungsinstitute, andere), durch Phase (Phase i, Phase ii, Phase iii, Phase iv, Phase iv, andere)
mehr über diesen Bericht erfahren, kostenlos herunterladen
europe Healthcare Contract Research Organisation Markt Zusammenfassung:
die europe Healthcare-Kontrakt-Forschungsorganisation Marktgröße wird auf schätzungsweise 8.21 Milliarden in 2025 und wird erwartet, um uns zu erreichen 12,7 Milliarden bis 2033, wächst mit einem cagr von 5.60% von 2026 bis 2033. European Healthcare Contract Research Organisationen fungieren als ausgelagerte Arzneimittelentwicklungslabore, die alle Aspekte der klinischen Studiendurchführung für Pharma- und Biotech-Kunden behandeln. die Organisationen ermöglichen es Sponsoren, die Therapieentwicklung von Labortests bis zur Marktfreigabe durch die Bereitstellung wesentlicher operativer Ressourcen und spezialisierter Expertise zu führen, die ihnen fehlt.
dezentrale und hybride Testmodelle, die digitale Monitoring-Tools und Remote-Patienten-Eingriffsmethoden verwenden, sind in den letzten drei bis fünf Jahren zum primären Forschungsansatz geworden. die Schicht ermöglicht es Forscherteams, mit mehr Patienten zu arbeiten, weil sie ihre Notwendigkeit, bestimmte Forschungseinrichtungen zu verwenden reduziert. die covid-19 Pandemie diente als Hauptkatalysator, weil es Versuche erforderte, trotz der Einschränkungen der Bewegung fortzufahren und es führte zu einer schnelleren Akzeptanz virtueller Methoden durch Regulierungsbehörden.
die zunehmende Anforderung an schnelle und flexible Lösungen hat sich als Haupttreiber für Sponsoren herausgestellt, die nun Outsourcing-Dienste zu höheren Preisen nutzen. die Kombination von Datenanalysen und realen Beweisen und adaptiven Testfunktionen ermöglichte es Cros, skalierbare Einnahmenströme aus ihren operativen Komplexitäten zu erstellen.
wichtige Markteinsichten
- Westeuropäische Länder kontrollieren den europäischen Markt für Gesundheitswesen-Vertragsforschung, weil sie mehr als 65% Marktanteil halten, den Deutschland, das vereinte Königreich und France im Jahr 2024 führen.
- Osteuropa steht bis 2030 als am schnellsten expandierendes Gebiet, da es seine Fähigkeit hat, kosteneffektive Prüfungen durchzuführen und die Teilnehmer schnell und ihren Fortschritt in Richtung auf die entsprechenden europäischen Rechtsvorschriften zu rekrutieren.
- Der Bereich der klinischen Studienleistungen führt den Markt mit einem Anteil von 70%, da die europäischen Länder ihre Phase ii und iii Studien auslagern.
- der zweitgrößte Marktanteil in der Branche gehört zu preklinischen Dienstleistungen, die Unterstützung von Biotech-Unternehmen erhalten, die neue Produkte entwickeln und ihre expandierenden Forschungs- und Entwicklungsaktivitäten.
- das Segment des Datenmanagements und der Real-World-Evidenzdienste erfährt ein schnelles Wachstum, da die digitale Testdurchführung die Expansion von 2025 bis 2030 antreibt.
- das Onkologiefeld hält den größten Anwendungsmarktanteil, der 2024 30 % erreichte, weil medizinische Forscher komplexe Studien durchführen und Krebsforscher zahlreiche Krebsmedikamente entwickeln.
- die Entwicklung der personalisierten Medizin zusammen mit der regulatorischen Unterstützung für seltene Krankheiten schafft die am schnellsten entwickelnden medizinischen Behandlungsbereiche, die gezielte Therapien entwickeln.
- Pharmaunternehmen kontrollieren etwa 60% des Marktes, weil sie mit Cros zusammenarbeiten, um ihre operativen Ausgaben zu verringern, während sie ihren Drogenentwicklungsprozess beschleunigen.
- kleine und mittelständische Biotech-Firmen stellen das sich am schnellsten entwickelnde Anwendersegment dar, das jetzt von kompletten Service Outsourcing-Lösungen abhängt, um ihren Wachstumsbedarf zu unterstützen.
Was sind die wichtigsten Treiber, Einschränkungen und Chancen auf dem europe Healthcare-Vertrag Forschungsorganisation Markt?
das Hauptelement, das das Wachstum im europe Healthcare-Vertragsforschungsunternehmen Markt vorantreibt, resultiert aus einer verstärkten Auslagerung komplizierter klinischer Entwicklungsarbeiten, die sich aus steigenden Forschungs- und Entwicklungsaufwendungen ergaben, die uns jetzt 2 Milliarden pro zugelassenes Medikament überstiegen. Pharmaunternehmen müssen ihre Produktentwicklungszeiträume reduzieren, während sie sich mit komplizierten regulatorischen Anforderungen befassen, die in verschiedenen europäischen Ländern bestehen. Organisationen üben jetzt höhere Outsourcing-Raten, weil ihre späten Stadium klinischen Studien die schwierigsten Ausführungs- und Patienteneinschreibungsschwierigkeiten enthalten. Sponsoren, die mehr Geld für externe Testkosten ausgeben, schaffen wertvollere Verträge, die zu erweiterten Service-Beziehungen mit Cros führen.
das europäische Regulierungssystem bleibt trotz der Existenz von ema-Verordnungen, die die Forschungsaktivitäten kontrollieren, zwischen verschiedenen nationalen Vorschriften aufgeteilt. jede Nation betreibt eigene separate Systeme, um Ethik-Zulassungen zu erhalten und Patientendaten zu verwalten und die Einhaltung an Forschungseinrichtungen zu gewährleisten. das bestehende operationelle Modell für klinische Forschungsorganisationen (Krebs) stellt Herausforderungen, da sie standardisierte Operationen aufrecht erhalten müssen, die zu längeren Vorbereitungszeiten und erhöhten Verwaltungskosten führen. der Prozess führt zu Studienverzögerungen, die bestimmte Märkte weniger attraktiv machen und dadurch die Umsatzchancen begrenzen und das Wachstum der europäischen Forschungsmodelle einschränken.
das Wachstumspotenzial für dezentrale klinische Studien zeigt ein erhebliches Versprechen, da digitale Gesundheitssysteme in Ländern wie Deutschland und der nordischen Region weiter fortgeschritten werden. Fernüberwachung und umweltfreundliche und tragbare Datenerfassungstechnologien ermöglichen es mehr Patienten, an Studien teilzunehmen, die zu einer schnelleren Studieneinschreibung führen.
was hat die Auswirkungen der künstlichen Intelligenz auf den europe Healthcare-Vertrag Forschungsorganisation Markt?
europäische Vertragsforschungsorganisationen nutzen nun künstliche Intelligenz zusammen mit fortschrittlichen digitalen Werkzeugen, um ihren klinischen Prozess durch automatisierte Ausführung wesentlicher operativer Aufgaben zu transformieren. ai-powered Systeme nutzen nun die natürliche Sprachverarbeitung zusammen mit der robotischen Prozessautomatisierung, um den Patientenidentifikationsprozess und die Ortsdurchführbarkeitsbeurteilungen und Datenreinigungsaufgaben auszuführen. das System stellt einen Versuchsaufbau- und -überwachungsprozess fest, der weniger manuelle Arbeiten erfordert, um zwischen 20 % und 20 % Zeitersparnis zu erreichen und gleichzeitig genauere Datenergebnisse durch Mehrländerstudien zu erzeugen. digitale Kontrollschichten ermöglichen es Unternehmen, die Einhaltung zu überwachen, da sie die Testdaten kontinuierlich gegen wechselnde regulatorische Standards überprüfen.
maschinelle Lernmodelle fügen Vorhersagefähigkeiten hinzu, die die Testleistung direkt beeinflussen. Sponsoren und Cros nutzen Algorithmen, um Patientenrekrutierungsraten zu prognostizieren, Ausfallrisiken vorherzusagen und die Standortauswahl basierend auf historischen und realen Datensätzen zu optimieren. der Prozess führt zu einer besseren Einschreibungseffizienz, die teure Verzögerungen verringert, einige Studien berichten 15-25% schnellere Rekrutierungszyklen. ai unterstützt adaptive Testdesigns durch die Simulation von Protokolländerungen vor der Implementierung, was die Entscheidungsfindung unter unsicheren Bedingungen verbessert.
Die Technologien ermöglichen es Unternehmen, durch drei Hauptvorteile bessere operative Ergebnisse zu erzielen, die höhere Testerfolgsraten, weniger Protokolländerungen und geringere Gesamtentwicklungskosten beinhalten. der Prozess den Herausforderungen der Implementierung gegenübersteht, weil die Datenökosysteme fragmentiert bleiben und die Integrationskosten hoch bleiben, vor allem für die Vereinigung traditioneller klinischer Systeme in verschiedenen europäischen Regulierungsrahmen.
Schlüsselmarkttrends
- das Gebiet der dezentralen und hybriden Studien erlebte ein schnelles Wachstum seit 2020, weil mehr als 40 Prozent der europäischen Forschungsstudien Ferntestmethoden verabschiedeten, um ihren Betrieb während der Reisebeschränkungen fortzusetzen.
- die Pharmaindustrie hat ihre Outsourcing-Aktivitäten von 45 Prozent im Jahr 2018 auf mehr als 55 Prozent im Jahr 2024 erhöht, was darauf hindeutet, dass die Industrie jetzt ihre klinische Forschungsarbeit an externe Partner auslagern will.
- East europe wurde nach 2021 der beliebteste Standort für klinische Studien, da Patientenrekrutierungsprozesse in dieser Region 15 bis 20 Prozent weniger Zeit erforderten als in den westlichen europäischen Märkten.
- der Zeitraum von 2019 bis 2024 brachte zunehmende Komplexität auf Onkologie-Studien, die dazu führte, dass klinische Forschungsorganisationen komplette Servicelösungen für ihre Biomarker-Tests und flexible Testentwicklungsanforderungen benötigen.
- Biotech-Unternehmen, die mit mittlerer Größe tätig sind, begannen nach 2020 strategische Partnerschaften mit cros zu etablieren, da diese Vorgehensweise es ihnen ermöglichte, ihren Bedarf an internen Betriebskapazitäten zu verringern und gleichzeitig ihre ersten in-human-Studien zu beschleunigen.
- die covid-19 Pandemie hat neue Regulierungsregeln geschaffen, die es den Agenturen erlaubten, Fernüberwachung und Ökonsent zu nutzen und damit die Compliance-Standards in ganz Europa zu ändern.
- real-world-Beweis-Integration erreichte nach 2022 Geschwindigkeit, da Sponsoren außerhalb von Daten verwendet, um ihre regulatorischen Anwendungen und Post-Marke-Forschungsarbeit zu unterstützen.
- cros verwandelte ihr Geschäftsmodell von Service Providern zu strategischen Entwicklungspartnern durch Investitionen in digitale Gesundheitstechnologien und Standortnetzwerkfähigkeiten.
europe Healthcare Contract Research Organisation Marktsegmentierung
Typ
die Kategorie der primären klinischen Forschungsdienstleistungen unterhält Marktführerschaft, weil die Unternehmen ihre komplexen Testoperationen auslagern, die insbesondere bei späten Studien, die maximale Ausgaben und regulatorische Kontrolle beinhalten, spezialisierte Expertise erfordern. preklinische Dienstleistungen halten einen stabilen Anteil, weil europäische Biotech-Unternehmen ihre frühesten Forschungsaktivitäten ausbauen, während Labordienstleistungen durch steigende Anforderungen an Biomarkertests und zentralisierte Diagnostikdienstleistungen ein kontinuierliches Wachstum erfahren. Sponsoren bevorzugen nun komplette Service-Lösungen, weil sie integrierte Service-Modelle als effektiver betrachten als mehrere separate Anbieter-Partnerschaften.
Cros, die klinische Dienstleistungen in Verbindung mit fortschrittlichen Datenanalysen und real-world Beweisfähigkeiten bieten, erleben derzeit die höchste Nachfrage nach Markttrends. in der kommenden Wachstumsperiode werden die Anbieter die Entwicklung digitaler Werkzeugpakete verlangen, die sie mit ihren bestehenden Dienstleistungen kombinieren können, um wertvolle Aufträge zu schaffen und gleichzeitig die betriebliche Effizienz in verschiedenen Phasen der klinischen Studien zu erhalten.
mehr über diesen Bericht erfahren, kostenlos herunterladen
von Anwendungsbereich
klinische Studien bilden den größten Teil der Forschung durch ihre laufende Finanzierung, die unterstützt Drogen Entwicklungspipelines und europabasierte multinationale Forschungsstudien, die eine komplexe Durchführung benötigen. der Bereich der Drogenentwicklungsdienste unterhält seine Position, weil Biotech-Cluster eine verstärkte Finanzierung aus Risikokapital erfahren, die ihre frühe Forschungsarbeit unterstützt. die eu-medizinische Geräteregelung erfordert nun mehr Compliance-Arbeits- und Prüfverfahren, die zu einer erhöhten Nachfrage nach medizinischen Gerätetests geführt haben.
Sponsoren suchen nun Regulierungsdienste, weil sie Hilfe benötigen, um mehrere Genehmigungsverfahren zu navigieren, die in ihrem Geschäftsbetrieb existieren. der Forschungsbereich zeigt zunehmenden Fokus auf Präzisionsmedizin und seltene Krankheitsstudien, die verschiedene klinische Studienmethoden und spezifische Techniken zur Auswahl von Forschungsteilnehmern verlangen. Zukunftsentwicklungen werden dazu führen, dass Cros und Sponsoren durch adaptives Management von regulatorischen Anforderungen und Testtests enger zusammenarbeiten, die datengesteuerte Techniken für schnellere Prüfverfahren verwenden.
von Endverbraucher
der Endbenutzermarkt unterstützt Pharmaunternehmen, weil ihre umfangreichen klinischen Forschungsprogramme und laufende Bedürfnisse, um die operativen Kosten zu minimieren. Biotech-Firmen stellen die am schnellsten wachsende Gruppe dar, die von Outsourcing abhängig ist, weil sie keine ausreichenden internen Fähigkeiten haben und anpassbare Entwicklungsprozesse benötigen. medizinische Geräteunternehmen halten aufgrund strengererer Compliance-Anforderungen eine laufende Nachfrage aufrecht, während Forschungseinrichtungen durch ihre akademischen und staatlichen Forschungsprojekte Wissen fördern.
die verschiedenen Gruppen zeigen einzigartige Muster der Beteiligung, weil Pharmaunternehmen vorziehen, dauerhafte Partnerschaften zu etablieren, während Biotechnologie-Unternehmen müssen Operationen entwickeln, die sich schnell erweitern können. die zukünftige Forschungsrichtung wird stärkere Verbindungen zwischen cro-Fähigkeiten und Sponsor-Organisationsgröße herstellen, weil maßgeschneiderte Servicepakete und Risikoteilungsvereinbarungen Marktwettbewerb und Kundenbindungsmethoden bestimmen.
von Phase
Die drei Versuchsphasen bilden die Phase iii als Haupteinnahmequelle für Cros aufgrund ihrer umfangreichen Größe und teuren Operationen und ihrer entscheidenden Funktion bei der Erlangung der Zulassung. Der zunehmende Bedarf an Nachweis-of-concept-Studien und der Dosisoptimierungsforschung ermöglicht Phasen ii-Studien, ihren erheblichen Marktanteil zu erhalten. Die Zahl der Phase-I-Studien steigt weiter, weil mehr Biotech-Unternehmen neue Produkte schaffen und ihre ersten menschlichen Tests durchführen. die Nachfrage nach Phasen iv-Diensten steigt, weil die Unternehmen nach der Marktüberwachung im Rahmen neuer Sicherheitsüberwachungsvorschriften durchführen müssen.
die Nachfragemuster zeigen, dass spätere Phasentests komplexere Dienstleistungen benötigen, die dazu führen, dass Unternehmen ihre Arbeit auslagern und spezialisierte Expertise suchen. die Zukunft bringt neue adaptive Testdesigns zusammen mit dezentralen Methoden, die ändern, wie klinische Studien ihre Phasen verteilen, während sie nach schnelleren Wegen suchen, um alle Testphasen abzuschließen und ihre operative Leistung zu verbessern.
Was sind die wichtigsten Anwendungsfälle, die den europe Healthcare-Vertragsforschungsunternehmen Markt fahren?
die primäre Anwendung von klinischen Studienzentren auf ihre Durchführung, weil große pharmazeutische Unternehmen arbeiten Mehrländerphase ii und iii Studien nach europäischen Regulierungsanforderungen. die anspruchsvollste Anforderung ergibt sich aus diesem Anwendungsfall, weil es operative Tätigkeiten zwischen mehreren Zuständigkeiten, einschließlich Patientenrekrutierung und Standortmanagement und Compliance-Bedarf beinhaltet.
das Unternehmen hat seine Fähigkeiten entwickelt, um medizinische Gerätetests nach eu-medizinischer Geräteregelung zu unterstützen und regulatorische Beratungsleistungen für Biotech-Unternehmen in Erst-in-Menschen-Tests bereitzustellen. die kleinen und mittleren Biotech-Unternehmen wenden sich nun zu zwei Zwecken an cros, darunter die Suche nach ihren Genehmigungswegen und das Erreichen eines effizienten Wachstums während ihres frühen Entwicklungsprozesses.
die aufstrebenden Anwendungsfälle dezentraler Versuche beinhalten die Anwendung von Fernüberwachungswerkzeugen, während Real-Welt-Beweissstudien als Methoden für die Überwachung nach dem Markt funktionieren. die Modelle sind populärer geworden, weil Regulatoren begonnen haben, digitale Endpunkte zu akzeptieren, während Sponsoren jetzt schneller Zugang zu erheblichen Daten durch fortgeschrittene klinische Forschungsmethoden verfolgen.
Bericht Metriken | Details |
Marktgrößenwert 2025 | wirt 8,21 Milliarden |
Marktgrößenwert 2026 | 8.67 Milliarden |
Umsatzprognose 2033 | mit 12,7 Milliarden |
Wachstumsrate | cagr von 5,60% von 2026 bis 2033 |
Basisjahr | 2025 |
historische Daten | 2021 - 2024 |
Vorausschätzungszeitraum | 2026 - 2033 |
Berichterstattung | Umsatzprognose, Wettbewerbslandschaft, Wachstumsfaktoren und Trends |
Regionaler Geltungsbereich | europe (deutsch, vereinigtes Königreich, frankreich, italy, spain und rest von europe) |
Schlüsselunternehmen Profil | iqvia, labcorp, parexel, icon, syneos health, charles river, medpace, ppd, covance, wuxi apptec, pra health sciences, sgs, eurofins, envigo, clinipace |
Anpassungsbereich | freier Bericht Anpassung (Land, Region & Segment Bereich). nutzen Sie kundenspezifische Kaufoptionen, um Ihren genauen Forschungsanforderungen gerecht zu werden. |
Berichtsegmentierung | nach Typ (klinische Forschungsdienstleistungen, präklinische Dienstleistungen, Labordienstleistungen, andere), durch Anwendung (Drogenentwicklung, klinische Studien, medizinische Gerätetests, Regulierungsdienstleistungen, andere), durch Endverbraucher (Apotheken, Biotech-Firmen, medizinische Geräteunternehmen, Forschungsinstitute, andere), durch Phase (Phase i, Phase ii, Phase iii, Phase iv, andere)) |
welche Regionen treiben das europe Healthcare-Vertragsforschungsunternehmen Marktwachstum?
Western europe kontrolliert den europe Healthcare-Vertragsforschungsorganisationsmarkt, weil sein Regulierungssystem über die europäische Arzneimittelagentur und ihre klinischen Forschungseinrichtungen auf fortgeschrittenem Niveau arbeitet. die Länder Deutschlands und des vereinten Königreichs pflegen umfangreiche Netzwerke von Studienplätzen und akademischen Krankenhäusern zusammen mit qualifizierten Ermittlern. das etablierte System, das pharmazeutische Hauptquartier und Biotech Cluster sowie digitale Gesundheitsplattformen halten ständige Nachfrage nach Outsourcing. die Kombination von robusten Datenschutzsystemen und fortschrittlichen Gesundheitsnetzwerken ermöglicht Organisationen, komplexe internationale klinische Studien durchzuführen, die zahlreiche Länder zur Teilnahme benötigen.
Nordeuropa arbeitet als eine verlässliche Region, die Denmark und Finnland nutzt, um Patientenregisterintegration und Datenqualitätskontrolle zu priorisieren. Diese Region unterscheidet sich von Westeuropa durch ihren Fokus auf kleinere, aber hocheffiziente Studien, die von nationalen Gesundheitsdatenbanken und einheitlichen digitalen Systemen unterstützt werden. Cros erlebt stabile Betriebsbedingungen aufgrund regelmäßiger regulatorischer Compliance- und staatlich geförderter Forschungsentwicklungsinitiativen. das System pflegt Wachstum durch transparenten Patientendatenzugriff und hohe Beteiligung der öffentlichen Gesundheitsversorgung, die die Entwicklung ohne die grundlegenden betrieblichen Anforderungen anderer Systeme ermöglicht.
Eastern europe zeigt seine schnellste Entwicklungsrate durch seine jüngsten Investitionen in die klinische Infrastruktur zusammen mit der Einhaltung europäischer Regulierungsstandards. die Länder von poland hungary und romania haben verbesserte Standortfähigkeiten und reduzierte Genehmigung Zeitlinien seit 2020. Globale Sponsoren haben sich für die Durchführung der Studie entschieden, da die Kombination von geringeren Betriebskosten und schnellerer Patientenrekrutierung Effizienzgewinne mit sich bringt. die aktuelle Dynamik schafft mehrere Einstiegspunkte für Cros und Investoren, die Kapazität aufbauen möchten, während sie neue Marktnachfrage zwischen 2026 und 2033 erfassen.
wer sind die Schlüsselakteure im europe Healthcare Contract Research Organisation Markt und wie konkurrieren sie?
der europe Healthcare-Vertragsforschungsorganisation Markt Erfahrungen Wettbewerb, der zwischen zwei entgegengesetzten Markttrends der Konsolidierung und Spezialisierung besteht. global cros unterhält ihre Marktführerschaft mit ihren umfangreichen Geschäften und Komplettserviceangeboten und ihren etablierten Beziehungen zu Pharmaunternehmen, während mittelständische und Nischenunternehmen ihr spezifisches therapeutisches Wissen und regionales Know-how nutzen, um zu konkurrieren. Unternehmen konkurrieren nun über technologiebasierte Dienstleistungen, die bessere Ergebnisse liefern als ihre bisherigen kostenbasierten Methoden, weil Datenintegration und dezentrale Testsysteme und schnelle Ausführungsmethoden ihre Fähigkeit bestimmen, Verträge zu gewinnen. die digitale Plattform und die komplette Service-Erweiterung halten Marktanteil für etablierte Unternehmen, während Neuankömmlinge Marktstörungen, die sich auf seltene Krankheiten und frühen Studien durch ihren flexiblen Betrieb und Fachwissen konzentrieren.
die von iqvia entwickelten fortschrittlichen Analyse- und Echtzeit-Datenplattformen bieten Sponsoren die Werkzeuge, die sie benötigen, um adaptive Vorhersageversuche zu erstellen. Organisationen, die in ai-powered-Einsichten investieren und Partnerschaften mit Gesundheitsorganisationen entwickeln, verbessern ihre Fähigkeit, auf Daten zuzugreifen, was zu besseren Testergebnissen führt. icon plc bietet komplette Service-Lösungen, die die klinische Entwicklung mit der Healthcare-Intelligenz verbinden, durch seine mehrfachen Akquisitionen, um eine bessere Kontrolle über Projektpläne und Betriebskosten zu erhalten. parexel hilft Sponsoren, europäische regulatorische Anforderungen durch seine spezialisierte Beratungs- und Durchführungshilfe zu navigieren.
die Labcorp-Drogenentwicklungsorganisation nutzt ihre Laboreinrichtungen, um diagnostische Tests mit klinischen Testoperationen zu verknüpfen, was eine bessere Gestaltung von biomarkerbasierten Studien und Patientengruppen ermöglicht. syneos health bietet ein umfassendes Geschäftsmodell, das seine Dienstleistungen für die klinische Entwicklung mit dem Marktzugang über ein einziges System verbindet, das nahtlose Testdurchführung und Markteintrittslösungen bietet.
Firmenliste
- Iqvia
- Labcorp
- Parexel
- Symbol
- Syneos Gesundheit
- Der Fluss
- Medpac
- Seiten
- Covance
- wuxi apptec
- pra Gesundheitswissenschaften
- Sgs
- Eurofins
- Envigo
- Clinipac
aktuelle Entwicklungsnachrichten
im Oktober 2025 erweitert Thermo-Fischer klinische Studienleistungen über die Integration von Claario Akquisitionen: Thermo-Fischer wird aktiv seine Akquisition von clario Holdings, die Stärkung seiner europäischen klinischen Studiendaten und Analysen Dienstleistungen Footprint. clario ist spezialisiert auf die Erfassung und Verwaltung von klinischen Studiendaten – Kerninfrastruktur, die von cros in ganz Europa für fortgeschrittene Studien genutzt wird. der Deal wird voraussichtlich Anfang 2026 schließen.
Quelle: http://www.reuters.com
in april 2026, Thermo-Fischer zu tauchen Mikrobiologie Geschäft zu astorg: thermo fisher wissenschaftlich hat zugestimmt, sein Mikrobiologie-Geschäft an europäische Private Equity-Unternehmen zu verkaufen astorg in einem ~$1.075 Milliarden Deal. die Einheit unterstützt klinische und pharmazeutische Test-Workflows, die eng mit cro-enabled Labor-Services in Europa verbunden sind. die Bewegung spiegelt die kontinuierliche Konsolidierung der ausgelagerten klinischen Unterstützungsfähigkeiten in der Region wider.
Quelle: http://www.wsj.com
Welche strategischen Erkenntnisse definieren die Zukunft des europe Healthcare Contract Research Organisation Markt?
der europe Healthcare-Vertragsforschungsorganisationsmarkt verfolgt einen strukturellen Wandel zu plattformbasierten Systemen, die digitale Infrastruktur und reale Daten und dezentrale Testdurchführung nutzen, um Wettbewerbsvorteile zu schaffen. der grundlegende Treiber dieser Bewegung erfordert Organisationen, ihre Entwicklungszeiten zu verkürzen, während sie komplexe Therapien entwickeln, die große Mengen an Daten erfordern, um Behandlungen wie Biologik und personalisierte Medizin zu schaffen. der Markt wird sich in Richtung strategischer Zusammenarbeit bewegen, da Organisationen ihre Fähigkeiten entwickeln, um als komplette Daten- und Ausführungspartner zu dienen, die ihnen helfen, mehr Geld von Sponsoren zu erhalten.
die versteckte Gefahr der Datenfragmentierung zusammen mit unterschiedlichen Vorschriften über die Nutzung von Patientendaten schafft eine Gefahr, dass ai-getriebene Testmodelle in verschiedenen Ländern zu operieren kämpfen. Diese Einschränkung wird Hindernisse für internationale Normungsbemühungen schaffen, die die Effizienzvorteile verringern, die Organisationen durch ihre digitalen Transformationsinitiativen erreichen werden.
Eastern europe bietet eine neue Chance für die Hybrid-Studienerweiterung, da die Entwicklung von Infrastruktur und Regulierungsrahmen eine leichtere Patientenrekrutierung ermöglichen, die sich vergrößern lässt. Marktteilnehmer müssen digitale Plattformen entwickeln, die die Systeminteroperabilität zusammen mit der Einrichtung regionaler Standortnetze ermöglichen, um ihre Ziele zur Aufrechterhaltung des Datenzugangs zu erreichen und gleichzeitig die Einhaltung der Vorschriften und die operative Flexibilität zu gewährleisten.
europe Healthcare Contract Research Organisation Marktbericht Segmentierung
Typ
- klinische Forschungsleistungen
- Dienstleistungen
- Labordienstleistungen
- andere
durch Anwendung
- Entwicklung von Drogen
- klinische Studien
- Prüfung der medizinischen Geräte
- Regulierungsdienstleistungen
- andere
durch Endverbraucher
- Pharmaunternehmen
- Biotech-Unternehmen
- Medizinische Gerätefirmen
- Forschungsinstitute
- andere
durch Phase
- Phase i
- Phase ii
- Phase iii
- Phase iv
- andere
Häufig gestellte Fragen
Finden Sie schnelle Antworten auf die häufigsten Fragen.
die ungefähr europe gesundheit vertrag forschungsorganisation marktgröße für den markt wird im jahr 2033 mit 12,7 milliarden zu tun.
die wichtigsten segmente des europe healthcare contract research organisation markt sind nach typ (klinische forschungsdienstleistungen, preklinische dienstleistungen, labordienstleistungen, andere), durch anwendung (drug development, klinische studien, medizinische gerätetests, regulierungsdienstleistungen, andere), durch endbenutzer (apotheken, biotech-firmen, medizinische geräteunternehmen, forschungsinstitute, andere), durch phase (phase i, phase ii, phase iii, phase iv, phase iv, andere).
hauptakteure im europe healthcare-vertrag forschungsorganisation markt sind iqvia, labcorp, parexel, icon, syneos health, charles river, medpace, ppd, covance, wuxi apptec, pra health sciences, sgs, eurofins, envigo, clinipace.
die aktuelle marktgröße des europe healthcare-vertragsforschungsunternehmensmarktes beträgt 2025 8,21 milliarden.
der europe healthcare-vertragsforschungsorganisation markt cagr ist 5.60%.
- Iqvia
- Labcorp
- Parexel
- Symbol
- Syneos Gesundheit
- Der Fluss
- Medpac
- Seiten
- Covance
- wuxi apptec
- pra Gesundheitswissenschaften
- Sgs
- Eurofins
- Envigo
- Clinipac
Zuletzt veröffentlichte Berichte
-
Apr 2026
Markt für Cord Blood Banking Services
cord-blut-banking-dienste marktgröße, aktien- und analysebericht nach art des dienstes (sammlung, verarbeitung, lagerung), per banktyp (private banken, öffentliche banken und hybridbanken), durch komponente (bandblut und kordelgewebe), durch endbenutzer (krankenhäuser, forschungseinrichtungen, biotechnologie-unternehmen und andere) und geographie (nordamerika, europa, asien-pazifik, mittelost und afrika, süd- und zentralamerika), 2021
-
Apr 2026
Markt für ELISA-Prozessoren
elisa-prozessoren marktgröße, aktien- und analysebericht nach typ (optischer filter elisa-analyser, optische gitter elisa-analyser), nach modus (automatisierte elisa-analyser und semi-automatisierte elisa-analyser), nach anwendungen (immunologie, impfstoffentwicklung, drogenüberwachung und andere), von endnutzern (biotechnologie-unternehmen, pharmaunternehmen, vertragsforschungsorganisation, und diagnoselabors) und geographie (nordamerika, mittelamerika, mitteleuropa
-
Apr 2026
Markt für Mikroskop Slide Scanner
mikroskopische diascanner marktgröße, aktien- und analysebericht nach typ (portable mikroskop-disaster und desktop-mikroskop-disaster), durch anwendung (biologische forschung, medizin, tierarznei und andere) und geographie (nordamerika, europa, asien-pazifik, mittelost und afrika, süd- und zentralamerika), 2021 - 2031
-
Apr 2026
Markt für Mikrowellenherd
mikrowellenherd marktgröße, aktien- und analysebericht nach materialtyp (kunststoff, glas, keramik, silikon und metall), durch anwendung (kochen, nachwärmen und abtauen), durch endverbraucher (haushalt, gewerbe (restaurants, hotels und cafés) und lebensmittel-service-industrie), durch verkaufskanal (online-einzelhandel, offline-einzelhandel (supermärkte, supermärkte, spezialgeschäfte)


