Marktübersicht
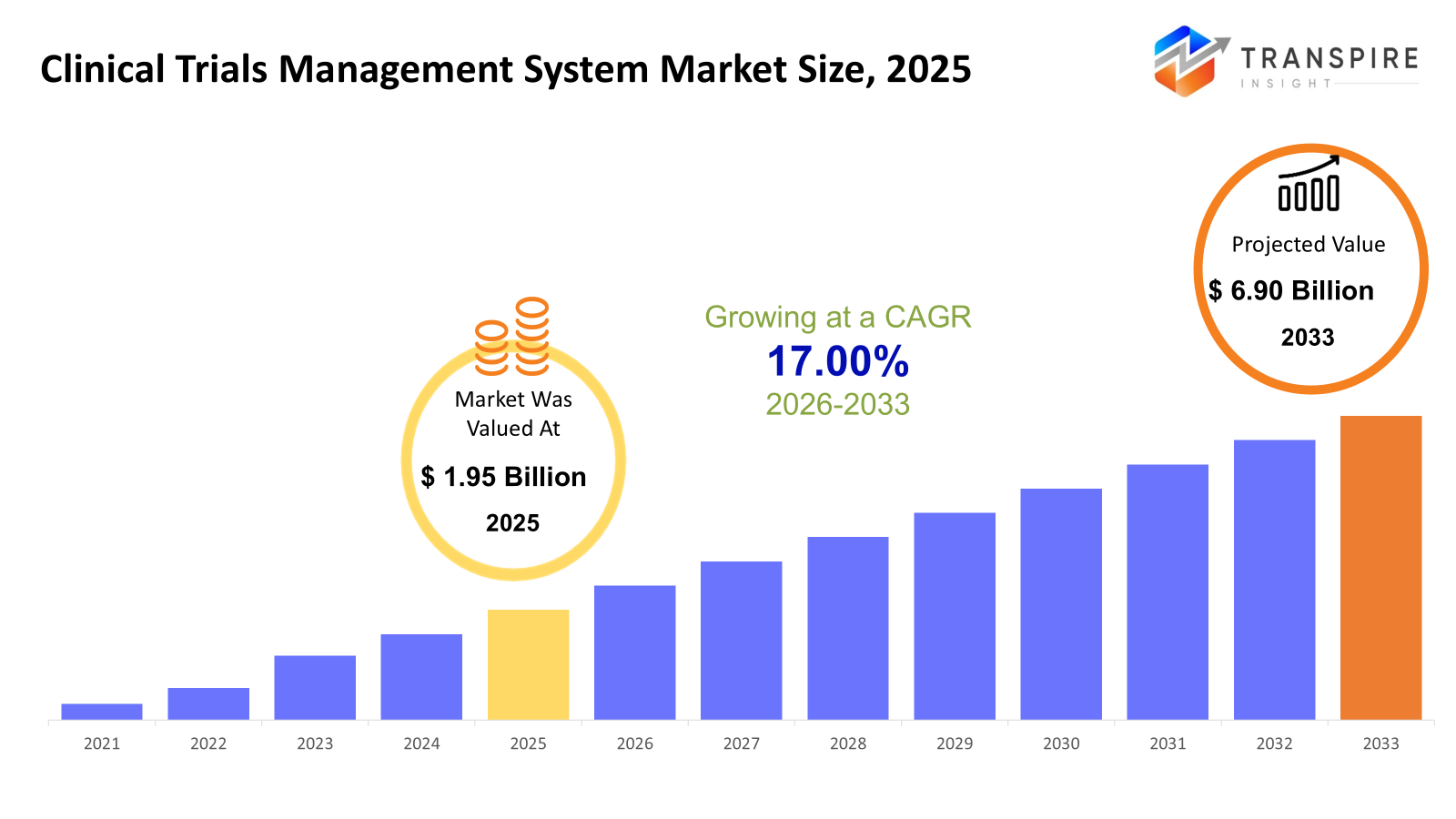
die globale klinische Studien Management System Marktgröße wurde bei usd 1,95 Milliarden im Jahr 2025 geschätzt und wird prognostiziert, um 6.90 Milliarden zu erreichen bis 2033, wächst bei einem cagr von 17.00% von 2026 bis 2033. Der Markt für ctms erlebt eine konsistente Wachstumsrate im Laufe der Zeit aufgrund von Faktoren wie steigenden V&D-Kosten in der Pharma- und Biotechnologieindustrie, steigender Anzahl klinischer Studien und der Einführung digitaler Technologien zur Durchführung klinischer Studien. Es wurde beobachtet, dass regulatorische Compliance und kosteneffiziente, zeitgemanagte klinische Studien auch die Markttreiber für die ctms-Industrie sind. Cloud-basierte Technologie in ctms bietet mehr Zugang und Zusammenarbeit an mehreren Standorten, wobei die Integration mit ai zum Marktwachstum beiträgt
Marktgröße und Prognose
- 2025 Marktgröße: benutzt 1,95 Milliarden
- 2033 projizierte Marktgröße: 6.90 Milliarden
- cagr (2026-2033): 17,00%
- Nordamerika: größter Markt im Jahr 2026
- asia pacific: am schnellsten wachsender Markt
mehr über diesen Bericht erfahren, kostenlos herunterladen
Analyse der Markttendenzen
- Nord-Amerika fungiert als wichtiges Zentrum für die Umsetzung von ctms, aufgrund anspruchsvoller Gesundheit Infrastruktur, FuE-Ausgaben von Pharmaunternehmen und die Anwesenheit von Cros, um Studien über verschiedene Standorte in uns, Kanada und Mexiko zu verwalten
- einheitliche Staaten ist der Schlüsselmarkt in der nordamerikanischen Region aufgrund der zunehmenden Entwicklung der Technologie, eines harten Regulierungssystems im Land und der Praxis der Auslagerung von klinischen Testdaten an cros, um die Zeitlinie zu verkürzen und die operative Effizienz zu verbessern
- der asia pacific Markt stellt einen wachsenden Markt aus unterstützenden regulatorischen Umgebungen, zunehmende Outsourcing-Aktivitäten in Low-Cost-Länder, und die steigenden klinischen Studien in Indien, China, Japan und Südkorea
- Cloud-basiertes Bereitstellungsmodell wird als auf dem Vormarsch betrachtet, da Unternehmen auf der Suche nach Lösungen sind, die Skalierbarkeit bieten und somit Kosten sparen, während sie die Fernbedienung erleichtern, die Kosten senken und in Echtzeit über geografisch verteilte Umgebungen auf Testdaten zugreifen.
- es führt auch Anwendungen, da es für Genauigkeit, Integrität und regulatorische Einhaltung von Testdaten sorgt, eine Schlüsselkomponente, die schnellere Drogenzulassungen sowie eine effektive Überwachung von Mehrphasenversuchen gewährleistet.
- Pharmazeutika und Biotech-Unternehmen gelten als Endbenutzer von ctms aufgrund ihrer hohen Investitionen in r&d, innovative Kultur und benötigen eine integrierte ctms-Lösung, um komplexe globale klinische Studien effektiv durchzuführen.
so, die klinische Studien Management System Markt soll den Prozess der Planung, Durchführung und Verfolgung von klinischen Studien für Pharma-, Biotechnologie- und Forschungseinrichtungen vereinfachen. der Umfang der klinischen Studienmanagement-Software und -Dienste unterstützen das klinische Studiendatenmanagement, die rechtliche Compliance, die Registrierung und das Standortmanagement, um den Prozess zu optimieren und Zeit zu sparen. die zunehmenden Komplexität der klinischen Studien und die Notwendigkeit einer effizienten Operation an verschiedenen Standorten auf der ganzen Welt haben zur zunehmenden Popularität der klinischen Studien Management System Software geführt, um die Genauigkeit in dem Prozess zu gewährleisten. die Verwendung von Cloud Computing wurde als die am meisten bevorzugte Technologie erkannt, um klinische Studien Management-System aufgrund seiner Wirksamkeit, Zugänglichkeit und Kostenvorteile, insbesondere bei Cros und multinationalen Pharmaunternehmen einzusetzen. der zunehmende Druck, Patienten in klinischen Studien zu halten und den Prozess der Arzneimittelzulassungen zu beschleunigen, haben zur zunehmenden Popularität des klinischen Studienmanagementsystems beigetragen. die Bedeutung des klinischen Studienmanagementsystems wird durch seine Verwendung als wesentliches Instrument bei der Optimierung globaler klinischer Forschungsanstrengungen belegt.
klinische Studien Management System MarktSegmentierung
durch Komponente
- Software
die in diesem Segment am dominantsten Software ist ctms, da dies bei der effizienten Verwaltung von klinischen Studien, der Datenerhebung und der Einhaltung regulatorischer Anforderungen hilft. es hilft bei der effizienten Entscheidungsfindung mittels Analytik und stellt Berichte in Echtzeit zur Verfügung, wodurch die Produktivität erhöht wird.
- Dienstleistungen
Dienstleistungen, einschließlich Implementierungs-, Schulungs- und Support-Services, ergänzen die Software-Adoption, indem Sie eine einfache Integration mit der vorhandenen Infrastruktur gewährleisten. die Bedeutung von Managed Services und Consulting kann nicht überschätzt werden, vor allem für Unternehmen, die kein eigenes Know-how besitzen und dadurch das Wachstum in dieser Branche fördern.
durch den Einsatzmodus
- On-Premise
on-premise ctms-Lösungen bleiben bei großen Pharmaunternehmen und Cros bevorzugt, die eine vollständige Kontrolle über Datensicherheit und Anpassung benötigen. Während diese höhere Kosten haben, sind sie mit Integrationen verbunden, die ältere Systeme beinhalten und die Einhaltung strenger regionaler Datenvorschriften bieten.
- Cloud-basiert
Skalierbarkeit, geringere anfängliche Investitionen und Fernzugriffsmöglichkeit sind wichtige Features, die das schnelle Wachstum von Cloud-basierten Ctms-Lösungen vorantreiben. sie ermöglichen Echtzeit-Zusammenarbeit über mehrere Test-Websites. So ist es ideal für globale klinische Studien, insbesondere wenn multiregionale Forschungsstudien und Schwellenmärkte betrachtet werden.
mehr über diesen Bericht erfahren, kostenlos herunterladen
durch Anwendung
- klinische Datenverwaltung
Dies ist ein wesentlicher Abschnitt, weil es verwendet wird, um die Genauigkeit der klinischen Studiendatenerhebung und -speicherung zu validieren. die effektive Verwaltung von klinischen Daten minimiert nicht nur Fehler, sondern erleichtert auch schnelle Arzneimittelzulassungen.
- Regulierungsbehörden
Management-Tools für regulatorische Compliance ermöglichen Organisationen, internationale Standards und Verordnungen, wie fda, ema, und ich-gcp. Automatisierung der Berichterstattung und Überwachung von Compliance-Risiken hat es unerlässlich gemacht, insbesondere für globale klinische Studienoperationen.
- Testplanung & Management:
Dieses Teilsegment hilft bei der effizienten Planung und Planung über verschiedene Standorte. die analytischen Fähigkeiten helfen, die benötigten Kosten und Zeit vorherzusagen, wodurch die Effizienz erhöht und die Betriebskosten gesenkt werden.
- Standortverwaltung
Lösungen im Standortmanagement helfen bei der Standort-Koordination, Patienteneinschreibungsoptimierung sowie Leistungsüberwachung. Dies schafft das Bewusstsein unter Sponsoren und Cros, um Testergebnisse zu verbessern und Website-Protokoll zu erhalten.
- Personalrekrutierung und Retention
Dieses Segment befasst sich mit einigen der größten Herausforderungen, denen die klinischen Studien heute gegenüber stehen, nämlich der rechtzeitigen Probeeinschreibung und der Patientenkonformität. Diese Rekrutierungsanalysen, Engagements und Strategie-Tools helfen nicht nur bei der Senkung der Ausfallquoten, sondern auch bei der Sicherstellung des Testerfolgs.
von Endbenutzer
- Pharma- und Biotechnologieunternehmen
Diese Organisationen fördern die Annahme von ctms aufgrund hoher FuE-Aufwendungen und der Notwendigkeit effizienter Testoperationen. Diese Organisationen haben hohe Standards für Innovation und Compliance und erfordern ein effizientes und innovatives ctms-System, das hilft, komplizierte, mehrphasige Versuche durchzuführen.
- Kontraktforschungsorganisationen (cros)
cros verlassen sich auf ctms für die effiziente Verwaltung verschiedener Studien für Kunden. Cloud-basierte und skalierbare Lösungen helfen dabei, verschiedene Prozesse in verschiedenen Regionen zu standardisieren, eine präzise Berichterstattung zu gewährleisten und hohe Standards für regulatorische Zwecke zu erhalten.
- Wissenschafts- und Forschungseinrichtungen
Wissenschafts- und Forschungsinstitute nutzen ctms-Systeme zur Durchführung von Stipendien-geförderten Studien sowie investigatorinitiierte Studien. ctms-Systeme, die Kosteneffizienz, Einfachheit und Genauigkeit betonen, ermöglichen es, kleinere Studien durchzuführen, während die Einhaltung der institutionellen oder nationalen Richtlinien.
- Kliniken und Krankenhäuser
ctms wird von Krankenhäusern und Kliniken verwendet, um klinische Studien neben ihren regelmäßigen Operationen zu verwalten. Die Integration mit Patientenaufzeichnungen und Patientenangriffswerkzeugen erleichtert die Verwaltung und Minimierung der Verwaltungslast.
regionale Erkenntnisse
Nord-Amerika steht zuerst auf dem Markt. die vereinigten Staaten von Amerika, Kanada und Mexiko sind die wichtigsten Beitragsländer auf dem Markt aufgrund günstiger pharma r&d-Ausgaben, regulatorischer Umgebung und der Anwesenheit von großen Cros. europe umfasst große Ländersegmente wie Germany, uk, france, spain, und italy. Diese Ländersegmente zeugen von einem stetigen Wachstum, das durch regulatorische Compliance, Digitalisierung und Modernisierung ihrer jeweiligen Infrastruktur bedingt ist. asia pacific tritt als ein schnell wachsender Markt auf, der von Landsegmenten wie Indien, China, Japan, Südkorea und Australien aufgrund kostengünstiger klinischer Studien, erhöhter Outsourcing-Aktivitäten und landesweiten Regierungsinitiativen zur Förderung von Forschungsaktivitäten angetrieben wird. Südamerica umfasst Ländersegmente wie Brazil und Argentinien. Diese Ländersegmente nehmen langsam ctms mit Motiven an, um Kosten zu optimieren und klinische Studien durchzuführen. die mittlere Ost- und Afrika umfasst Ländersegmente wie saudi arabia, uae, südafrika. Diese Ländersegmente werden aufgrund wachsender infrastruktureller Ausgaben und klinischer Forschungsaktivitäten als auf dem Markt ankommend angesehen. ctms scheint von ihnen zu begünstigen, multi-site klinischen Studien mit Hilfe von Cloud-Infrastruktur aufgrund der geographischen Einschränkung von verteilten Teams zu verwalten.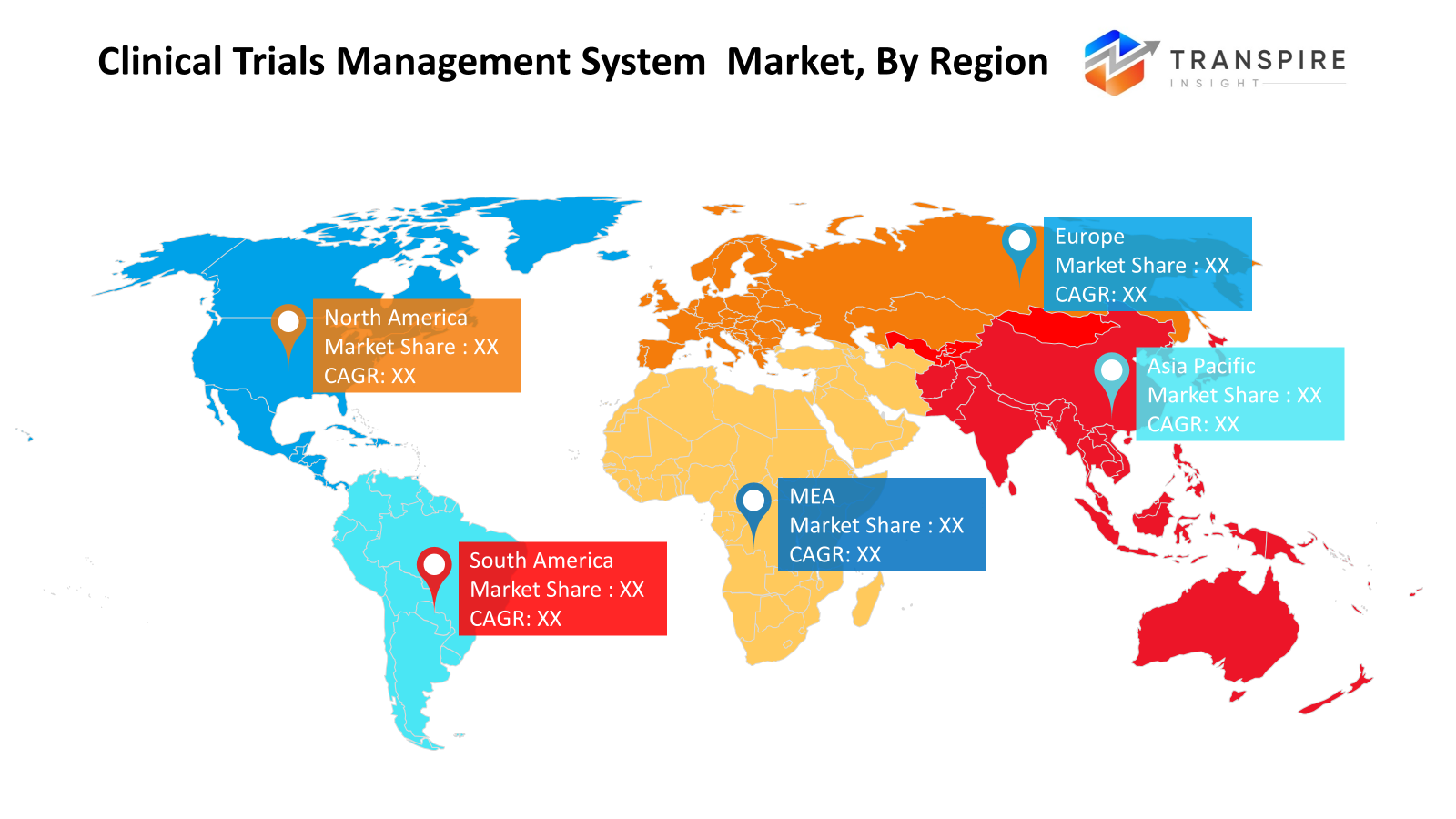
mehr über diesen Bericht erfahren, kostenlos herunterladen
aktuelle Entwicklungsnachrichten
- August 2025, Sowohl iqvia- als auch veeva-Systeme kündigten eine langfristige globale klinische und kommerzielle Partnerschaft an, die alle herausragenden Rechtsstreitigkeiten zwischen den Parteien festlegt und die nahtlose Integration sowohl der Software-, Daten- und Dienstleistungsangebote beider Unternehmen zu ihren Life Sciences-Kunden gewährleistet. Dies ermöglicht es den Kunden, die Anwendungen und Dienstleistungen sowohl des Unternehmens mit Lösungen im klinischen und kommerziellen Raum von dem anderen angeboten zu nutzen, um Verbesserungen in der klinischen und kommerziellen Effizienz zu ermöglichen.
- im Januar 2025, veeva-Systeme, inc. berichtete mehr als 200 Unternehmen, darunter 17 der Top 20 biopharmazeutischen Unternehmen, verwenden jetzt veeva ctms, um schnellere, effizientere klinische Studienoperationen zu fahren. die Pressemitteilung sagt, es sollte die Fähigkeit zur verbesserten Daten-Zentralisierung, optimierte Workflows, automatisierte Transfers zwischen Cros und Sponsoren, und neue Produktinnovationen regelmäßig über kundenorientierte Releases geliefert werden, um sowohl insourced als auch ausgelagerte klinische Test-Betriebsmodelle zu unterstützen.
(Quelle:https://www.veeva.com/resources/more-than-200-companies-advance-trial-management-with-veeva-ctms)
Bericht Metriken | Details |
Marktgrößenwert 2025 | usd 1,95 Milliarden |
Marktgrößenwert 2026 | 2.30 Milliarden |
Umsatzprognose 2033 | 6.90 Milliarden |
Wachstumsrate | cagr. 17,00% von 2026 bis 2033 |
Basisjahr | 2025 |
historische Daten | 2021 – 2024 |
Vorausschätzungszeitraum | 2026 – 2033 |
Berichterstattung | Umsatzprognose, Wettbewerbslandschaft, Wachstumsfaktoren und Trends |
Regionaler Geltungsbereich | Nord-Amerika; europe; asia pacific; latin america; mittelost & africa |
Länderumfang | vereinigte Staaten; canada; mexico; vereinigtes Königreich; germany; france; italy; spain; denmark; sweden; norway; china; japan; india; australia; Südkorea; thailand; brazil; argentina; Südafrika; saudi arabia; vereinigt arab emirates |
Schlüsselunternehmen Profil | medidata solutions, oracle Corporation, veeva systems, iqvia inc., dassault systèmes, parexel international, ibm watson health, clario, revity, wcg medical, bioclinica, arisglobal llc, datatrak international, mastercontrol inc., mednet solutions inc. |
Anpassungsbereich | freier Bericht Anpassung (Land, Region & Segment Bereich). nutzen Sie kundenspezifische Kaufoptionen, um Ihren genauen Forschungsanforderungen gerecht zu werden. |
Berichtsegmentierung | durch Komponente (Software, Dienstleistungen), durch Bereitstellungsmodus (auf Prämisse, Cloud-basiert), durch Anwendung (klinisches Datenmanagement, Compliance-Management, Testplanung & Management, Standortmanagement, Patientenrekrutierung & Retention) und durch Endbenutzer (Apotheken- & Biotechnologie-Unternehmen, Vertragsforschungsorganisationen (cros), akademische & Forschungsinstitute, Krankenhäuser & Kliniken) |
wichtige klinische Studien Management System Unternehmenseinsichten
medidata-Lösungen gelten als einer der führenden Anbieter von ctms sowie Cloud-basierte integrierte eklinische Systeme für klinische Studien weltweit. es bietet seinen Nutzern End-to-End-Funktionalitäten wie Planung, rechtzeitiges Datenmanagement, Analytik und Berichterstattung, die Entscheidungsprozesse optimieren können. Die Integration von medidata mit vielen Systemen, einschließlich edc-Systemen sowie patientenzentrierten Systemen, ist recht breit. dies ist von immenser Bedeutung, da es sowohl qualitativ hochwertige Daten als auch schnellere Zeitlinien sicherstellt. Darüber hinaus hat Innovation durch ai-Fähigkeiten sowie hochentwickelte Monitoring-Tools medidata zu einem der führenden Spieler gemacht. ihre Lösungen werden von großen Pharma- und Biotechnologie-Unternehmen durch ihren Fokus auf Geschwindigkeit und Innovation gesucht.
Schlüssel klinische Studien Management System Unternehmen:
- Medidata Lösungen
- Oracle Corporation
- Veeva Systeme
- iqvia inc.
- Das ist das erste Mal.
- parexel international
- ibm watson Gesundheit
- Clario
- Wiederbelebung
- wcg klinisch
- Biozid
- arisglobale llc
- datatrak international
- Mastercontrol inc.
- mednet lösungen inc.
global klinische Studien Management System Markt Bericht Segmentierung
durch Komponente
- Software
- Dienstleistungen
durch den Einsatzmodus
- On-Premise
- Cloud-basiert
durch Anwendung
- klinische Datenverwaltung
- Regulierungsbehörden
- Prozessplanung und -management
- Standortverwaltung
- Personalrekrutierung und Retention
von Endbenutzer
- Pharma- und Biotechnologieunternehmen
- Kontraktforschungsorganisationen (cros)
- Wissenschafts- und Forschungsinstitute
- Kliniken und Krankenhäuser
Regionalaussichten
- Nordamerika
- vereinigte Staaten
- Canada
- Mexiko
- europe
- Deutschland
- vereinigtes Königreich
- Franken
- Spaten
- Italy
- Rest von europe
- Asia pazifisch
- Japan
- China
- australia & neue zealand
- Südkorea
- indien
- rest von asia pacific
- Südamerika
- Brasilien
- Argentinien
- Rest von Süd-Amerika
- Mittelost & Afrika
- Saudi arabien
- vereinigte arabische Emirate
- Südafrika
- Rest des mittleren Ostens & Afrika
Häufig gestellte Fragen
Finden Sie schnelle Antworten auf die häufigsten Fragen.
die ungefähren klinischen studien management system marktgröße für den markt wird im jahr 2033 6,90 milliarden verwendet werden.
schlüsselsegmente für den klinischen studienmanagement-systemmarkt durch komponente (software, dienstleistungen), durch bereitstellungsmodus (on-premise, cloud-basiert), durch anwendung (klinisches datenmanagement, regulatorisches compliance management, testplanung & management, standortmanagement, patientenrekrutierung & retention) und durch endbenutzer (pharmazeutische & biotechnologische unternehmen, vertragsforschungsorganisationen (cros), akademische & forschungsinstitute, krankenhäuser & kliniken & kliniken).
wichtige klinische studien management system markt spieler sind medidata lösungen, oracle corporation, veeva systeme, iqvia inc, parexel international.
die region nord-amerika führt den markt für klinische studienmanagementsystem.
der markt für klinische studienmanagementsystem ist 17,00%.
- Medidata Lösungen
- Oracle Corporation
- Veeva Systeme
- iqvia inc.
- Das ist das erste Mal.
- parexel international
- ibm watson Gesundheit
- Clario
- Wiederbelebung
- wcg klinisch
- Biozid
- arisglobale llc
- datatrak international
- Mastercontrol inc.
- mednet lösungen inc.
Zuletzt veröffentlichte Berichte
-
Apr 2026
Markt für AI in Diabetische Retinopathie
ai in diabetic retinopathy market size, share & analysis report by type (screening ai systems, diagnostische ai-systeme und prognostizierende ai-modelle), durch anwendungssegment (krankenhäuser, augenheilkliniken, diagnostische zentren und forschung und entwicklung), und geographie (nordamerika, europa, asien-pazifik, mittelost und afrika, süd- und zentralamerika), 2021
-
Apr 2026
Markt für Psychologische Tests
psychometrische tests marktgröße, aktien- und analysebericht nach typ (persönlichkeitstests, eignungstests, fähigkeiten/wissenstests und andere), durch anwendung (talent akquisition und talent management), und geographie (north america, europe, asia-pacific, middle east and africa, south and central america), 2021 – 2031
-
Apr 2026
Markt für Seltene biologische Sammlung
seltene biologische probensammlung marktgröße, aktien- und analysebericht nach typ (isolationskits & reagenz, blutentnahmeröhren u.a.), durch anwendung (onkologie, transkriptomik, pharmakogenomics u.a.) und geographie (nordamerika, europa, asien-pazifik, mittelosten und afrika, süd- und zentralamerika), 2021 – 2031
-
Apr 2026
Markt für Anhänger für den Aufzug
patientenlift-anhängermarkt nach produkttyp (verdrahtete anhänger, kabellos, programmierbar), nach betriebsart (manuell, elektrisch), durch endbenutzer (gesundheitsprofis, patienten), durch anwendung (krankenhäuser, heimpflege, rehabilitationszentren, andere), durch industrieanalyse, größe, anteil, wachstum, trends und prognosen 2021-2033
Unsere Kunden
.jpg)









